![]() — Все документы — ГОСТы — ГОСТ Р ИСО 18363-3-2019 ЖИРЫ И МАСЛА ЖИВОТНЫЕ И РАСТИТЕЛЬНЫЕ. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ СЛОЖНЫХ ЭФИРОВ ЖИРНЫХ КИСЛОТ МОНОХЛОРПРОПАНДИОЛОВ (МХПД) И ГЛИЦИДОЛА С ПРИМЕНЕНИЕМ ГХ/МС. Часть 3. МЕТОД С ИСПОЛЬЗОВАНИЕМ КИСЛОТНОЙ ПЕРЕЭТЕРИФИКАЦИИ И ИЗМЕРЕНИЕ СОДЕРЖАН
— Все документы — ГОСТы — ГОСТ Р ИСО 18363-3-2019 ЖИРЫ И МАСЛА ЖИВОТНЫЕ И РАСТИТЕЛЬНЫЕ. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ СЛОЖНЫХ ЭФИРОВ ЖИРНЫХ КИСЛОТ МОНОХЛОРПРОПАНДИОЛОВ (МХПД) И ГЛИЦИДОЛА С ПРИМЕНЕНИЕМ ГХ/МС. Часть 3. МЕТОД С ИСПОЛЬЗОВАНИЕМ КИСЛОТНОЙ ПЕРЕЭТЕРИФИКАЦИИ И ИЗМЕРЕНИЕ СОДЕРЖАН
ГОСТ Р ИСО 18363-3-2019 ЖИРЫ И МАСЛА ЖИВОТНЫЕ И РАСТИТЕЛЬНЫЕ. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ СЛОЖНЫХ ЭФИРОВ ЖИРНЫХ КИСЛОТ МОНОХЛОРПРОПАНДИОЛОВ (МХПД) И ГЛИЦИДОЛА С ПРИМЕНЕНИЕМ ГХ/МС. Часть 3. МЕТОД С ИСПОЛЬЗОВАНИЕМ КИСЛОТНОЙ ПЕРЕЭТЕРИФИКАЦИИ И ИЗМЕРЕНИЕ СОДЕРЖАН
Добавил:
Дата: [13.01.2021]
Animal and vegetable fats and oils. Determination of fatty-acid-bound chloropropanediols (MCPDs) and glycidol by GC/MS. Part 3. Method using acid transesterification and measurement for 2-MCPD, 3-MCPD and glycidol
ОКС 67.200.10
Дата введения - 1 февраля 2020 г.
Введен впервые
Предисловие
1 Подготовлен Некоммерческой организацией "Ассоциация производителей и потребителей масложировой продукции" на основе собственного перевода на русский язык англоязычной версии стандарта, указанного в пункте 4
2 Внесен Техническим комитетом по стандартизации ТК 238 "Масла растительные и продукты их переработки"
3 Утвержден и введен в действие Приказом Федерального агентства по техническому регулированию и метрологии от 19 декабря 2019 г. N 1414-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 18363-3:2017 "Животные и растительные жиры и масла. Определение содержания сложных эфиров жирных кислот монохлорпропандиолов (МХПД) и глицидола с применением ГХ/МС. Часть 3. Метод с использованием кислотной переэтерификации и измерение содержания 2-МХПД, 3-МХПД и глицидола" [ISO 18363-3:2017 "Animal and vegetable fats and oils - Determination of fatty-acid-bound chloropropandiols (MCPDs) and glycidol by GC/MS - Part 3: Method using acid transesterification and measurement for 2-MCPD, 3-MCPD and glycidob, IDT].
При применении настоящего стандарта рекомендуется использовать вместо ссылочного международного стандарта соответствующий ему национальный стандарт, сведения о котором приведены в дополнительном приложении ДА
5 Введен впервые
Введение
ИСО 18363 представляет собой серию международных стандартов, которые могут быть использованы для определения содержания сложных эфиров жирных кислот монохлорпропандиола (МХПД) и глицидола. В настоящее время действуют три международных стандарта, и данное введение является описанием методов, которые могут быть использованы специалистами для определения того, какие методы являются наиболее подходящими. Подробное описание применения каждого метода содержится в области применения соответствующего метода.
Международный стандарт ИСО 18363 состоит из следующих частей под общим названием "Животные и растительные жиры и масла. Определение содержания сложных эфиров жирных кислот монохлорпропандиолов (МХПД) и глицидола с применением ГХ/МС":
- часть 1. Метод с использованием быстрой щелочной переэтерификации и измерения содержания 3-МХПД и дифференциальное измерение содержания глицидола;
- часть 2. Метод с использованием медленной щелочной переэтерификации и измерение содержания 2-МХПД, 3-МХПД и глицидола;
- часть 3. Метод с использованием кислотной переэтерификации и измерение содержания 2-МХПД, 3-МХПД и глицидола.
Первая часть международного стандарта ИСО 18363 [7] представляет собой дифференциальный метод, эквивалентный стандарту DGF C-VI 18 (10) и идентичный официальному методу AOCS Cd 29с-13. Метод основан на быстром щелочном каталитическом выделении 3-МХПД и глицидола из производных сложных эфиров. Затем глицидол преобразуется в индуцированный 3-МХПД. Он состоит из двух частей. Первая часть (А) позволяет определить сумму связанного эфира 3-МХПД и глицидола, тогда как вторая часть (В) определяет только связанный эфир 3-МХПД. Оба определения основаны на выделении меченных изотопами соединений 3-МХПД и глицидола из формы связанного эфира с применением алкоголиза с щелочным катализатором, проводимым при комнатной температуре. В части А подкисленный раствор хлорида натрия используется для прекращения реакции и последующего преобразования глицидола в индуцированный 3-МХПД. Таким образом, в части А 3-МХПД и глицидол становятся неразличимыми. В части В остановка реакции достигается добавлением свободного от хлора подкисленного соляного раствора, который также предотвращает преобразование глицидола в индуцированный МХПД. Таким образом, часть В позволяет определить действительное содержание 3-МХПД. Наконец, содержание глицидола в образце пропорционально разности обоих определений (А, В) и может быть вычислено после определения коэффициента преобразования глицидола в 3-МХПД. Первая часть международного стандарта ИСО 18363 применима для быстрого определения связанного эфира 3-МХПД и глицидола в рафинированных и нерафинированных растительных маслах и жирах. Первая часть международного стандарта ИСО 18363 может применяться к животным жирам, а также к маслам и жирам после жарки, но перед анализом данных образцов необходимо провести валидационное исследование. Любые свободные соединения, содержащиеся в образце, будут включены в результаты, так как эталон не позволяет различать свободные и связанные соединения. Однако на момент публикации этого документа исследования не показали каких-либо доказательств содержания свободного соединения в том же количестве, что и содержание этерифицированного соединения в растительных маслах и жирах. Первая часть международного стандарта ИСО 18363 может быть изменена таким образом, чтобы определение 2-МХПД стало возможным, но опять же перед анализом данного соединения необходимо провести валидационное исследование.
Вторая часть международного стандарта ИСО 18363 для определения связанных эфиров МХПД и глицидола представляет собой официальный метод AOCS Cd 29b-13. Метод основан на медленном щелочном высвобождении МХПД и глицидола из сложных эфиров. Затем глицидол преобразуется в 3-монобромпропандиол (3-МБПД). Вторая часть международного стандарта ИСО 18363 подразумевает подготовку двух образцов, что отличается от используемых внутренних стандартов. Обе части могут использоваться для определения связанных эфиров 2-МХПД и 3-МХПД. В части А определяется предварительный результат для связанного эфира глицидола. Поскольку 3-МХПД, присутствующий в образце, будет в какой-то степени преобразован в индуцированный глицидол при приготовлении образца, часть В служит для количественного определения доли индуцированного глицидола, который затем вычитается из предварительного количества глицидола, полученного в части А. Используя меченные изотопами свободные МХПД-изомеры в пробе А и меченные изотопами связанные эфиры 2-МХПД и 3-МХПД в части В, можно контролировать эффективность расщепления сложного эфира. Оба определения, А и В, основаны на выделении определяемых соединений 2-МХПД, 3-МХПД и глицидола из связанной (этерифицированной) формы медленным алкоголизом с щелочным катализатором в холодных условиях. При подготовке обоих образцов реакцию останавливают добавлением подкисленного концентрированного раствора бромида натрия для преобразования нестабильного и летучего глицидола в 3-МБПД, который демонстрирует свойства, сопоставимые с 3-МХПД в отношении его стабильности и хроматографических характеристик. Кроме того, основной избыток ионов бромида предотвращает нежелательное образование 3-МХПД из глицидола в случае с образцами, которые содержат определенное природное количество хлорида. Вторая часть международного стандарта ИСО 18363 применима для определения связанных эфиров 3-МХПД, 2-МХПД, также глицидола в рафинированных и нерафинированных растительных маслах и жирах. Вторая часть международного стандарта ИСО 18363 может применяться к животным жирам, а также к маслам и жирам после жарки, но перед анализом этих образцов необходимо провести валидационное исследование. Любые свободные соединения, содержащиеся в образце, будут включены в результаты, но стандарт не позволяет различать свободные и связанные соединения. Однако на момент публикации этого документа исследования не показали каких-либо доказательств содержания свободного соединения в том же количестве, что и содержание этерифицированного соединения в растительных маслах и жирах.
Данная часть международного стандарта ИСО 18363 для определения связанного эфира МХПД и глицидола представляет собой официальный метод AOCS Cd 29а-13. Метод основан на преобразовании глицидиловых сложных эфиров в эфиры 3-МБПД и медленном кислотном каталитическом высвобождении МХПД и МБПД из сложных эфиров. Данная часть международного стандарта основана на подготовке одного образца, в котором сложные глицидиловые эфиры преобразовываются в моноэфиры МБПД, а затем свободные соединения 2-МХПД, 3-МХПД и 3-МБПД высвобождаются медленным алкоголизом с кислотным катализатором. 3-МБПД представляет собой истинное содержание связанного глицидола. Третья часть международного стандарта ИСО 18363 может применяться для определения связанных эфиров 3-МХПД, 2-МХПД, а также глицидола в рафинированных и нерафинированных растительных маслах и жирах. Третья часть международного стандарта ИСО 18363 может применяться к животным жирам, а также к маслам и жирам после жарки, но перед анализом этих образцов необходимо провести валидационное исследование. Данный метод подходит для анализа связанных (этерифицированных) определяемых соединений, но при необходимости этот метод может быть также выполнен без первоначального преобразования глицидиловых эфиров. В таком случае результаты будут включать как свободные, так и связанные формы 2-МХПД и 3-МХПД, а количество свободных соединений может быть рассчитано как разница между двумя результатами, определенными в обоих определениях. Однако на момент публикации этого документа исследования не показали каких-либо доказательств того, что содержание свободного определяемого соединения столь же высоко, как и содержание этерифицированного определяемого соединения в растительных маслах и жирах.
Настоящий стандарт устанавливает процедуру одновременного определения сложных эфиров 2-МХПД (связанного 2-МХПД), 3-МХПД (связанного 3-МХПД) и глицидиловых эфиров (связанный глицидол) в одной пробе на основе кислотного каталитического расщепления сложного эфира и преобразования расщепленных (свободных) соединений с фенилборной кислотой (ФБК) перед анализом газовой хроматографии/масс-спектрометрии (ГХ/МС).
Настоящий стандарт применим для твердых и жидких масел и жиров. Для каждого из трех определяемых соединений предел количественного определения (LOQ) составляет 0,1 мг/кг, а нижний предел чувствительности (LOD) - 0,03 мг/кг.
В настоящем стандарте использованы нормативные ссылки на следующие стандарты. Для датированных ссылок применяют только указанное издание ссылочного стандарта, для недатированных - последнее издание (включая все изменения к нему):
ISO 3696, Water for analytical laboratory use - Specification and test methods (Вода для лабораторного анализа. Технические требования и методы испытаний)
В настоящем стандарте применены следующие термины с соответствующими определениями.
Международная организация по стандартизации (ИСО) и Международная электротехническая комиссия (МЭК) ведут терминологические базы данных для использования в области стандартизации, доступ к которым можно получить по следующим адресам:
- МЭК Электропедия: доступна по адресу http://www.electropedia.org/;
- платформа интернет-поиска ИСО: доступна по адресу https://www.iso.org/obp.
3.1 связанный 2-МХПД (bound 2-MCPD): Количество 2-МХПД, высвобожденного из сложного эфира (связанной формы) путем переэтерификации, катализируемой кислотой, в соответствии с методом стандарта.
Примечание - Содержание связанного 2-МХПД рассчитывается и выражается в миллиграммах на килограмм (мг/кг).
3.2 связанный 3-МХПД (bound 3-MCPD): Количество 3-МХПД, высвобожденного из сложного эфира (связанной формы) путем переэтерификации, катализируемой кислотой, в соответствии с методом стандарта.
Примечание - Содержание связанного 3-МХПД рассчитывается и выражается в миллиграммах на килограмм (мг/кг).
3.3 связанный глицидол (bound glycidol): Количество глицидола, высвобожденного из сложного эфира (связанной формы) путем переэтерификации, катализируемой кислотой, в соответствии с методом стандарта.
Примечание - Содержание связанного глицидола рассчитывается и выражается в миллиграммах на килограмм (мг/кг).
Образец масла/жира растворяют в тетрагидрофуране и в полученный раствор добавляют внутренний стандарт (пентадейтерированный двухзамещенный эфир 3-МХПД и пентадейтерированный глицидиловый эфир). В ходе первого шага подготовки образца сложные эфиры глицидола превращаются в однозамещенные сложные эфиры 3-МБПД путем добавления подкисленного раствора бромида натрия. После завершения реакции органическую фазу, содержащую сложные эфиры 2- и 3-МХПД, а также 3-МБПД, отделяют и выпаривают досуха. На втором шаге полученный осадок растворяют в тетрогидрофуране и запускают процесс кислотной переэтерификации с добавлением кислотно-спиртового раствора. После 16 часов выдержки при температуре 40 °С образец смеси нейтрализуют и удаляют метиловые эфиры жирных кислот, образовавшиеся при переэтерификации. По окончании очищенный образец [содержащий высвобожденные (свободные) определяемые вещества] преобразовывают фенилборной кислотой перед проведением ГХ/МС анализа.
Количественное определение сложных эфиров 2- и 3-МХПД (выраженных как связанные 2- и 3-МХПД) основывается на отношении площадей пиков 2-МХПД/3-МХПД-d5 и 3-МХПД/3-МХПД-d5 соответственно. Количественное определение сложных эфиров глицидола (выраженных как связанный глицидол) основывается на отношении площадей пиков 3-МБПД/3-МБПД-d5.
Настоящий метод позволяет количественно определять все три соединения в одном анализе.
ПРЕДУПРЕЖДЕНИЕ - Следует обратить внимание на правила, регламентирующие обращение с опасными веществами. Следует соблюдать технические, организационные и личные меры безопасности.
При проведении анализа следует использовать реактивы чистые для анализа, если не указано иное. Вода должна соответствовать требованиям класса 3 стандарта ISO 3696.
5.1 Стандартные и эталонные соединения
5.1.1 1,2-дипальмитоил-З-хлорпропандиол (PP-3-MCPD), чистота ≥ 95 % (например, от поставщика или синтезированный из 3-МХПД и пальмитоил хлорида, как это описано в [1]).
Примечание - 1,2-дипальмитоил-З-хлорпропандиол можно заменить на 1,2-диолеил-3-хлорпропандиол или другой двухзамещенный сложный эфир 3-МХПД со сходной длиной цепи (С16-С18 являются предпочтительными из-за их преобладания в маслах/жирах).
5.1.2 1,3-дипальмитоил-2-хлорпропандиол (PP-2-MCPD), чистота ≥ 95 % (например, синтезированный из 2-МХПД и пальмитоил хлорида, как это описано в [1]).
Примечание - Аналогично рекомендациям, приведенным для PP-3-MCPD, 1,3-дипальмитоил-2-хлорпропандиол можно заменить на другой двухзамещенный сложный эфир жирной кислоты 2-МХПД со сходной длиной цепи (С16-С18 являются предпочтительными из-за их преобладания в маслах/жирах).
5.1.3 Пентадейтерированный 1,2-дипальмитоил-З-хлорпропандиол (PP-3-MCPD-d5), чистота ≥ 95 %.
Примечание - Аналогично рекомендациям, приведенным для 1,2-дипальмитоил-З-хлорпропандиола и его пентадейтерированного аналога, см. примечание к п. 5.1.1.
5.1.4 Глицидиловый эфир пальмитиновой кислоты (Gly-P), чистота ≥ 98 %.
Примечание - Глицидиловый эфир пальмитиновой кислоты может быть заменен глицидиловым эфиром олеиновой кислоты или другим сложным эфиром жирной кислоты со сходной длиной цепи (С16-С18 являются предпочтительными из-за их преобладания в маслах/жирах).
5.1.5 Пентадейтерированный глицидиловый эфир пальмитиновой кислоты (Gly-P-d5), чистота ≥ 98 %.
Примечание - Рекомендации, аналогичные приведенным, для глицидилового эфира пальмитиновой кислоты могут быть применены для его пентадейтерированного аналога, см. примечание к 5.1.4.
5.2 Стандартные растворы
5.2.1 Общие положения
Все стандартные растворы могут быть приготовлены с толуолом (5.3.5) или тетрагидрофураном (5.3.1). Толуол предпочтителен в качестве растворителя для растворов сложных эфиров глицидола.
5.2.2 Основной раствор (1 мг/мл)
a) Взвешивают 10 мг PP-3-MCPD (5.1.1) в мерной колбе объемом 10 мл. Заполняют до отметки и убеждаются, что стандарт полностью растворился в растворителе.
b) Взвешивают 10 мг PP-2-MCPD (5.1.2) в мерной колбе объемом 10 мл. Заполняют до отметки и убеждаются, что стандарт полностью растворился в растворителе.
c) Взвешивают 10 мг PP-3-MCPD-d5 (5.1.3) в мерной колбе объемом 10 мл. Заполняют до отметки и убеждаются, что стандарт полностью растворился в растворителе.
d) Взвешивают 10 мг Gly-P (5.1.4) в мерной колбе объемом 10 мл. Заполняют до отметки и убеждаются, что стандарт полностью растворился в растворителе.
e) Взвешивают 10 мг Gly-P-d5 (5.1.5) в мерной колбе объемом 10 мл. Заполняют до отметки и убеждаются, что стандарт полностью растворился в растворителе.
Примечание - Основные растворы стабильны в течение трех месяцев при температуре хранения минус 18 °С.
5.2.3 Рабочие растворы
a) Калибровочный раствор I (PP-3-MCPD, 55 мкг/мл). Пипеткой вносят 550 мкл основного раствора [5.2.2 а)] в мерную колбу объемом 10 мл и доводят до метки растворителем.
b) Калибровочный раствор II (PP-3-MCPD, 5,5 мкг/мл). Пипеткой вносят 1 мл калибровочного раствора I [5.2.3 а)] в мерную колбу объемом 10 мл и доводят до метки растворителем.
c) Калибровочный раствор III (PP-2-MCPD, 55 мкг/мл). Пипеткой вносят 550 мкл основного раствора [5.2.2 b)] в мерную колбу объемом 10 мл и доводят до метки растворителем.
d) Калибровочный раствор IV (PP-2-MCPD, 5,5 мкг/мл). Пипеткой вносят 1 мл калибровочного раствора III [5.2.3 с)] в мерную колбу объемом 10 мл и доводят до метки растворителем.
e) Калибровочный раствор V (Gly-P, 100 мкг/мл). Пипеткой вносят 1 мл основного раствора [5.2.2 d)] в мерную колбу объемом 10 мл и доводят до метки растворителем.
f) Калибровочный раствор VI (Gly-P, 10 мкг/мл). Пипеткой вносят 1 мл калибровочного раствора V [5.2.3 е)] в мерную колбу объемом 10 мл и доводят до метки растворителем.
g) Внутренний стандарт I (PP-3-MCPD-d5, 40 мкг/мл). Пипеткой вносят 400 мкл основного раствора [5.2.2 с)] в мерную колбу объемом 10 мл и доводят до метки растворителем.
h) Внутренний стандарт II (Gly-P-d5, 50 мкг/мл). Пипеткой вносят 500 мкл основного раствора [5.2.2 е)] в мерную колбу объемом 10 мл и доводят до метки растворителем.
Примечание 1 - В качестве альтернативного способа приготовления стандартных растворов каждого определяемого соединения [5.2.3 а), с) и е)] может быть применено объединение этих трех растворов с высокой концентрацией в один стандартный раствор ("Калибровочная смесь I"). Для приготовления смешанного раствора вносят пипеткой 550 мкл основного раствора PP-3-MCPD [5.2.2 а)], 550 мкл основного раствора PP-2-MCPD [5.2.2 b)] и 1 мл основного раствора Gly-P [5.2.2 d)] в мерную колбу объемом 10 мл и доводят до метки растворителем. Кроме того, растворы 5.2.3 b), d) и f) могут быть объединены в один стандартный раствор при низкой концентрации всех трех определяемых веществ ("Калибровочная смесь II"). Для приготовления смешанного раствора вносят 1 мл калибровочной смеси I в мерную колбу объемом 10 мл и заполняют ее растворителем до метки.
Примечание 2 - Растворы внутреннего стандарта [5.2.3 g) и h)] также можно объединить в один раствор ("смешанный внутренний стандарт"). Для приготовления смешанного раствора пипеткой вносят 400 мкл PP-3-MCPD-d5 [5.2.2 с)] и 500 мкл Gly-P-d5 [5.2.2 е)] в мерную колбу объемом 10 мл и заполняют ее растворителем до метки.
5.3 Другие реактивы
5.3.1 Тетрагидрофуран безводный.
5.3.2 Метанол, чистый для анализа.
5.3.3 н-Гептан, чистый для анализа.
5.3.4 Ацетон, чистый для анализа.
5.3.5 Толуол, чистый для анализа.
5.3.6 Вода ультрачистая (например, полученная с помощью системы очистки).
5.3.7 Серная кислота, чистота ≥ 95 %.
5.3.8 Гидрокарбонат натрия, чистота ≥ 99 %.
5.3.9 Сульфат натрия, чистота ≥ 99 %.
5.3.10 Фенилборная кислота, чистота ≥ 97 %.
5.3.11 Бромид натрия, чистота ≥ 99,5 %.
5.4 Растворы реактивов
5.4.1 Кислый водный раствор бромида натрия [бромид натрия 3 мг/мл, серная кислота 5 % (объемная доля)]. Подготавливают концентрированный водный раствор бромида натрия, растворив 1 г бромида натрия (5.3.11) в 10 мл ультрачистой воды (5.3.6). Переносят 180 мкл концентрированного раствора в пустую коническую колбу. Добавляют 0,3 мл серной кислоты (5.3.7) и 5,5 мл ультрачистой воды (5.3.6). Хорошо встряхивают.
Рекомендуется ежедневно готовить свежий раствор.
5.4.2 Раствор гидрокарбоната натрия (массовая концентрация 0,6 %). Взвешивают 0,6 г гидрокарбоната натрия (5.3.8) в мерную колбу объемом 100 мл и заполняют ее до метки ультрачистой водой (5.3.6). Используют ультразвуковую ванну (6.3) для полного растворения реагента.
Примечание - Раствор также можно приготовить путем разбавления насыщенного раствора гидрокарбоната натрия (5.4.4).
5.4.3 Раствор серной кислоты в метаноле (1,8 %, объемная доля). Добавляют пипеткой 1,8 мл серной кислоты (5.3.7) в мерную колбу объемом 100 мл и доводят до метки метиловым спиртом (5.3.2).
Рекомендуется ежедневно готовить свежий раствор.
5.4.4 Раствор гидрокарбоната натрия (насыщенный). Взвешивают навеску 9,6 г гидрокарбоната натрия (5.3.8) в мерную колбу объемом 100 мл и доводят до метки ультрачистой водой (5.3.6). Используют ультразвуковую ванну (6.3) для полного растворения реагента.
Примечание - Для повышения точности метода насыщенный раствор гидрокарбоната натрия можно заменить раствором с точной концентрацией (массовая концентрация 9 %).
5.4.5 Раствор сульфата натрия (массовая концентрация 20 %). Взвешивают навеску 20 г сульфата натрия (5.3.9) в мерную колбу объемом 100 мл и доводят до метки ультрачистой водой (5.3.6). Используют ультразвуковую ванну (6.3) для полного растворения реагента.
5.4.6 Раствор фенилборной кислоты (насыщенный). Взвешивают навеску 3 г фенилборной кислоты (5.3.10), добавляют 12 мл смеси ацетона (5.3.4)/ультрачистой воды (5.3.6) (объемная концентрация 19/1). Хорошо встряхивают.
Примечание - Фенилборная кислота не растворяется полностью в смеси растворителей. На этапе получения производных используют только надосадочную жидкость (8.1.6).
6.1 Вихревая мешалка.
6.2 Сушильная камера, поддерживающая (45 ± 5) °С.
6.3 Ультразвуковая ванна.
6.4 Лабораторный испаритель (с азотом).
6.5 Центрифуга.
6.6 Оборудование ГХ/МС, состоящее из:
a) капиллярного газового хроматографа с квадрупольным масс-селективным детектором и блоком обработки данных, и
b) капиллярной колонки с неподвижной фазой поли(диметилсилоксан) (например, длина 30 м, внутренний диаметр 0,25 мм и толщина пленки 1,0 мкм).
7.1 Отбор проб
Отбор проб не является частью данного метода. Рекомендуемый метод отбора проб приведен в ИСО 5555.
7.2 Подготовка пробы для анализа
Жидкие образцы следует использовать без дополнительной обработки. Твердые или мутные жиры должны быть расплавлены при температуре 80 °С в сушильном шкафу или на водяной бане. Для жиров с высокой температурой плавления температуру постепенно увеличивают с шагом 10 °С до начала процесса плавления.
8.1 Подготовка анализируемого образца
8.1.1 Взвешивают навеску масла/жира массой от 100 до 110 мг (с точностью 0,01 мг) в пробирку с винтовой крышкой. Добавляют 50 мкл рабочего раствора внутреннего стандарта I [5.2.3 g)] и II [5.2.3 h)] и 2 мл тетрагидрофурана (5.3.1). Перемешивают смесь в течение 15 с (или до полного растворения) на вихревой мешалке (6.1).
Наличие воды может мешать преобразованию сложных эфиров глицидола в однозамещенные эфиры МБПД (8.1.2), поэтому рекомендуется использование безводного тетрагидрофурана (5.3.1) [2].
Если используется смешанный раствор внутреннего стандарта (см. примечание к 5.2.3), то к образцу необходимо добавить 50 мкл этого раствора.
Если предполагают высокое содержание хлоридных солей в образце, необходимо проведение дополнительного этапа жидкость/жидкостной экстракции водой, описанной в [3]. Особое внимание необходимо уделить процессу полного отделения водного слоя после экстракции.
8.1.2 Добавляют к образцу 30 мкл кислого водного раствора бромида натрия (5.4.1), тщательно перемешивают на вихревой мешалке (6.1) и выдерживают смесь при 50 °С в течение 15 мин. Останавливают реакцию добавлением 3 мл водного раствора 0,6 % гидрокарбоната натрия (5.4.2). Для отделения масла/жира от водной фазы добавляют 2 мл н-гептана (5.3.3) и тщательно перемешивают на вихревой мешалке (6.1) в течение 15 с. После разделения двух фаз переносят верхний слой в пустую стеклянную пробирку и испаряют досуха в потоке азота (максимум от 15 до 20 мин при температуре от 35 °С до 40 °С). Растворяют твердый остаток в 1 мл тетрагидрофурана (5.3.1).
Время и температуру реакции следует тщательно контролировать, чтобы избежать неполного преобразования сложных эфиров глицидола или образования новых сложных эфиров 3-МБПД [2].
Четкое разделение органической фазы и водной фазы может быть затруднено. Поэтому часто требуется выполнение центрифугирования образца (примерно от 1 до 2 мин при 250 g).
Процесс испарения органической фазы в потоке азота следует тщательно контролировать и останавливать сразу после испарения растворителя. Небольшое количество растворителя (< 50 мкл), оставшегося в образце, не влияет на качество результатов, и это предпочтительнее, чем длительное воздействие потока азота на образец.
Добавляют к образцу 1,8 мл смеси серной кислоты/метанола (5.4.3) и перемешивают на вихревой мешалке (6.1) в течение 10 с. Плотно закрывают стеклянную пробирку крышкой и выдерживают смесь при 40 °С в течение 16 ч.
8.1.3 После выдерживания останавливают реакцию добавлением к образцу 0,5 мл насыщенного раствора гидрокарбоната натрия (5.4.4). Перемешивают смесь на вихревой мешалке (6.1) в течение 10 с. Выпаривают органический растворитель из смеси в потоке азота.
Примечание - Удаление органических растворителей из пробы повышает точность метода. Испарение можно остановить по визуальным признакам, когда объем в пробирке составит около 1 мл.
8.1.4 Добавляют 2 мл раствора сульфата натрия (5.4.5) и 2 мл н-гептана (5.3.3). Перемешивают смесь на вихревой мешалке (6.1) в течение 10 с. Две фазы самостоятельно разделяются в течение нескольких секунд. Удаляют верхнюю фазу (она содержит метиловые эфиры жирных кислот, растворенные в н-гептане) и повторяют экстракцию с н-гептаном.
В ходе второй экстракции важно полностью удалить органическую фазу.
8.1.5 Добавляют 250 мкл раствора фенилборной кислоты (5.4.6), перемешивают в течение 10 с на вихревой мешалке (6.1) и выдерживают смесь в течение 5 мин в ультразвуковой ванне (6.3) при комнатной температуре.
8.1.6 Экстрагируют фенилборные производные 2- и 3-МХПД, а также 3-МБПД, добавив 1 мл н-гептана (5.3.3), перемешивают смесь в течение 10 с на вихревой мешалке (6.1), переносят верхнюю фазу в пустую пробирку. Повторяют экстракцию 1 мл н-гептана и объединяют два экстракта. Выпаривают экстракт досуха в потоке азота. Растворяют остаток в 400 мкп н-гептана, перемешав на вихревой мешалке в течение 10 с (6.1), переносят полученную смесь в пустую виалу для хроматографии (обычно используется стеклянная вставка объемом 250 мкп).
Для облегчения удаления н-гептана испарение экстракта в потоке азота проводится в температурном диапазоне от 35 °С до 40 °С, но процесс следует остановить сразу после испарения растворителя, чтобы избежать потерь, связанных с высокой летучестью фенилборных производных.
Если испарение экстракта выполняется при повышенной температуре (максимум 40 °С), то перед растворением полученных осадков пробирки необходимо охладить до комнатной температуры.
Примечание - В процессе упаривания экстракта избыток фенилборной кислоты, не прореагировавшей с 2- и 3-МХПД, а также 3-МБПД кристаллизуется на стенках пробирки в форме белого осадка. Добавление 400 мкп н-гептана (заключительный этап подготовки образца) не приводит к полному растворению, так как это мешало бы анализу.
8.2 Построение калибровочной кривой
8.2.1 Приготавливают девять калибровочных образцов путем ввода 50 мкл как рабочих растворов внутренних стандартов [5.2.3 g) и h)], так и калибровочных растворов [5.2.3 а) до f)], указанных в таблице А.1. Добавляют 2 мл тетрагидрофурана (5.3.1) и перемешивают смесь на вихревой мешалке (6.1) в течение 10 с.
Примечание - Добавление от 100 до 110 мг чистого масла (не содержащего сложных эфиров 2-МХПД/3-МХПД и глицидола) в калибровочные образцы может повысить точность метода, поскольку основа масла действует как среда, удерживающая определяемые вещества на этапе упаривания.
8.2.2 Подготавливают калибровочные образцы согласно процедуре подготовки для анализируемых образцов (8.1).
8.3 Условия проведения анализа методом газовой хроматографии/масс-спектрометрии
8.3.1 Объем вводимой пробы: 1,0 мкл.
8.3.2 Режим ввода пробы: импульсный без разделения потока.
8.3.3 Температура инжектора: 250 °С.
8.3.4 Газ-носитель: гелий, расход: 0,8 мл/мин.
8.3.5 Программирование температуры термостата колонки ГХ: 80 °С (изотермический режим в течение 1 мин), от 80 °С до 170 °С со скоростью 10 °С/мин, от 170 °С до 200 °С со скоростью 3 °С/мин, от 200 °С до 300 °С со скоростью 15 °С/мин, 300 °С (изотермический режим в течение 15 мин).
8.3.6 Масс-спектрометрический детектор: электронная ионизация (ЕЭ), температура переходной линии: 300 °С, температура ионного источника: 230 °С, температура квадруполя: 150 °С, SIM-режим (режим селективно выбранных масс ионов) - время экспозиции: от 5 до 20 мин.
Примечание - Молекулярные ионы (m/z 196 и 201 для 3-МХПД и 3-МХПД-d5 соответственно; m/z 240 и 245 для 3-МБПД и 3-МБПД-d5 соответственно) также могут использоваться для количественного определения, при этом необходимо учитывать, что низкая интенсивность их сигнала может повлиять на точность определения.
8.3.7 Параметры SIM-режима: а) фенилборная производная 3-МХПД (m/z) 147 (характеристический ион), 196, 198 (подтверждающие ионы); b) фенилборная производная 2-МХПД (m/z) 196 (характеристический ион), 198 (подтверждающий ион); с) фенилборная производная 3-МХПД-d5 (m/z) 150 (характеристический ион для 3-МХПД), 201 (характеристический ион для 2-МХПД), 203 (подтверждающий ион); d) фенилборная производная 3-МБПД (m/z) 147 (характеристический ион), 240 подтверждающий ион); е) фенилборная производная 3-МБПД-d5 (m/z) 150 (характеристический ион), 245 (подтверждающий ион).
9.1 Количественное определение сложных эфиров 3-МХПД
9.1.1 Подготавливают калибровочную кривую, откладывая отношение количества стандарта (выраженного как эквивалент свободного 3-МХПД) к количеству внутреннего стандарта (выраженного как эквивалент свободного 3-МХПД-d5) по оси X и отношение площадей соответствующих пиков по оси Y (рисунок А.1). Ионы с m/z 147 (3-МХПД) и 150 (3-МХПД-d5) используют для количественного определения. Линейную регрессию рассчитывают по формуле
y=ax+b,
(1)
где a - тангенс угла наклона;
b - точка пересечения с осью Y.
Для обеспечения высокой точности определения в образцах с низкой концентрацией сложных эфиров 3-МХПД необходимо, чтобы подтверждалась хорошая линейность (R2 > 0,99), и желательно, чтобы точка пересечения с осью Y была < |0,02|.
9.1.2 Концентрацию эфиров 3-МХПД в анализируемом образце (мг/кг) рассчитывают по формуле
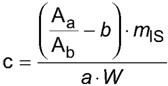 ,
,
(2)
где с - концентрация сложных эфиров 3-МХПД в анализируемом образце (выраженная как связанный 3-МХПД, мг/кг масла);
Аа - площадь пика, соответствующая производной 3-МХПД (m/z 147);
Ab - площадь пика, соответствующая производной 3-МХПД-d5 (m/z 150);
b - точка пересечения калибровочной кривой с осью Y;
mIS - абсолютное значение количества внутреннего стандарта (в мкг, скорректированное с учетом его чистоты), добавленного в анализируемый образец;
а - тангенс угла наклона калибровочной кривой;
W - масса образца в граммах.
9.2 Количественное определение сложных эфиров 2-МХПД
9.2.1 Подготавливают калибровочную кривую, откладывая отношение количества стандарта (выраженного как эквивалент свободного 2-МХПД) к количеству внутреннего стандарта (выраженного как эквивалент свободного 3-МХПД-d5) по оси X и отношение площадей соответствующих пиков по оси Y. Ионы с m/z 196 (2-МХПД) и 201 (3-МХПД-d5) используются для количественного определения. Линейную регрессию рассчитывают по формуле
y=ax+b,
(3)
где а - тангенс угла наклона;
b - точка пересечения с осью Y.
Для обеспечения высокой точности определения в образцах с низкой концентрацией сложных эфиров 2-МХПД необходимо подтвердить линейность (R2 > 0,99) и что точка пересечения с осью Y < |0,05|.
9.2.2 Концентрацию сложных эфиров 2-МХПД в анализируемом образце (мг/кг) рассчитывают по формуле
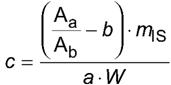 ,
,
(4)
где с - концентрация сложных эфиров 2-МХПД в анализируемом образце (выраженная как связанный 2-МХПД, мг/кг масла);
Аа - площадь пика, соответствующая производной 2-МХПД (m/z 196);
Ab - площадь пика, соответствующая производной 3-МХПД-d5 (m/z 201);
b - точка пересечения калибровочной кривой с осью Y;
mIS - абсолютное значение количества внутреннего стандарта (в мкг, скорректированное с учетом его чистоты), добавленного в анализируемый образец;
а - тангенс угла наклона калибровочной кривой;
W - масса образца в граммах.
9.3 Количественное определение сложных эфиров глицидола
9.3.1 Подготавливают калибровочную кривую, откладывая отношение количества стандарта (выраженного как эквивалент глицидола) к количеству внутреннего стандарта (выраженного как эквивалент дейтерированного глицидола) по оси X и отношение площади соответствующих пиков по оси Y (рисунок А.2). Ионы с m/z 147 (3-МХПД) и 150 (3-МХПД-d5) используют для количественного определения. Линейную регрессию рассчитывают по формуле
y=ax+b,
(5)
где а - тангенс угла наклона;
b - точка пересечения с осью Y.
Для обеспечения высокой точности определения в образцах с низкой концентрацией сложных эфиров глицидола необходимо, чтобы подтверждалась хорошая линейность (R2 > 0,99), и желательно, чтобы точка пересечения с осью Y была < |0,02|.
9.3.2 Концентрацию сложных эфиров глицидола в анализируемом образце (мг/кг) рассчитывают по формуле
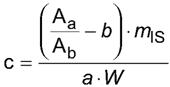 ,
,
(6)
где с - концентрация сложных эфиров глицидола в анализируемом образце (выраженная как связанный глицидол, мг/кг масла);
Аа - площадь пика, соответствующая производной 3-МХПД (m/z 147);
Ab - площадь пика, соответствующая производной 3-МХПД-d5 (m/z 150);
b - точка пересечения калибровочной кривой с осью Y;
mIS - абсолютное значение количества внутреннего стандарта (в мкг, скорректированное с учетом его чистоты), добавленного в анализируемый образец;
а - тангенс угла наклона калибровочной кривой;
W - масса образца в граммах.
Примечание - Типичные хроматограммы реального образца приведены на рисунках А.3 и А.4.
10.1 Общие положения
Оценка метода была осуществлена при совместном исследовании, проведенном AOCS. Благодаря удовлетворительным результатам, предоставленным участвующими лабораториями, метод был признан в качестве официального метода AOCS Cd29a-13. Подробная информация о межлабораторном испытании точности метода приведена в приложении В. Результаты, полученные в ходе межлабораторного испытания, не могут применяться к диапазонам концентраций и основным веществам, отличным от приведенных в приложении В.
10.2 Повторяемость
Разница между результатами двух однократных независимых испытаний, полученными одним и тем же методом, на идентичном анализируемом материале, в одной и той же лаборатории, одним и тем же оператором и с использованием одного и того же оборудования, в течение одного дня не должна превышать 3 % Sr [2].
10.3 Воспроизводимость
Разница между результатами двух однократных независимых испытаний, полученными одним и тем же методом, на идентичном анализируемом материале, в одной и той же лаборатории, одним и тем же оператором и с использованием одного и того же оборудования, в течение короткого периода времени (например, пять дней) не должна превышать 5 % SR [2].
Протокол испытания должен содержать, как минимум, следующее:
a) всю информацию, необходимую для полной идентификации образца;
b) использованный метод испытания и элемент, подлежащий определению, со ссылкой на настоящий стандарт;
c) результаты испытаний, полученные согласно разделу 9, и единицы измерения, в которых они выражены;
d) дату отбора пробы и процедуру отбора пробы (если она известна);
e) дату завершения анализа;
f) все технические данные, не указанные в настоящем стандарте или рассматриваемые в качестве необязательных, а также сведения о любых инцидентах, произошедших при выполнении метода, которые могли повлиять на результат(ы) испытания.
Приложение А
(справочное)
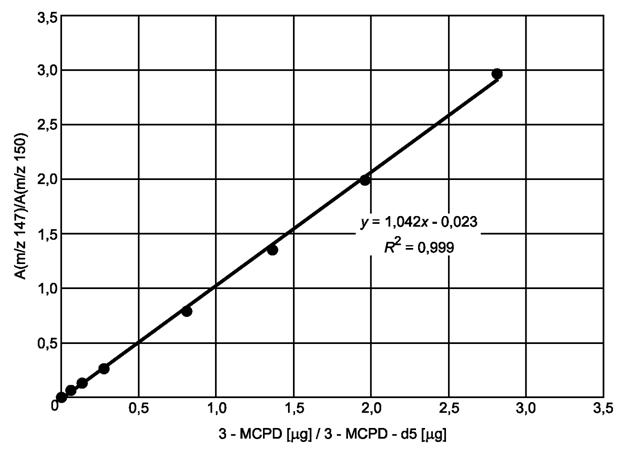
Рисунок А.1 - Калибровочная кривая PP-3-MCPD
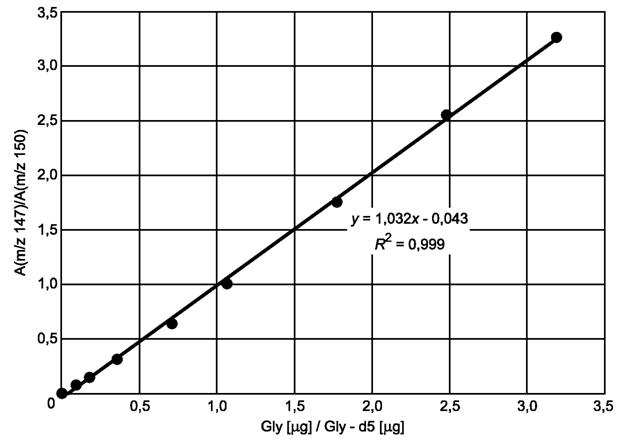
Рисунок А.2 - Калибровочная кривая Gly-P
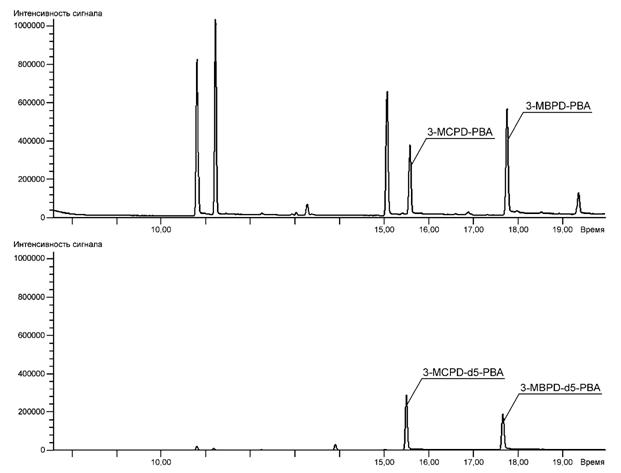
Рисунок А.3 - SIM-хроматограмма образца полностью рафинированного пальмового масла (выделенные ионы m/z 147 и 150)
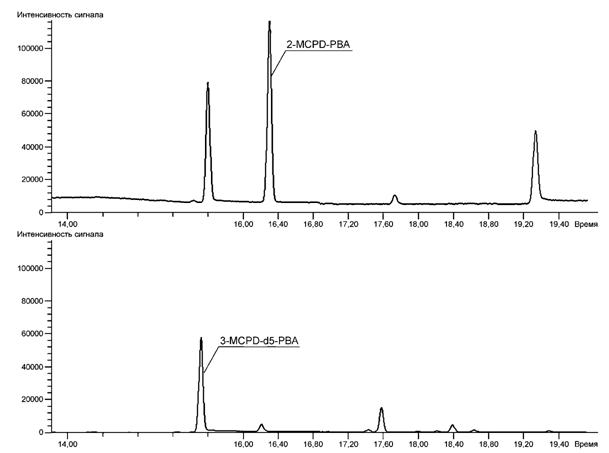
Рисунок А.4 - SIM-хроматограмма образца полностью рафинированного пальмового масла (выделенные ионы m/z 196 и 201)
|
Калибровочный раствор |
2-МХПД a, |
3-МХПД a, |
Gly a, |
Раствор внутреннего стандарта |
3-МХПД a-d5 a, |
Gly-d5 a, | |
|
[5.2.3 a)-f)] |
мкг |
мкг |
мкг |
[5.2.3 g), h)] |
мкг |
мкг | |
|
Калибровочная кривая 0 |
- |
0,00 |
0,00 |
0,00 |
50 мкл (g) + 50 мкл (h) или 50 мкл смешанного внутреннего стандарта |
0,39 |
0,62 |
|
Калибровочная кривая 1 |
25 мкл (b) + 25 мкл (d) + 25 мкл (f) или 25 мкл калибровочной смеси II |
0,03 |
0,03 |
0,06 |
50 мкл (g) + 50 мкл (h) или 50 мкл смешанного внутреннего стандарта |
0,39 |
0,62 |
|
Калибровочная кривая 2 |
50 мкл (b) + 50 мкл (d) + 50 мкл (f) или 50 мкл калибровочной смеси II |
0,05 |
0,05 |
0,12 |
50 мкл (g) + 50 мкл (h) или 50 мкл смешанного внутреннего стандарта |
0,39 |
0,62 |
|
Калибровочная кривая 3 |
100 мкл (b) + 100 мкл (d) + 100 мкл (f) или 100 мкл калибровочной смеси II |
0,10 |
0,10 |
0,24 |
50 мкл (g) + 50 мкл (h) или 50 мкл смешанного внутреннего стандарта |
0,39 |
0,62 |
|
Калибровочная кривая 4 |
20 мкл (а) + 20 мкл (с) + 20 мкл (е) или 20 мкл калибровочной смеси I |
0,21 |
0,21 |
0,47 |
50 мкл (g) + 50 мкл (h) или 50 мкл смешанного внутреннего стандарта |
0,39 |
0,62 |
|
Калибровочная кривая 5 |
30 мкл (а) + 30 мкл (с) + 30 мкл (е) или 30 мкл калибровочной смеси I |
0,31 |
0,31 |
0,71 |
50 мкл (g) + 50 мкл (h) или 50 мкл смешанного внутреннего стандарта |
0,39 |
0,62 |
|
Калибровочная кривая 6 |
50 мкл (а) + 50 мкл (с) + 50 мкл (е) или 50 мкл калибровочной смеси I |
0,52 |
0,52 |
1,19 |
50 мкл (g) + 50 мкл (h) или 50 мкл смешанного внутреннего стандарта |
0,39 |
0,62 |
|
Калибровочная кривая 7 |
70 мкл (а) + 70 мкл (с) + 70 мкл (е) или 70 мкл калибровочной смеси I |
0,72 |
0,72 |
1,66 |
50 мкл (g) + 50 мкл (h) или 50 мкл смешанного внутреннего стандарта |
0,39 |
0,62 |
|
Калибровочная кривая 8 |
90 мкл (а) + 90 мкл (с) + 90 мкл (е) или 90 мкл калибровочной смеси I |
0,93 |
0,93 |
2,13 |
50 мкл (g) + 50 мкл (h) или 50 мкл смешанного внутреннего стандарта |
0,39 |
0,62 |
|
а Данные значения должны быть скорректированы по чистоте использованного стандарта. | |||||||
Приложение В
(справочное)
Точность метода была установлена международным межлабораторным исследованием, организованным Американским обществом специалистов в области химии жиров в 2014 году. Статистическая оценка метода была выполнена в соответствии с ИСО 5725-1 и ИСО 5725-2.
Определение образца:
- образец 1: полностью рафинированное рапсовое масло с добавлением эфиров 3-МХПД и глицидиловых эфиров;
- образец 2: полностью рафинированное рапсовое масло с добавлением глицидиловых эфиров;
- образец 3: полностью рафинированное рапсовое масло с добавлением эфиров 3-МХПД;
- образец 4: полностью рафинированное рапсовое масло с добавлением эфиров 3-МХПД и глицидиловых эфиров;
- образец 5: полностью рафинированное рапсовое масло;
- образец 6: полностью рафинированное пальмовое масло;
- образец 7: полностью рафинированное пальмовое масло с добавлением эфиров 3-МХПД и глицидиловых эфиров.
В таблицах В.1-В.3 представлены статистические результаты.
|
Образец 1 |
Образец 2 |
Образец 3 |
Образец 4 |
Образец 5 |
Образец 6 |
Образец 7 | |
|
Количество лабораторий |
10 |
10 |
12 |
11 |
9 |
11 |
12 |
|
Повторы |
20 |
20 |
24 |
22 |
18 |
22 |
24 |
|
Среднее |
47,28 |
0,49 |
5,82 |
18,92 |
0,50 |
1,95 |
3,41 |
|
Повторяемость | |||||||
|
CV,r |
0,46 |
0,03 |
0,35 |
0,35 |
0,05 |
0,09 |
0,08 |
|
sr, % |
0,97 |
5,45 |
5,99 |
1,85 |
9,76 |
4,65 |
2,43 |
|
r |
1,28 |
0,08 |
0,98 |
0,98 |
0,14 |
0,25 |
0,23 |
|
Воспроизводимость | |||||||
|
CV,R |
3,97 |
0,08 |
0,79 |
1,87 |
0,05 |
0,13 |
0,41 |
|
SR, % |
8,40 |
16,12 |
13,54 |
9,88 |
9,76 |
6,42 |
11,96 |
|
R |
11,12 |
0,22 |
2,20 |
5,23 |
0,14 |
0,35 |
1,14 |
|
Образец 1 |
Образец 2 |
Образец 3 |
Образец 4 |
Образец 5 |
Образец 6 |
Образец 7 | |
|
Количество лабораторий |
10 |
11 |
11 |
11 |
10 |
11 |
12 |
|
Повторы |
20 |
22 |
22 |
22 |
20 |
22 |
24 |
|
Среднее |
0,32 |
0,21 |
0,22 |
0,26 |
0,22 |
0,93 |
1,61 |
|
Повторяемость | |||||||
|
CV,r |
0,03 |
0,03 |
0,04 |
0,03 |
0,03 |
0,06 |
0,09 |
|
sr, % |
9,62 |
14,24 |
16,20 |
13,49 |
12,57 |
6,31 |
5,58 |
|
r |
0,09 |
0,08 |
0,10 |
0,10 |
0,08 |
0,16 |
0,25 |
|
Воспроизводимость | |||||||
|
CV,R |
0,09 |
0,05 |
0,06 |
0,07 |
0,03 |
0,13 |
0,22 |
|
SR, % |
27,79 |
25,28 |
26,56 |
25,62 |
15,20 |
13,56 |
13,76 |
|
R |
0,25 |
0,15 |
0,16 |
0,19 |
0,09 |
0,35 |
0,62 |
|
Образец 1 |
Образец 2 |
Образец 3 |
Образец 4 |
Образец 5 |
Образец 6 |
Образец 7 | |
|
Количество лабораторий |
11 |
10 |
8 |
12 |
8 |
12 |
12 |
|
Повторы |
22 |
20 |
16 |
24 |
15 |
24 |
24 |
|
Среднее |
8,76 |
1,46 |
0,28 |
4,69 |
0,32 |
10,91 |
4,92 |
|
Повторяемость | |||||||
|
CV,r |
0,31 |
0,03 |
0,03 |
0,16 |
0,04 |
0,42 |
0,13 |
|
sr, % |
3,51 |
2,19 |
12,28 |
3,46 |
12,13 |
3,87 |
2,70 |
|
r |
0,86 |
0,09 |
0,10 |
0,45 |
0,11 |
1,18 |
0,37 |
|
Воспроизводимость | |||||||
|
CV,R |
0,82 |
0,05 |
0,12 |
0,41 |
0,13 |
1,37 |
0,49 |
|
SR, % |
9,33 |
3,15 |
44,38 |
8,84 |
40,12 |
12,56 |
9,93 |
|
R |
2,29 |
0,13 |
0,35 |
1,16 |
0,36 |
3,84 |
1,37 |
Приложение ДА
(справочное)
Таблица ДА.1
|
Обозначение ссылочного международного стандарта |
Степень соответствия |
Обозначение и наименование соответствующего национального стандарта |
|
ISO 3696 |
MOD |
ГОСТ Р 52501-2005 (ИСО 3696:1987) "Вода для лабораторного анализа. Технические условия" * |
|
Примечание - В настоящей таблице использовано следующее условное обозначение степени соответствия стандарта: - MOD - модифицированный стандарт. | ||
──────────────────────────────
* Качество воды для лабораторного анализа со степенью чистоты 3 по стандарту ИСО соответствует качеству дистиллированной воды по ГОСТ 6709-72 "Вода дистиллированная. Технические условия".
──────────────────────────────
Библиография
|
[1] |
Kraft R., Brachwitz H., Etzold G., Langen P., Zöpel H.-J. Massenspektrometrische Strukturuntersuchung Stellungsisomerer Fettsäureester der Halogenpropandiole (Desoxyhalogen-glyceride). J. Prakt. Chem. 1979, 321, pp. 756-768 |
|
[2] |
Ermacora A., & Hrnčiřík K. A Novel Method for Simultaneous Monitoring of 2-MCPD, 3-MCPD and Glycidyl Esters in Oils and Fats J. Am. Oil Chem. Soc. 2013, 90, pp. 1-8 |
|
[3] |
Ermacora A., & Hrnčiřík K. Evaluation of an Improved Indirect Method for the Analysis of 3-MCPD Esters Based on Acid Transesterification J. Am. Oil Chem. Sos. 2012, 89, pp. 211-217 |
|
[4] |
ISO 5555, Animal and vegetable fats and oils - Sampling (Жиры и масла животные и растительные. Отбор проб) |
|
[5] |
ISO 5725-1, Accuracy (trueness and precision) of measurement methods and results - Part 1: General principles and definitions [Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Общие принципы и определения] |
|
[6] |
ISO 5725-2, Accuracy (trueness and precision) of measurement methods and results - Part 2: Basic method for the determination of repeatability and reproducibility of a standard measurement method [Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерения] |
|
[7] |
ISO 18363-1, Animal and vegetable fats and oils - Determination of fatty-acid-bound chloropropanediols (MCPDs) and glycidol by GC/MS - Part 1: Method using fast alkaline transesterification and measurement for 3-MCPD and differential measurement for glycidol [Жиры и масла животные и растительные. Определение содержания сложных эфиров жирных кислот монохлорпропандиола (МХПД) и глицидола с применением газовой хроматографии/масс-спектрометрии. Часть 1. Метод с применением быстрой щелочной переэтерификации и измерение содержания 3-МХПД и дифференциальное измерение содержания глицидола] |
(Нет голосов) |
-
29.05.2025
Слухи о скорой заморозке вкладов в России объяснили
 Банкир Хотимский объяснил слухи о заморозке вкладов в России идеей застройщиков
Банкир Хотимский объяснил слухи о заморозке вкладов в России идеей застройщиков
-
29.05.2025
Дачникам рассказали о штрафах за нескошенную траву
 Эксперт по ЖКХ Бондарь: За нескошенную траву дачникам грозит штраф до 50 тысяч
Эксперт по ЖКХ Бондарь: За нескошенную траву дачникам грозит штраф до 50 тысяч
-
29.05.2025
Вероятность исчезновения в России наличных денег оценили
 Экс-глава ЦБ Дубинин: В России никогда не откажутся от наличных рублей
Экс-глава ЦБ Дубинин: В России никогда не откажутся от наличных рублей
-
29.05.2025
Перспективы исламского банкинга в России оценили
 Комитет ГД поддержал продление на три года эксперимента по исламскому банкингу
Комитет ГД поддержал продление на три года эксперимента по исламскому банкингу
-
30.04.2025
Россиянам объяснили опасность зарплаты в конвертах
 Депутат Бессараб: Россияне с зарплатой в конвертах могут остаться без пенсии
Депутат Бессараб: Россияне с зарплатой в конвертах могут остаться без пенсии