┬тхфхэ т фхщёҐтшх яЁшърчюь ╘хфхЁры№эюую рухэҐёҐтр яю Ґхєэшіхёъюьґ ЁхуґышЁютрэш■ ш ьхҐЁюыюушш юҐ 12 фхърсЁ 2017 у. N 1903-ёҐ
╠хцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ ├╬╤╥ 34230-2017
"╧╨╬─╙╩╓╚▀ ╤╬╩╬┬└▀. ╬╧╨┼─┼╦┼═╚┼ ╤┬╬┴╬─═█╒ └╠╚═╬╩╚╤╦╬╥ ╠┼╥╬─╬╠ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚"
Juice products. Determination of free amino acids by high performance liquid chromatography method
╠╩╤ 67.080.01
═69
─рҐр ттхфхэш - 1 этрЁ 2019 у.
┬тхфхэ тяхЁт√х
╧Ёхфшёыютшх
╓хыш, юёэютэ√х яЁшэІшя√ ш юёэютэющ яюЁ фюъ яЁютхфхэш ЁрсюҐ яю ьхцуюёґф𨸥тхээющ ёҐрэфрЁҐшчрІшш ґёҐрэютыхэ√ т ├╬╤╥ 1.0-2015 "╠хцуюёґф𨸥тхээр ёшёҐхь𠸥рэфрЁҐшчрІшш. ╬ёэютэ√х яюыюцхэш " ш ├╬╤╥ 1.2-2015 "╠хцуюёґф𨸥тхээр ёшёҐхь𠸥рэфрЁҐшчрІшш. ╤ҐрэфрЁҐ√ ьхцуюёґф𨸥тхээ√х, яЁртшыр ш ЁхъюьхэфрІшш яю ьхцуюёґф𨸥тхээющ ёҐрэфрЁҐшчрІшш. ╧Ёртшыр ЁрчЁрсюҐъш, яЁшэ Ґш , юсэютыхэш ш юҐьхэ√"
╤тхфхэш ю ёҐрэфрЁҐх
1 ╨рчЁрсюҐрэ ═хъюььхЁіхёъющ юЁурэшчрІшхщ "╨юёёшщёъшщ ёю■ч яЁюшчтюфшҐхыхщ ёюъют" (╨╤╧╤) яЁш ґірёҐшш └ъІшюэхЁэюую юсїхёҐтр "╠ґыҐюэ" (└╬ "╠ґыҐюэ") ш ╘хфхЁры№эюую уюёґф𨸥тхээюую с■фцхҐэюую ґіЁхцфхэш эрґъш "╘хфхЁры№э√щ шёёыхфютрҐхы№ёъшщ ІхэҐЁ яшҐрэш , сшюҐхєэюыюушш ш схчюярёэюёҐш яшїш" (╘├┴╙═ "╘╚╓ яшҐрэш ш сшюҐхєэюыюушш")
2 ┬эхёхэ ╘хфхЁры№э√ь рухэҐёҐтюь яю Ґхєэшіхёъюьґ ЁхуґышЁютрэш■ ш ьхҐЁюыюушш
3 ╧Ёшэ Ґ ╠хцуюёґф𨸥тхээ√ь ёютхҐюь яю ёҐрэфрЁҐшчрІшш, ьхҐЁюыюушш ш ёхЁҐшЄшърІшш (яЁюҐюъюы юҐ 30 эю сЁ 2017 у. N 52-2017)
╟р яЁшэ Ґшх яЁюуюыюёютрыш:
|
╩ЁрҐъюх эршьхэютрэшх ёҐЁрэ√ яю ╠╩ (╚╤╬ 3166) 004-97
|
╩юф ёҐЁрэ√ яю ╠╩ (╚╤╬ 3166) 004-97
|
╤юъЁрїхээюх эршьхэютрэшх эрІшюэры№эюую юЁурэр яю ёҐрэфрЁҐшчрІшш
|
|
┴хырЁґё№
|
BY
|
├юёёҐрэфрЁҐ ╨хёяґсышъш ┴хырЁґё№
|
|
╩шЁушчш
|
KG
|
╩√Ёу√чёҐрэфрЁҐ
|
|
╨юёёш
|
RU
|
╨юёёҐрэфрЁҐ
|
|
╥рфцшъшёҐрэ
|
TJ
|
╥рфцшъёҐрэфрЁҐ
|
|
╙чсхъшёҐрэ
|
UZ
|
╙чёҐрэфрЁҐ
|
|
╙ъЁршэр
|
UA
|
╠шэ¤ъюэюьЁрчтшҐш ╙ъЁршэ√
|
4 ╧Ёшърчюь ╘хфхЁры№эюую рухэҐёҐтр яю Ґхєэшіхёъюьґ ЁхуґышЁютрэш■ ш ьхҐЁюыюушш юҐ 12 фхърсЁ 2017 у. N 1903-ёҐ ьхцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ ├╬╤╥ 34230-2017 ттхфхэ т фхщёҐтшх т ъріхёҐтх эрІшюэры№эюую ёҐрэфрЁҐр ╨юёёшщёъющ ╘хфхЁрІшш ё 1 этрЁ 2019 у.
5 ┬тхфхэ тяхЁт√х
1 ╬сы𸥹 яЁшьхэхэш
═рёҐю їшщ ёҐрэфрЁҐ ЁрёяЁюёҐЁрэ хҐё эр ёюъютґ■ яЁюфґъІш■ шч ЄЁґъҐют ш ютюїхщ ш ґёҐрэртыштрхҐ ьхҐюф т√ёюъю¤ЄЄхъҐштэющ цшфъюёҐэющ юсЁрїхээю-Єрчютющ єЁюьрҐюуЁрЄшш фы юяЁхфхыхэш ьрёёютющ ъюэІхэҐЁрІшш (ьрёёютющ фюыш) ётюсюфэ√є рьшэюъшёыюҐ:
- L-└ёярЁрушэютющ ъшёыюҐ√;
- L-├ыґҐрьшэр;
- L-├ыґҐрьшэютющ ъшёыюҐ√;
- L-╤хЁшэр;
- L-├шёҐшфшэр;
- L-╥Ёхюэшэр;
- L-└ёярЁрушэр;
- L-└ырэшэр;
- L-└Ёушэшэр;
- L-╥шЁючшэр;
- γ-└ьшэюьрёы эющ ъшёыюҐ√;
- L-╠хҐшюэшэр;
- L-┬рышэр;
- L-╚чюыхщІшэр;
- L-схҐр-╘хэшырырэшэр;
- L-╦хщІшэр;
- L-╦шчшэр;
- ├ышІшэр;
- L-╧Ёюышэр;
- L(+)-╬ЁэшҐшэр.
─шрярчюэ шчьхЁхэшщ ьрёёютющ ъюэІхэҐЁрІшш (ьрёёютющ фюыш) ётюсюфэ√є рьшэюъшёыюҐ ёюёҐрты хҐ юҐ 5, 0 фю 20, 0 ьу/фь3 (ьыэ-1) схч ґіхҐр Ёрчсртыхэш ш ъюэІхэҐЁшЁютрэш яЁюс.
╧Ёшьхірэшх - 1 ьыэ-1 ёююҐтхҐёҐтґхҐ 1 ьу/ъу.
2 ═юЁьрҐштэ√х ёё√ыъш
┬ эрёҐю їхь ёҐрэфрЁҐх шёяюы№чютрэ√ эюЁьрҐштэ√х ёё√ыъш эр ёыхфґ■їшх ьхцуюёґф𨸥тхээ√х ёҐрэфрЁҐ√:
├╬╤╥ 12.1.004-91 ╤шёҐхь𠸥рэфрЁҐют схчюярёэюёҐш ҐЁґфр. ╧юцрЁэр схчюярёэюёҐ№. ╬сїшх ҐЁхсютрэш
├╬╤╥ 12.1.007-76 ╤шёҐхь𠸥рэфрЁҐют схчюярёэюёҐш ҐЁґфр. ┬Ёхфэ√х тхїхёҐтр. ╩ырёёшЄшърІш ш юсїшх ҐЁхсютрэш схчюярёэюёҐш
├╬╤╥ 12.1.019-79* ╤шёҐхь𠸥рэфрЁҐют схчюярёэюёҐш ҐЁґфр. ▌ыхъҐЁюсхчюярёэюёҐ№. ╬сїшх ҐЁхсютрэш ш эюьхэъы𥴨р тшфют чрїшҐ√
├╬╤╥ 61-75 ╨хръҐшт√. ╩шёыюҐр ґъёґёэр . ╥хєэшіхёъшх ґёыютш
├╬╤╥ OIML R 76-1-2011 ├юёґф𨸥тхээр ёшёҐхьр юсхёяхіхэш хфшэёҐтр шчьхЁхэшщ. ┬хё√ эхртҐюьрҐшіхёъюую фхщёҐтш . ╫𸥹 1. ╠хҐЁюыюушіхёъшх ш Ґхєэшіхёъшх ҐЁхсютрэш . ╚ёя√Ґрэш
├╬╤╥ 199-78 ╨хръҐшт√. ═рҐЁшщ ґъёґёэюъшёы√щ 3-тюфэ√щ. ╥хєэшіхёъшх ґёыютш
├╬╤╥ 1770-74 (╚╤╬ 1042-83, ╚╤╬ 4788-80) ╧юёґфр ьхЁэр ырсюЁрҐюЁэ𠸥хъы ээр . ╓шышэфЁ√, ьхэчґЁъш, ъюыс√, яЁюсшЁъш. ╬сїшх Ґхєэшіхёъшх ґёыютш
├╬╤╥ ISO 3696-2013** ┬юфр фы ырсюЁрҐюЁэюую рэрышчр. ╥хєэшіхёъшх ҐЁхсютрэш ш ьхҐюф√ ъюэҐЁюы
├╬╤╥ 4199-76 ╨хръҐшт√. ═рҐЁшщ ҐхҐЁрсюЁэюъшёы√щ 10-тюфэ√щ. ╥хєэшіхёъшх ґёыютш
├╬╤╥ 4328-77 ╨хръҐшт√. ═рҐЁш ушфЁююъшё№. ╥хєэшіхёъшх ґёыютш
├╬╤╥ ╚╤╬ 5725-6-2003*** ╥юіэюёҐ№ (яЁртшы№эюёҐ№ ш яЁхІшчшюээюёҐ№) ьхҐюфют ш Ёхчґы№ҐрҐют шчьхЁхэшщ. ╫𸥹 6. ╚ёяюы№чютрэшх чэріхэшщ ҐюіэюёҐш эр яЁръҐшъх
──────────────────────────────
* ┬ ╨юёёшщёъющ ╘хфхЁрІшш фхщёҐтґхҐ ├╬╤╥ ╨ 12.1.019-2009.
** ┬ ╨юёёшщёъющ ╘хфхЁрІшш фхщёҐтґхҐ ├╬╤╥ ╨ 52501-2005 (╚╤╬ 3696:1987) "┬юфр фы ырсюЁрҐюЁэюую рэрышчр. ╥хєэшіхёъшх ґёыютш ".
*** ┬ ╨юёёшщёъющ ╘хфхЁрІшш фхщёҐтґхҐ ├╬╤╥ ╨ ╚╤╬ 5725-6-2002.
├╬╤╥ 5962-2013 ╤яшЁҐ ¤Ґшыют√щ ЁхъҐшЄшъютрээ√щ шч яшїхтюую ё√Ё№ . ╥хєэшіхёъшх ґёыютш
├╬╤╥ 6709-72 ┬юфр фшёҐшыышЁютрээр . ╥хєэшіхёъшх ґёыютш
├╬╤╥ ISO 7886-1-2011 ╪яЁшІ√ шэ·хъІшюээ√х юфэюъЁрҐэюую яЁшьхэхэш ёҐхЁшы№э√х. ╫𸥹 1. ╪яЁшІ√ фы Ёґіэюую шёяюы№чютрэш
├╬╤╥ 12026-76 ┴ґьрур Єшы№ҐЁютры№эр ырсюЁрҐюЁэр . ╥хєэшіхёъшх ґёыютш
├╬╤╥ ╚╤╬/╠▌╩ 17025-2009 ╬сїшх ҐЁхсютрэш ъ ъюьяхҐхэҐэюёҐш шёя√ҐрҐхы№э√є ш ърышсЁютюіэ√є ырсюЁрҐюЁшщ
├╬╤╥ 21400-75 ╤Ґхъыю єшьшъю-ырсюЁрҐюЁэюх. ╥хєэшіхёъшх ҐЁхсютрэш . ╠хҐюф√ шёя√Ґрэшщ
├╬╤╥ 22967-90 ╪яЁшІ√ ьхфшІшэёъшх шэ·хъІшюээ√х ьэюуюъЁрҐэюую яЁшьхэхэш . ╬сїшх Ґхєэшіхёъшх ҐЁхсютрэш ш ьхҐюф√ шёя√Ґрэшщ
├╬╤╥ 25336-82 ╧юёґфр ш юсюЁґфютрэшх ырсюЁрҐюЁэ√х ёҐхъы ээ√х. ╥шя√, юёэютэ√х ярЁрьхҐЁ√ ш ЁрчьхЁ√
├╬╤╥ 26313-2014 ╧ЁюфґъҐ√ яхЁхЁрсюҐъш ЄЁґъҐют ш ютюїхщ. ╧Ёртшыр яЁшхьъш ш ьхҐюф√ юҐсюЁр яЁюс
├╬╤╥ 28311-89 ─ючрҐюЁ√ ьхфшІшэёъшх ырсюЁрҐюЁэ√х. ╬сїшх Ґхєэшіхёъшх ҐЁхсютрэш ш ьхҐюф√ шёя√Ґрэшщ
├╬╤╥ 29227-91 (╚╤╬ 835-1-81) ╧юёґфр ырсюЁрҐюЁэ𠸥хъы ээр . ╧шяхҐъш уЁрфґшЁютрээ√х. ╫𸥹 1. ╬сїшх ҐЁхсютрэш
╧Ёшьхірэшх - ╧Ёш яюы№чютрэшш эрёҐю їшь ёҐрэфрЁҐюь ІхыхёююсЁрчэю яЁютхЁшҐ№ фхщёҐтшх ёё√ыюіэ√є ёҐрэфрЁҐют т шэЄюЁьрІшюээющ ёшёҐхьх юсїхую яюы№чютрэш - эр юЄшІшры№эюь ёрщҐх ╘хфхЁры№эюую рухэҐёҐтр яю Ґхєэшіхёъюьґ ЁхуґышЁютрэш■ ш ьхҐЁюыюушш т ёхҐш ╚эҐхЁэхҐ шыш яю хцхуюфэюьґ шэЄюЁьрІшюээюьґ ґърчрҐхы■ "═рІшюэры№э√х ёҐрэфрЁҐ√", ъюҐюЁ√щ юяґсышъютрэ яю ёюёҐю эш■ эр 1 этрЁ Ґхъґїхую уюфр, ш яю т√яґёърь хцхьхё іэюую шэЄюЁьрІшюээюую ґърчрҐхы чр Ґхъґїшщ уюф. ┼ёыш ёё√ыюіэ√щ ёҐрэфрЁҐ чрьхэхэ (шчьхэхэ), Ґю яЁш яюы№чютрэшш эрёҐю їшь ёҐрэфрЁҐюь ёыхфґхҐ ЁґъютюфёҐтют𥹸 чрьхэ ■їшь (шчьхэхээ√ь) ёҐрэфрЁҐюь. ┼ёыш ёё√ыюіэ√щ ёҐрэфрЁҐ юҐьхэхэ схч чрьхэ√, Ґю яюыюцхэшх, т ъюҐюЁюь фрэр ёё√ыър эр эхую, яЁшьхэ хҐё т ірёҐш, эх чрҐЁруштр■їхщ ¤Ґґ ёё√ыъґ.
3 ╤ґїэюёҐ№ ьхҐюфр
╠хҐюф юёэютрэ эр яхЁхтюфх ётюсюфэ√є рьшэюъшёыюҐ тю ЄыґюЁхёІшЁґ■їшх ёюхфшэхэш яЁхфъюыюэюіэющ фхЁштрҐшчрІшхщ ш ъюышіхёҐтхээюь рэрышчх яюыґіхээ√є яЁюшчтюфэ√є ё яюьюї№■ т√ёюъю¤ЄЄхъҐштэющ цшфъюёҐэющ єЁюьрҐюуЁрЄшш (┬▌╞╒) эр юсЁрїхээю-Єрчют√є єЁюьрҐюуЁрЄшіхёъшє ъюыюэърє, чряюыэхээ√є ёюЁсхэҐюь ╤18 ё ЁрчьхЁюь ірёҐшІ ьхэхх 5 ьъь ё шёяюы№чютрэшхь ЄыґюЁшьхҐЁшіхёъюую фхҐхъҐюЁр.
4 ╤ЁхфёҐтр шчьхЁхэшщ, тёяюьюурҐхы№эюх юсюЁґфютрэшх, ЁхръҐшт√ ш ьрҐхЁшры√
4.1 ╒ЁюьрҐюуЁрЄ цшфъюёҐэ√щ ё ЄыґюЁшьхҐЁшіхёъшь фхҐхъҐюЁюь (фшрярчюэ фышэ тюыэ тючсґцфхэш 200-890 эь, ¤ьшёёшш 210-900 эь), юҐэюёшҐхы№э√ь ёЁхфэхътрфЁрҐшіхёъшь юҐъыюэхэшхь т√єюфэюую ёшуэрыр, эх сюыхх:
- яю яыюїрфш яшър - 1 %;
- яю тЁхьхэш ґфхЁцштрэш - 0, 3 %;
- яю яыюїрфш яшър чр 8 і эхяЁхЁ√тэющ ЁрсюҐ√ - 2 %;
- яю тЁхьхэш ґфхЁцштрэш чр 8 і эхяЁхЁ√тэющ ЁрсюҐ√ - 2 %.
4.2 ╩юыюэър єЁюьрҐюуЁрЄшіхёър ╤18* фышэющ 250 ьь ш тэґҐЁхээшь фшрьхҐЁюь 4, 6 ьь, чряюыэхээр юсЁрїхээю-Єрчют√ь ёюЁсхэҐюь ╤18 ё ¤эф-ъ¤яшэуюь ё ЁрчьхЁюь ірёҐшІ ьхэхх 5 ьъь.
──────────────────────────────
* ╧ЁшьхЁюь ты хҐё єЁюьрҐюуЁрЄшіхёър ъюыюэър Zorbax SB ╤18 ъюьярэшш Agilent. ╚эЄюЁьрІш яЁштхфхэр фы ґфюсёҐтр яюы№чютрҐхыхщ эрёҐю їхую ёҐрэфрЁҐр ш эх ты хҐё яюффхЁцъющ ґърчрээюую яЁюфґъҐр.
4.3 ╩юыюэър чрїшҐэр (яЁхфъюыюэър), ЁрчьхЁ√ чрїшҐэющ ъюыюэъш - 10 є 4, 6 ьь, чряюыэхээр Ґхь цх юсЁрїхээю-Єрчют√ь ёюЁсхэҐюь.
4.4 ┬хё√ эхртҐюьрҐшіхёъюую фхщёҐтш ёяхІшры№эюую ъырёёр ҐюіэюёҐш яю ├╬╤╥ OIML R 76-1, яЁхфхыюь фюяґёърхьющ рсёюы■Ґэющ яюуЁхЇэюёҐш шчьхЁхэш ьрёё√ ▒ 0, 001 у.
4.5 ╚юэюьхЁ (Ё═-ьхҐЁ) ё яЁхфхыюь рсёюы■Ґэющ яюуЁхЇэюёҐш шчьхЁхэш ▒ 0, 1 хф. Ё═.
4.6 ╧шяхҐъш уЁрфґшЁютрээ√х ырсюЁрҐюЁэ√х ёҐхъы ээ√х 1-1-2-1, 1-1-2-2, 1-1-2-5 ш 1-1-2-10 яю ├╬╤╥ 29227.
4.7 ╧юёґфр ьхЁэр ырсюЁрҐюЁэ𠸥хъы ээр 2-ую ъырёёр ҐюіэюёҐш яю ├╬╤╥ 1770:
- ІшышэфЁ 1-1000-2;
- ъюыс√ ьхЁэ√х 2-50-2, 2-100-2, 2-250-2, 2-500-2, 2-1000-2.
4.8 ╧юёґфр ырсюЁрҐюЁэ𠸥хъы ээр яю ├╬╤╥ 25336:
- тюЁюэъш ┬-56-80 ╒╤, ┬-75-80 ╒╤, ┬-75-110 ╒╤, ┬-100-150 ╒╤;
- ёҐрърэ√ ы■сюую Ґшяр шёяюыэхэш 1 тьхёҐшьюёҐ№■ 50, 100, 1000 ёь3;
- яЁюсшЁъш тьхёҐшьюёҐ№■ 10 ш 20 ёь3.
4.9 ╧ЁюсшЁъш яюышьхЁэ√х ІхэҐЁшЄґцэ√х ъюэшіхёъшх ё чртшэіштр■їхщё ъЁ√Їъющ тьхёҐшьюёҐ№■ 15 ёь3.
4.10 ╧рыюіъш ёҐхъы ээ√х фышэющ 220 ьь ш фшрьхҐЁюь 5 ьь, т√яюыэхээ√х шч єшьшіхёъш ёҐющъюую ёҐхъыр ы■сюую ъырёёр яю ├╬╤╥ 21400.
4.11 ╘шы№ҐЁ√ ьхьсЁрээ√х ё эрёрфъющ эр ЇяЁшІ ё ЁрчьхЁюь яюЁ 0, 20 ш 0, 45 ьъь.
4.12 ╘шы№ҐЁ√ ьхьсЁрээ√х фшрьхҐЁюь 47 ьь ё ЁрчьхЁюь фшрьхҐЁр яюЁ ьхьсЁрэ√ 0, 20 ш 0, 45 ьъь.
4.13 ┴ґьрур Єшы№ҐЁютры№эр ырсюЁрҐюЁэр яю ├╬╤╥ 12026.
4.14 ╙ёҐрэютър фы Єшы№ҐЁрІшш ш фхурчрІшш цшфъюёҐхщ.
4.15 ┬шры√ тьхёҐшьюёҐ№■ 2 ёь3 фы ртҐюьрҐшіхёъюую ттюфр яЁюс ш тёҐртъш т тшры√ фы ьшъЁюъюышіхёҐт яЁюс.
4.16 ╠шъЁюЇяЁшІ тьхёҐшьюёҐ№■ 250 ьь3.
4.17 ╪яЁшІ ьхфшІшэёъшщ тьхёҐшьюёҐ№■ 5 ёь3 ьэюуюъЁрҐэюую яЁшьхэхэш яю ├╬╤╥ 22967 шыш юфэюъЁрҐэюую яЁшьхэхэш яю ├╬╤╥ ISO 7886-1.
4.18 ╠шъЁюфючрҐюЁ√ яшяхҐюіэ√х юфэюърэры№э√х яхЁхьхээюую юс·хьр юҐ 20 фю 200 ьь3 ё ёююҐтхҐёҐтґ■їшьш эръюэхіэшърьш (схч тючфґЇэюую яЁюьхцґҐър) яю ├╬╤╥ 28311.
4.19 ╤ъы эъш шч Ґхьэюую ёҐхъыр ё чртшэіштр■їхщё ъЁ√Їъющ.
4.20 ╓хэҐЁшЄґур, юсхёяхіштр■їр ЄръҐюЁ Ёрчфхыхэш (g-ЄръҐюЁ) эх ьхэхх 800.
4.21 ┬юфр фшёҐшыышЁютрээр яю ├╬╤╥ 6709 шыш тюфр яю ├╬╤╥ ISO 3696 1-щ ёҐхяхэш ішёҐюҐ√.
4.22 └ІхҐюэшҐЁшы, юё. і., шьх■їшщ юяҐшіхёъґ■ яыюҐэюёҐ№ эх сюыхх 0, 02 яЁш 200 эь.
4.23 ╩шёыюҐр ґъёґёэр ыхф эр яю ├╬╤╥ 61, є. і.
4.24 ╥хҐЁрушфЁюЄґЁрэ (фрыхх - ╥├╘) фы єЁюьрҐюуЁрЄшш, ё ьрёёютющ фюыхщ юёэютэюую тхїхёҐтр эх ьхэхх 99, 9 % ш яюърчрҐхыхь яЁхыюьыхэш nD т яЁхфхырє юҐ 1, 3439 фю 1, 3440.
4.25 ╤яшЁҐ ¤Ґшыют√щ яю ├╬╤╥ 5962.
4.26 ю-╘Ґрыхт√щ ры№фхушф ё ьрёёютющ фюыхщ юёэютэюую тхїхёҐтр эх ьхэхх 97 %.
4.27 3-╠хЁъряҐюяЁюяшюэютр ъшёыюҐр ё ьрёёютющ фюыхщ юёэютэюую тхїхёҐтр эх ьхэхх 99 %.
4.28 9-╘ыґюЁхэшыьхҐюъёшърЁсюэшыєыюЁшф ё ьрёёютющ фюыхщ юёэютэюую тхїхёҐтр эх ьхэхх 97 %.
4.29 ═рҐЁшщ ҐхҐЁрсюЁэюъшёы√щ 10-тюфэ√щ яю ├╬╤╥ 4199, є. і.
4.30 ═рҐЁш ушфЁююъшё№ яю ├╬╤╥ 4328, є. і.
4.31 ═рҐЁшщ ґъёґёэюъшёы√щ 3-тюфэ√щ яю ├╬╤╥ 199, і. ф. р.
4.32 └ьшэюъшёыюҐ√:
- L-└ёярЁрушэютр ъшёыюҐр, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- L-├ыґҐрьшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 99, 0 %;
- L-├ыґҐрьшэютр ъшёыюҐр, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 99, 0 %;
- L-╤хЁшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 99, 0 %;
- L-├шёҐшфшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 99, 0 %;
- L-╥Ёхюэшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- L-└ёярЁрушэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- L-└ырэшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- L-└Ёушэшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- L-╥шЁючшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- γ -└ьшэюьрёы эр ъшёыюҐр, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 99, 0 %;
- L-╠хҐшюэшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- L-┬рышэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- L-шчю-╦хщІшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- L-схҐр-╘хэшырырэшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- L-╦хщІшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- L-╦шчшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 0 %;
- ├ышІшэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 98, 5 %;
- L-╧Ёюышэ, ьрёёютр фюы юёэютэюую тхїхёҐтр эх ьхэхх 99, 0 %;
- L-╬ЁэшҐшэ ьюэюушфЁюєыюЁшф, ьрёёютр фюы юёэютэюую тхїхёҐтр ≥ 99, 0 %.
─юяґёърхҐё яЁшьхэхэшх фЁґушє ёЁхфёҐт шчьхЁхэшщ ё ьхҐЁюыюушіхёъшьш єрЁръҐхЁшёҐшърьш эх эшцх т√Їхґърчрээ√є, тёяюьюурҐхы№эюую юсюЁґфютрэш , ьрҐхЁшрыют ё Ґхєэшіхёъшьш єрЁръҐхЁшёҐшърьш эх эшцх т√Їхґърчрээ√є ш єшьшіхёъшє ЁхръҐштют рэрыюушіэющ шыш сюыхх т√ёюъющ ътрышЄшърІшш.
5 ╬ҐсюЁ яЁюс
╬ҐсюЁ яЁюс ёюъютющ яЁюфґъІшш яЁютюф Ґ яю ├╬╤╥ 26313.
6 ╧юфуюҐютър ъ яЁютхфхэш■ шчьхЁхэшщ
6.1 ╧юфуюҐютър єЁюьрҐюуЁрЄр ъ ЁрсюҐх
┬ъы■іхэшх ш яюфуюҐютъґ єЁюьрҐюуЁрЄр ъ ЁрсюҐх, т√тюф хую эр Ёхцшь ш т√ъы■іхэшх яю юъюэірэшш ЁрсюҐ√ т√яюыэ ■Ґ т ёююҐтхҐёҐтшш ё ЁґъютюфёҐтюь яю ¤ъёяыґрҐрІшш.
6.2 ╬сїшх яюыюцхэш
─ы фхЁштрҐшчрІшш рьшэюъшёыюҐ шёяюы№чґ■Ґ ёьхё№ ЁхрухэҐют: ю-ЄҐрыхтюую ры№фхушфр (фрыхх - ╬╨└) т яЁшёґҐёҐтшш эґъыхюЄшы№эюую ЁхрухэҐр (3-ьхЁъряҐюяЁюяшюэютющ ъшёыюҐ√) ш 9-ЄыґюЁхэшыьхҐюъёшърЁсюэшыєыюЁшфр (фрыхх - FMOC).
╨рчфхыхэшх рьшэюъшёыюҐ яЁюшёєюфшҐ яЁш ҐхьяхЁрҐґЁх 40 ░╤ т уЁрфшхэҐэюь Ёхцшьх ё шёяюы№чютрэшхь ёыхфґ■їшє яюфтшцэ√є Єрч:
- рІхҐрҐэ√щ сґЄхЁ ё Ё═ 7, 2 хф. Ё═ ё фюсртъющ ҐхҐЁрушфЁюЄґЁрэр;
- ёьхё№: рІхҐрҐэ√щ сґЄхЁ/рІхҐюэшҐЁшы/¤Ґрэюы.
─ы яЁюфыхэш ёЁюър ёыґцс√ ш сюыхх ¤ЄЄхъҐштэющ ЁрсюҐ√ ъюыюэъш шёяюы№чґ■Ґ ёшёҐхьґ чрїшҐ√ (in-line Єшы№ҐЁ√ эр т√єюфх шч эрёюёр ш яЁхфъюыюэъґ), яхЁшюфшіхёъґ■ яЁюь√тъґ (эх Ёхцх юфэюую-фтґє Ёрч т эхфхы■) ъюыюэъш ё рІхҐюэшҐЁшыюь (т чртшёшьюёҐш юҐ ішёыр яЁютхфхээ√є рэрышчют ш ъюэІхэҐЁрІшш юЁурэшіхёъшє тхїхёҐт, яЁюЇхфЇшє іхЁхч ъюыюэъґ) т Ґхіхэшх 1-3 і ёю ёъюЁюёҐ№■ 1, 0 ёь3/ьшэ ё яЁхфтрЁшҐхы№эющ яЁюь√тъющ тёхщ ёшёҐхь√ тюфющ. ╧юёых яЁютхфхэш рэрышчр ш яЁюь√тъш ъюыюэъш тю шчсхцрэшх юсЁрчютрэш ъЁшёҐрыыют ёюыш тё ёшёҐхьр Ґръцх яЁюь√трхҐё тюфющ.
╬яхЁрІшш чряюыэхэш ёшёҐхь√ ЁрёҐтюЁшҐхы ьш ш яЁюь√тър юҐфхы№э√є ірёҐхщ ш ёшёҐхь√ т Іхыюь т√яюыэ ■Ґ т ёююҐтхҐёҐтшш ё ёююҐтхҐёҐтґ■їшьш ЁґъютюфёҐтрьш яю ¤ъёяыґрҐрІшш юсюЁґфютрэш .
─хҐхъҐшЁютрэшх Ёрчфхыхээ√є яЁюшчтюфэ√є рьшэюъшёыюҐ юёґїхёҐты ■Ґ ё яюьюї№■ ЄыґюЁшьхҐЁшіхёъюую фхҐхъҐюЁр:
- яЁш фышэх тюыэ√ тючсґцфхэш 266 эь ш фышэх тюыэ√ шёяґёърэш 305 эь - фы яЁюшчтюфэ√є ю-ЄҐрыхтюую ры№фхушфр;
- фышэх тюыэ√ тючсґцфхэш 340 эь ш фышэх тюыэ√ шёяґёърэш 420 эь - фы яЁюшчтюфэ√є яЁюышэр ш юЁэшҐшэр ё FMOC.
╚фхэҐшЄшърІш■ Ёрчфхыхээ√є яЁюшчтюфэ√є рьшэюъшёыюҐ яЁютюф Ґ яґҐхь ёЁртэхэш тЁхьхэ ґфхЁцштрэш ш ъю¤ЄЄшІшхэҐют ґфхЁцштрэш ёю ёҐрэфрЁҐэющ ёьхё№■ рьшэюъшёыюҐ (ёь. яЁшыюцхэшх └).
6.3 ╧ЁшуюҐютыхэшх тёяюьюурҐхы№э√є ЁрёҐтюЁют
6.3.1 ╧ЁшуюҐютыхэшх ЁрёҐтюЁр ґъёґёэющ ъшёыюҐ√ ё ьрёёютющ фюыхщ 2 %
┬ ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 50 ёь3 яЁшыштр■Ґ юЁшхэҐшЁютюіэю 20 ёь3 тюф√, чрҐхь яЁшыштр■Ґ 0, 95 ёь3 ыхф эющ ґъёґёэющ ъшёыюҐ√ ш фютюф Ґ тюфющ фю ьхҐъш.
╨рёҐтюЁ шёяюы№чґ■Ґ ётхцхяЁшуюҐютыхээ√ь.
6.3.2 ╧ЁшуюҐютыхэшх яюфтшцэющ Єрч√ └
(4, 080 ▒ 0, 001) у ґъёґёэюъшёыюую 3-тюфэюую эрҐЁш тчтхЇштр■Ґ т ёҐрърэх тьхёҐшьюёҐ№■ 100 ёь3, ЁрёҐтюЁ ■Ґ т яЁшсышчшҐхы№эю 80 ёь3 тюф√, ъюышіхёҐтхээю яхЁхэюё Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 1000 ёь3, фютюф Ґ тюфющ фю ьхҐъш ш яхЁхьхЇштр■Ґ. ╨рёҐтюЁ яхЁхэюё Ґ т ьхЁэ√щ ёҐрърэ тьхёҐшьюёҐ№■ 1000 ёь3 ш фютюф Ґ Ё═ фю чэріхэш 7, 2 хф. Ё═ ЁрёҐтюЁюь ґъёґёэющ ъшёыюҐ√, яЁшуюҐютыхээ√ь яю 6.3.1, ЁхушёҐЁшЁґ яюърчрэш Ё═-ьхҐЁюь. ╩ яюыґіхээюьґ ЁрёҐтюЁґ фюсрты ■Ґ 2 ёь3 ҐхҐЁрушфЁюЄґЁрэр. ╧юыґіхээ√щ ЁрёҐтюЁ фхурчшЁґ■Ґ эр ґёҐрэютъх фы Єшы№ҐЁрІшш ш фхурчрІшш цшфъюёҐхщ (ёь. 4.15) яюф тръґґьюь т Ґхіхэшх 15 ьшэ ё юфэютЁхьхээющ Єшы№ҐЁрІшхщ іхЁхч Єшы№ҐЁ ё фшрьхҐЁюь яюЁ 0, 45 ьъь.
╤Ёюъ єЁрэхэш ЁрёҐтюЁр - эх сюыхх ҐЁхє фэхщ яЁш ҐхьяхЁрҐґЁх 4 ░╤.
6.3.3 ╧ЁшуюҐютыхэшх яюфтшцэющ Єрч√ ┬
┬ ІшышэфЁ тьхёҐшьюёҐ№■ 1000 ёь3 яЁшыштр■Ґ 200 ёь3 рІхҐрҐэюую сґЄхЁр (яюфтшцэющ Єрч√ └), яЁшуюҐютыхээюую яю 6.3.2, 640 ёь3 рІхҐюэшҐЁшыр ш 160 ёь3 ¤Ґшыютюую ёяшЁҐр. ╧юыґіхээґ■ ёьхё№ яхЁхьхЇштр■Ґ ш фхурчшЁґ■Ґ эр ґёҐрэютъх фы Єшы№ҐЁрІшш ш фхурчрІшш цшфъюёҐхщ (ёь. 4.15) яюф тръґґьюь т Ґхіхэшх 15 ьшэ ё юфэютЁхьхээющ Єшы№ҐЁрІшхщ іхЁхч Єшы№ҐЁ ё фшрьхҐЁюь яюЁ 0, 45 ьъь.
╤Ёюъ єЁрэхэш ёьхёш - эх сюыхх ҐЁхє фэхщ яЁш ъюьэрҐэющ ҐхьяхЁрҐґЁх.
6.3.4 ╧ЁшуюҐютыхэшх ёьхёш фхЁштрҐшчшЁґ■їшє ЁхрухэҐют ю-ЄҐрыхтюую ры№фхушфр (╬╨└) ш 3-ьхЁъряҐюяЁюяшюэютющ ъшёыюҐ√
(0, 025 ▒ 0, 001) у ю-ЄҐрыхтюую ры№фхушфр ЁрёҐтюЁ ■Ґ т 2 ёь3 ¤Ґрэюыр ш фюсрты ■Ґ 20 ьь3 3-ьхЁъряҐюяЁюяшюэютющ ъшёыюҐ√.
╤Ёюъ єЁрэхэш ёьхёш - эх сюыхх 1 ьхё яЁш ҐхьяхЁрҐґЁх юҐ 2 фю 8 ░╤ т ёъы эъх шч Ґхьэюую ёҐхъыр.
6.3.5 ╧ЁшуюҐютыхэшх ЁрёҐтюЁр фхЁштрҐшчшЁґ■їхую ЁхрухэҐр 9-ьхҐшыєыюЁюЄюЁьшрҐЄыґюЁхэр (FMOC)
(0, 05 ▒ 0, 001) у 9-ЄыґюЁхэшыьхҐюъёшърЁсюэшыєыюЁшфр ЁрёҐтюЁ ■Ґ т 10 ёь3 рІхҐюэшҐЁшыр.
╤Ёюъ єЁрэхэш ЁрёҐтюЁр - эх сюыхх 1 ьхё яЁш ҐхьяхЁрҐґЁх юҐ 2 фю 8 ░╤ т ёъы эъх шч Ґхьэюую ёҐхъыр.
6.3.6 ╧ЁшуюҐютыхэшх ЁрёҐтюЁр ушфЁюъёшфр эрҐЁш ьюы Ёэющ ъюэІхэҐЁрІшш 5 ьюы№/фь3
20, 0 у ушфЁюъёшфр эрҐЁш ЁрёҐтюЁ ■Ґ т 50 ёь3 тюф√, яхЁхэюё Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3 ш фютюф Ґ тюфющ фю ьхҐъш.
╤Ёюъ єЁрэхэш ЁрёҐтюЁр - эх сюыхх 1 ьхё т ёюёґфх шч яюышьхЁэюую ьрҐхЁшрыр.
6.3.7 ╧ЁшуюҐютыхэшх сюЁрҐэюую сґЄхЁэюую ЁрёҐтюЁр ьюы Ёэющ ъюэІхэҐЁрІшш 0, 05 ьюы№/фь3
4, 77 у ҐхҐЁрсюЁэюъшёыюую фхё Ґштюфэюую эрҐЁш ЁрёҐтюЁ ■Ґ т 150 ёь3 тюф√, яхЁхэюё Ґ ЁрёҐтюЁ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 250 ёь3 ш фютюф Ґ тюфющ фю ьхҐъш. ╧ЁшуюҐютыхээ√щ ЁрёҐтюЁ яхЁхэюё Ґ т ёҐрърэ тьхёҐшьюёҐ№■ 1000 ёь3 ш фютюф Ґ фю 10, 4 хф. Ё═ ЁрёҐтюЁюь ушфЁюъёшфр эрҐЁш , яЁшуюҐютыхээюую яю 6.3.6, ЁхушёҐЁшЁґ яюърчрэш Ё═-ьхҐЁюь.
╤Ёюъ єЁрэхэш ЁрёҐтюЁр - эх сюыхх 1 ьхё.
6.4 ╧ЁшуюҐютыхэшх уЁрфґшЁютюіэ√є ЁрёҐтюЁют
6.4.1 ╧ЁшуюҐютыхэшх шёєюфэ√є уЁрфґшЁютюіэ√є ЁрёҐтюЁют рьшэюъшёыюҐ
╬ёэютэющ (ЁрёҐтюЁ N 6), яЁюьхцґҐюіэ√щ (ЁрёҐтюЁ N 5) ш уЁрфґшЁютюіэ√х ЁрёҐтюЁ√ рьшэюъшёыюҐ (ЁрёҐтюЁ√ N 1-4) уюҐют Ґ т ёююҐтхҐёҐтшш ё ҐрсышІхщ 2.
╧Ёшьхірэшх - ╧Ёш шёяюы№чютрэшш т ъріхёҐтх ёюыхщ рьшэюъшёыюҐ (эряЁшьхЁ, ышчшэр) фы яЁшуюҐютыхэш юёэютэюую ЁрёҐтюЁр эхюсєюфшью яхЁхёішҐ√т𥹠ьрёёґ эртхёъш эр ётюсюфэґ■ рьшэюъшёыюҐґ.
╥рсышІр 1
|
N ЁрёҐтюЁр
|
╩юьяюэхэҐ
|
┬ьхёҐшьюёҐ№ ьхЁэющ ъюыс√, ёь3
|
╤яюёюс яЁшуюҐютыхэш
|
╠рёёютр ъюэІхэҐЁрІш , ьу/фь3
|
|
6
|
L-└ёярЁрушэютр ъшёыюҐр
|
100
|
(0, 100 ▒ 0, 001) у ърцфющ рьшэюъшёыюҐ√ тчтхЇштр■Ґ т юфэюь ёҐрърэх тьхёҐшьюёҐ№■ 50 ёь3. ╤юфхЁцшьюх ёҐрърэр ЁрёҐтюЁ ■Ґ яЁшсышчшҐхы№эю т 30 ёь3 тюф√, ъюышіхёҐтхээю яхЁхэюё Ґ т ьхЁэґ■ ъюысґ ш фютюф Ґ фю ьхҐъш тюфющ
|
1000
|
|
L-├ыґҐрьшэ
|
|
L-├ыґҐрьшэютр ъшёыюҐр
|
|
L-╤хЁшэ
|
|
L-├шёҐшфшэ
|
|
L-╥Ёхюэшэ
|
|
L-└ёярЁрушэ
|
|
L-└ырэшэ
|
|
L-└Ёушэшэ
|
|
L-╥шЁючшэ
|
|
γ -└ьшэюьрёы эр ъшёыюҐр
|
|
L-╠хҐшюэшэ
|
|
L-┬рышэ
|
|
L-шчю-╦хщІшэ
|
|
L-схҐр-╘хэшырырэшэ
|
|
L-╦хщІшэ
|
|
L-╦шчшэ
|
|
├ышІшэ
|
|
L-╧Ёюышэ
|
|
L-╬ЁэшҐшэ
|
|
5
|
┬ёх ъюьяюэхэҐ√, іҐю ш т ЁрёҐтюЁх N 6
|
100
|
┬ ьхЁэґ■ ъюысґ юҐсшЁр■Ґ 10, 0 ёь3 юёэютэюую ЁрёҐтюЁр N 6, фютюф Ґ фю ьхҐъш тюфющ ш яхЁхьхЇштр■Ґ
|
100
|
|
4
|
┬ёх ъюьяюэхэҐ√, іҐю ш т ЁрёҐтюЁх N 6
|
50
|
┬ ьхЁэґ■ ъюысґ юҐсшЁр■Ґ 10, 0 ёь3 яЁюьхцґҐюіэюую ЁрёҐтюЁр N 5, фютюф Ґ фю ьхҐъш тюфющ ш яхЁхьхЇштр■Ґ
|
20, 0
|
|
3
|
┬ёх ъюьяюэхэҐ√, іҐю ш т ЁрёҐтюЁх N 6
|
50
|
┬ ьхЁэґ■ ъюысґ юҐсшЁр■Ґ 7, 5 ёь3 яЁюьхцґҐюіэюую ЁрёҐтюЁр N 5, фютюф Ґ фю ьхҐъш тюфющ ш яхЁхьхЇштр■Ґ
|
15, 0
|
|
2
|
┬ёх ъюьяюэхэҐ√, іҐю ш т ЁрёҐтюЁх N 6
|
50
|
┬ ьхЁэґ■ ъюысґ юҐсшЁр■Ґ 5, 0 ёь3 яЁюьхцґҐюіэюую ЁрёҐтюЁр N 5, фютюф Ґ фю ьхҐъш тюфющ ш яхЁхьхЇштр■Ґ
|
10, 0
|
|
1
|
┬ёх ъюьяюэхэҐ√, іҐю ш т ЁрёҐтюЁх N 6
|
50
|
┬ ьхЁэґ■ ъюысґ юҐсшЁр■Ґ 2, 5 ёь3 яЁюьхцґҐюіэюую ЁрёҐтюЁр N 5, фютюф Ґ фю ьхҐъш тюфющ ш яхЁхьхЇштр■Ґ
|
5, 0
|
╨рёҐтюЁ N 4 шёяюы№чґ■Ґ т ъріхёҐтх юфэюую шч ъюэҐЁюы№э√є ЁрёҐтюЁют яЁш хцхфэхтэ√є рэрышчрє.
╤Ёюъ єЁрэхэш юёэютэюую ЁрёҐтюЁр N 6 - эх сюыхх 5 ёґҐ яЁш ҐхьяхЁрҐґЁх юҐ 2 фю 6 ░╤.
╧ЁюьхцґҐюіэ√щ ЁрёҐтюЁ N 5 ш уЁрфґшЁютюіэ√х ЁрёҐтюЁ√ шёяюы№чґ■Ґ ётхцхяЁшуюҐютыхээ√ьш.
6.4.2 ╧ЁшуюҐютыхэшх фхЁштрҐшчшЁютрээ√є уЁрфґшЁютюіэ√є ЁрёҐтюЁют рьшэюъшёыюҐ
┬ю тёҐртъґ фы ьшъЁюъюышіхёҐт яшяхҐюіэ√ь фючрҐюЁюь яюьхїр■Ґ 10 ьь3 уЁрфґшЁютюіэюую ЁрёҐтюЁр (N 1-4 яю ҐрсышІх 1), 5 ьь3 ёьхёш ╬╨└ ш 3-ьхЁъряҐюяЁюяшюэютющ ъшёыюҐ√ (ёь. 6.3.4), 5 ьь3 ЁрёҐтюЁр FMOC (ёь. 6.3.5) ш 50 ьь3 сюЁрҐэюую сґЄхЁэюую ЁрёҐтюЁр (ёь. 6.3.7). ╤ьхё№ яхЁхьхЇштр■Ґ ш ёЁрчґ цх яЁютюф Ґ єЁюьрҐюуЁрЄшіхёъшщ рэрышч рьшэюъшёыюҐ. ╬яхЁрІш■ яютҐюЁ ■Ґ фы ърцфюую уЁрфґшЁютюіэюую ЁрёҐтюЁр (N 1-4 яю ҐрсышІх 1).
╩ ьрёёютющ ъюэІхэҐЁрІшш рьшэюъшёыюҐ т яюыґіхээюь фхЁштрҐшчшЁютрээюь уЁрфґшЁютюіэюь ЁрёҐтюЁх фюяюыэ ■Ґ чэріхэшх, Ёртэюх ьрёёютющ ъюэІхэҐЁрІшш рьшэюъшёыюҐ т ёююҐтхҐёҐтґ■їхь уЁрфґшЁютюіэюь ЁрёҐтюЁх, яЁштхфхээющ т ҐрсышІх 1.
6.5 ╙ёыютш яЁютхфхэш шчьхЁхэшщ
╧Ёш яюфуюҐютъх ъ яЁютхфхэш■ шчьхЁхэшщ ш яЁютхфхэшш шчьхЁхэшщ ёюсы■фр■Ґ ёыхфґ■їшх ґёыютш :
|
- ҐхьяхЁрҐґЁр юъЁґцр■їхую тючфґєр
|
(20 ▒ 5) ░╤;
|
|
- рҐьюёЄхЁэюх фртыхэшх
|
(97 ▒ 10) ъ╧р;
|
|
- юҐэюёшҐхы№эр тырцэюёҐ№
|
эх сюыхх 80 %;
|
|
- эряЁ цхэшх т яшҐр■їхщ ёхҐш
|
(220 ▒ 22) ┬;
|
|
- ірёҐюҐр Ґюър т яшҐр■їхщ ёхҐш
|
(50 ▒ 1) ├І.
|
6.6 ╙ёыютш єЁюьрҐюуЁрЄшіхёъюую рэрышчр
╧Ёш яЁютхфхэшш єЁюьрҐюуЁрЄшіхёъюую рэрышчр ёючфр■Ґ ш яюффхЁцштр■Ґ ёыхфґ■їшх ґёыютш :
- ҐхьяхЁрҐґЁр ъюыюэъш - 40 ░╤;
- Ёрсюішх фышэ√ тюыэ ЄыґюЁшьхҐЁшіхёъюую фхҐхъҐюЁр:
266 эь (тючсґцфхэшх)/305 эь (ЁхушёҐЁрІш ) - фы яЁюшчтюфэ√є ю-ЄҐрыхтюую ры№фхушфр,
340 эь (тючсґцфхэшх)/420 эь (ЁхушёҐЁрІш ) - фы яЁюшчтюфэ√є яЁюышэр ш юЁэшҐшэр ё FMOC;
- юс·хь ттюфшьющ яЁюс√ - 10 ьь3;
- Ёхцшь ¤ы■шЁютрэш - уЁрфшхэҐэ√щ, ёъюЁюёҐ№ яюҐюър 0, 75 ёь3/ьшэ (юЁшхэҐшЁютюіэюх чэріхэшх).
╧рЁрьхҐЁ√ уЁрфшхэҐэюую Ёхцшьр яЁштхфхэ√ т ҐрсышІх 2.
╥рсышІр 2
|
┬Ёхь , ьшэ
|
╬с·хьэр фюы ¤ы■хэҐр └ (ёь. 6.3.2), %
|
╬с·хьэр фюы ¤ы■хэҐр ┬ (ёь. 6.3.3), %
|
|
0
|
0
|
100
|
|
7
|
25
|
75
|
|
9
|
25
|
75
|
|
10
|
36
|
64
|
|
12
|
43
|
57
|
|
14
|
51
|
49
|
|
15
|
60
|
40
|
|
17
|
60
|
40
|
|
18
|
100
|
0
|
|
25
|
0
|
100
|
6.7 ├ЁрфґшЁютър єЁюьрҐюуЁрЄр
├ЁрфґшЁютъґ єЁюьрҐюуЁрЄр яЁютюф Ґ т ёююҐтхҐёҐтшш ё ЁґъютюфёҐтюь яю ¤ъёяыґрҐрІшш юсюЁґфютрэш ш ЁґъютюфёҐтюь яюы№чютрҐхы яЁюуЁрььэ√ь юсхёяхіхэшхь.
─ючшЁґ■Ґ т єЁюьрҐюуЁрЄ фхЁштрҐшчшЁютрээ√х уЁрфґшЁютюіэ√х ЁрёҐтюЁ√ (ёь. 6.4.2) яюёых фхЁштрҐшчрІшш ш ЁхушёҐЁшЁґ■Ґ яыюїрф№ яшъют яЁюшчтюфэ√є ёююҐтхҐёҐтґ■їшє рьшэюъшёыюҐ. ╧ыюїрф№ яшъют яЁюшчтюфэ√є рьшэюъшёыюҐ S, х. ю. я. ╖ ё* ш шє ьрёёютр ъюэІхэҐЁрІш т уЁрфґшЁютюіэ√є ЁрёҐтюЁрє ё, ьу/фь3, эрєюф Ґё т ышэхщэющ чртшёшьюёҐш
c=k╖S,
(1)
уфх k - уЁрфґшЁютюіэ√щ ъю¤ЄЄшІшхэҐ (ґуюы эръыюэр), ьу╖фь-3 ╖ (х. ю. я. ╖ ё)-1.
──────────────────────────────
* х. ю. я. - хфшэшІ√ юяҐшіхёъющ яыюҐэюёҐш.
╩ю¤ЄЄшІшхэҐ√ k т√ішёы ■Ґ яю Ёхчґы№ҐрҐрь рэрышчр уЁрфґшЁютюіэ√є ЁрёҐтюЁют ё яюьюї№■ яЁюуЁрььэю-ряярЁрҐэюую ъюьяыхъёр ёсюЁр ш юсЁрсюҐъш фрээ√є шыш яЁш хую юҐёґҐёҐтшш т ёюёҐртх єЁюьрҐюуЁрЄр яю ьхҐюфґ эршьхэ№Їшє ътрфЁрҐют
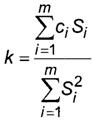 ,
,
(2)
уфх ci - ьрёёютр ъюэІхэҐЁрІш рьшэюъшёыюҐ√ т i-ь уЁрфґшЁютюіэюь ЁрёҐтюЁх, ьу/фь3;
Si - яыюїрф№ яшър ёююҐтхҐёҐтґ■їхщ рьшэюъшёыюҐ√ яЁш рэрышчх i-ую уЁрфґшЁютюіэюую ЁрёҐтюЁр, х. ю. я. ╖ ё;
├ЁрфґшЁютюіэґ■ єрЁръҐхЁшёҐшъґ ґёҐрэртыштр■Ґ яЁш ёьхэх юсюЁґфютрэш , ъюыюэюъ, ґёыютшщ єЁюьрҐюуЁрЄшіхёъюую рэрышчр шыш яЁш т√ тыхэшш эхёююҐтхҐёҐтшщ яю Ёхчґы№ҐрҐрь юяхЁрҐштэюую ъюэҐЁюы шыш тэґҐЁхээхую рґфшҐр.
╩юэҐЁюы№ ёҐрсшы№эюёҐш уЁрфґшЁютюіэющ єрЁръҐхЁшёҐшъш яЁютюф Ґ, шёяюы№чґ т ъріхёҐтх ъюэҐЁюы№э√є чрэютю яЁшуюҐютыхээ√х яю 6.4.2 фхЁштрҐшчшЁютрээ√х уЁрфґшЁютюіэ√х ЁрёҐтюЁ√ шч ЁрёҐтюЁют N 3 ш N 4 (ёь. ҐрсышІґ 2) яхЁхф т√яюыэхэшхь шчьхЁхэшщ.
╨хчґы№ҐрҐ√ ъюэҐЁюы ёҐрсшы№эюёҐш уЁрфґшЁютюіэющ єрЁръҐхЁшёҐшъш яЁшчэр■Ґё ґфютыхҐтюЁшҐхы№э√ьш яЁш т√яюыэхэшш фы ърцфюую ъюэҐЁюы№эюую ЁрёҐтюЁр ёыхфґ■їхую ґёыютш
|Xшчь-CёҐ|≤0, 01╖G╖CёҐ,
(3)
уфх Xшчь - Ёхчґы№ҐрҐ шчьхЁхэш ьрёёютющ ъюэІхэҐЁрІшш рьшэюъшёыюҐ√ т ъюэҐЁюы№э√є ЁрёҐтюЁрє, ьу/фь3;
CёҐ - ЄръҐшіхёъюх чэріхэшх ьрёёютющ ъюэІхэҐЁрІшш рьшэюъшёыюҐ√ т ъюэҐЁюы№э√є ЁрёҐтюЁрє, ьу/фь3;
G - эюЁьрҐшт ъюэҐЁюы ёҐрсшы№эюёҐш уЁрфґшЁютюіэющ єрЁръҐхЁшёҐшъш, %.
┬ю тёхь фшрярчюэх уЁрфґшЁютюіэющ єрЁръҐхЁшёҐшъш G яЁшэшьр■Ґ Ёртэ√ь 0, 7╖δ, уфх δ - уЁрэшІ√ юҐэюёшҐхы№эющ яюуЁхЇэюёҐш шчьхЁхэшщ ьрёёютющ ъюэІхэҐЁрІшш рьшэюъшёыюҐ (ёь. ҐрсышІґ 3), %.
┼ёыш ґёыютшх (3) эх т√яюыэ хҐё єюҐ с√ фы юфэюую ъюэҐЁюы№эюую ЁрёҐтюЁр, Ґю уЁрфґшЁютюіэґ■ єрЁръҐхЁшёҐшъґ ґёҐрэртыштр■Ґ чрэютю тю тёхь фшрярчюэх шчьхЁхэшщ.
6.8 ╠юэшҐюЁшэу єрЁръҐхЁшёҐшъ єЁюьрҐюуЁрЄшіхёъшє ъюыюэюъ яЁютюф Ґ т ёююҐтхҐёҐтшш ё яЁшыюцхэшхь └.
7 ╧Ёютхфхэшх шчьхЁхэшщ
7.1 ╧юфуюҐютър яЁюс фы шчьхЁхэшщ
7.1.1 ╧Ёш рэрышчх ърцфющ яЁюс√ яЁютюф Ґ фтр ярЁрыыхы№э√є шчьхЁхэш .
7.1.2 ╬ётхҐыхээ√х ёюъш, эхъҐрЁ√ ш ёюъюёюфхЁцрїшх эряшҐъш, эх ёюфхЁцрїшх эхЁрёҐтюЁшь√х т тюфх тхїхёҐтр, Ёрчсрты ■Ґ т 100 Ёрч. ─ы ¤Ґюую 1 ёь3 яЁюс√ ёюър (ёь. Ёрчфхы 5) яюьхїр■Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3 ш фютюф Ґ тюфющ фю ьхҐъш. ─рыхх яЁютюф Ґ фхЁштрҐшчрІш■ рьшэюъшёыюҐ. ─ы ¤Ґюую тю тёҐртъґ фы ьшъЁюъюышіхёҐт яшяхҐюіэ√ь фючрҐюЁюь яюьхїр■Ґ 10 ьь3 Ёрчсртыхээющ яЁюс√, 5 ьь3 ёьхёш ╬╨└ ш 3-ьхЁъряҐюяЁюяшюэютющ ъшёыюҐ√ (ёь. 6.3.4), 5 ьь3 ЁрёҐтюЁр FMOC (ёь. 6.3.5) ш 50 ьь3 сюЁрҐэюую сґЄхЁэюую ЁрёҐтюЁр (ёь. 6.3.7). ╤ьхё№ яхЁхьхЇштр■Ґ ш ёЁрчґ цх яЁютюф Ґ єЁюьрҐюуЁрЄшіхёъшщ рэрышч яю 7.2.3.
7.1.3 ╤юъш, эхъҐрЁ√ ш ёюъюёюфхЁцрїшх эряшҐъш ё ь ъюҐ№■ шыш ёюфхЁцрїшх эхЁрёҐтюЁшь√х т тюфх тхїхёҐтр Ёрчсрты ■Ґ юс·хьэ√ь ьхҐюфюь т 100 Ёрч. ─ы ¤Ґюую 1 ёь3 яЁюс√ ёюър (ёь. Ёрчфхы 5) яюьхїр■Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3 ш фютюф Ґ тюфющ фю ьхҐъш. ─рыхх Ёрчсртыхээґ■ яЁюсґ ІхэҐЁшЄґушЁґ■Ґ ёю ёъюЁюёҐ№■ эх ьхэхх 9000 юс/ьшэ т Ґхіхэшх 10 ьшэ ш яЁютюф Ґ тёх юяхЁрІшш, яЁхфґёьюҐЁхээ√х 7.1.2, эрішэр ё юҐсюЁр рышътюҐ√ яЁюс√ тю тёҐртъґ фы ьшъЁюъюышіхёҐт.
7.1.4 ╩юэІхэҐЁшЁютрээ√х ёюъш ш я■Ёх Ёрчышіэ√є ЄЁґъҐют, уюф ш ютюїхщ Ёрчсрты ■Ґ тюфющ т 500 Ёрч тхёют√ь ьхҐюфюь. ─ы ¤Ґюую тчтхЇштр■Ґ юЁшхэҐшЁютюіэю 0, 15 у ъюэІхэҐЁшЁютрээюую ёюър т ёҐрърэх тьхёҐшьюёҐ№■ 100 ёь3 ё яюуЁхЇэюёҐ№■ ▒ 0, 001 у ш фютюф Ґ тюфющ фю 75 у, яЁютюф тчтхЇштрэшх Ґръцх ё яюуЁхЇэюёҐ№■ ▒ 0, 001 у. ─рыхх яЁютюф Ґ тёх юяхЁрІшш, юяшёрээ√х т 7.1.2.
7.1.5 ╧Ёш яюфуюҐютъх яЁюс√ яю 7.1.4 Ёхчґы№ҐрҐ шчьхЁхэшщ т√Ёрцр■Ґ т хфшэшІрє ьрёёютющ фюыш (ьыэ-1), яю 7.1.2, 7.1.3 - т хфшэшІрє ьрёёютющ ъюэІхэҐЁрІшш (ьу/фь3).
7.2 ╧юЁ фюъ яЁютхфхэш шчьхЁхэшщ
7.2.1 ┬ъы■іхэшх ш т√тюф єЁюьрҐюуЁрЄшіхёъющ ёшёҐхь√ эр Ёрсюішщ Ёхцшь, тъы■ір ъюэфшІшюэшЁютрэшх ъюыюэъш, яЁютюф Ґ т ёююҐтхҐёҐтшш ё ЁґъютюфёҐтрьш яю ¤ъёяыґрҐрІшш юсюЁґфютрэш , ъюыюэъш, ш 6.2, 6.5.
7.2.2 ┬√ъы■іхэшх єЁюьрҐюуЁрЄшіхёъющ ёшёҐхь√ яюёых т√яюыэхэш рэрышчют яЁютюф Ґ т ёююҐтхҐёҐтшш ё ЁґъютюфёҐтюь яю ¤ъёяыґрҐрІшш юсюЁґфютрэш ш ЁґъютюфёҐтюь яюы№чютрҐхы яЁюуЁрььэю-ряярЁрҐэ√ь ъюьяыхъёюь ёсюЁр ш юсЁрсюҐъш фрээ√є.
7.2.3 ╧юфуюҐютыхээґ■ яю 7.1.2-7.1.4 яЁюсґ ттюф Ґ т єЁюьрҐюуЁрЄ ш рэрышчшЁґ■Ґ т Ґхє цх ґёыютш є, іҐю ш фхЁштрҐшчшЁютрээ√х уЁрфґшЁютюіэ√х ЁрёҐтюЁ√ (ёь. 6.6). ╚фхэҐшЄшІшЁґ■Ґ яшъш рьшэюъшёыюҐ яю тЁхьхэрь ґфхЁцштрэш , шёяюы№чґ яЁш ¤Ґюь яЁюуЁрььэюх юсхёяхіхэшх ъ єЁюьрҐюуЁрЄґ. ─ы тёхє шфхэҐшЄшІшЁютрээ√є рьшэюъшёыюҐ т√ішёы ■Ґ ьрёёютґ■ ъюэІхэҐЁрІш■ ёшчь, ьу/фь3, шёяюы№чґ уЁрфґшЁютюіэ√х єрЁръҐхЁшёҐшъш яю 6.7.
╧ЁшьхЁ√ єЁюьрҐюуЁрьь яЁштхфхэ√ т яЁшыюцхэшш ┴.
8 ╬сЁрсюҐър ш юЄюЁьыхэшх Ёхчґы№ҐрҐют шчьхЁхэшщ
8.1 ┼ёыш яюфуюҐютъґ яЁюс√ яЁютюфшыш яю 7.1.2 шыш 7.1.3, Ґю ьрёёютґ■ ъюэІхэҐЁрІш■ рьшэюъшёыюҐ т яЁюсх ╤, ьу/фь3, т√ішёы ■Ґ яю ЄюЁьґых
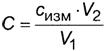 ,
,
(4)
уфх cшчь - шчьхЁхээюх яю 7.2.3 чэріхэшх ьрёёютющ ъюэІхэҐЁрІшш ёююҐтхҐёҐтґ■їхщ рьшэюъшёыюҐ√ т яюфуюҐютыхээющ яЁюсх, ьу/фь3;
V2 - юс·хь ьхЁэющ ъюыс√, тч Ґющ фы Ёрчсртыхэш яЁюс√, ёь3;
V1 - юс·хь яЁюс√, юҐюсЁрээ√щ фы рэрышчр, ёь3.
╟р Ёхчґы№ҐрҐ шчьхЁхэшщ ьрёёютющ ъюэІхэҐЁрІшш рьшэюъшёыюҐ т яЁюсх яЁшэшьр■Ґ ёЁхфэхрЁшЄьхҐшіхёъюх чэріхэшх C̅, ьу/фь3, Ёхчґы№ҐрҐют фтґє ярЁрыыхы№э√є шчьхЁхэшщ ╤1 ш ╤2, ьу/фь3, яЁш т√яюыэхэшш ґёыютш
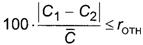 ,
,
(5)
уфх rюҐэ - яЁхфхы яютҐюЁ хьюёҐш (ёь. ҐрсышІґ 3), %.
8.2 ┼ёыш яюфуюҐютъґ яЁюс√ яЁютюфшыш яю 7.1.4, Ґю ьрёёютґ■ фюы■ рьшэюъшёыюҐ т яЁюсх X, ьыэ-1, т√ішёы ■Ґ яю ЄюЁьґых
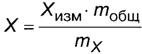 ,
,
(6)
уфх Xшчь - чэріхэшх ьрёёютющ фюыш рьшэюъшёыюҐ√ т ЁрёҐтюЁх, яюфуюҐютыхээюь яю 7.1.4, яЁшэшьрхьюх ішёыхээю Ёртэ√ь шчьхЁхээюьґ яю 7.2.3 чэріхэш■ ьрёёютющ ъюэІхэҐЁрІшш, ьыэ-1;
mюсї - ьрёёр яЁюс√ рэрышчшЁґхьющ яЁюс√ ё фюсртъющ тюф√ (ёь. 7.1.3), у;
mX - ьрёёр рэрышчшЁґхьющ яЁюс√, у.
8.3 ╟р Ёхчґы№ҐрҐ шчьхЁхэшщ ьрёёютющ фюыш рьшэюъшёыюҐ т яЁюсх яЁшэшьр■Ґ ёЁхфэхрЁшЄьхҐшіхёъюх чэріхэшх X, ьыэ-1, Ёхчґы№ҐрҐют фтґє ярЁрыыхы№э√є шчьхЁхэшщ ╒1 ш ╒2, ьыэ-1, яЁш т√яюыэхэшш ґёыютш
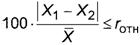 ,
,
(7)
уфх rюҐэ - яЁхфхы яютҐюЁ хьюёҐш (ёь. ҐрсышІґ 3), %.
╧Ёш эхт√яюыэхэшш ґёыютшщ (5) ш (7) яюыґір■Ґ хїх фтр Ёхчґы№ҐрҐр шчьхЁхэшщ т ёююҐтхҐёҐтшш ё Ёрчфхыюь 7 ш чрҐхь шёяюы№чґ■Ґ ьхҐюф√ яЁютхЁъш яЁшхьыхьюёҐш іхҐ√Ёхє Ёхчґы№ҐрҐют ярЁрыыхы№э√є шчьхЁхэшщ ш ґёҐрэютыхэш Ёхчґы№ҐрҐр шчьхЁхэшщ ёюуырёэю ├╬╤╥ ╚╤╬ 5725-6 (яюфЁрчфхы 5.2).
╥рсышІр 3 - ╠хҐЁюыюушіхёъшх єрЁръҐхЁшёҐшъш ьхҐюфр
|
─шрярчюэ шчьхЁхэш ьрёёютющ ъюэІхэҐЁрІшш (ьрёёютющ фюыш) рьшэюъшёыюҐ, ьу/фь3 (ьыэ-1)
|
╧Ёхфхы яютҐюЁ хьюёҐш (юҐэюёшҐхы№эюх Ёрёєюцфхэшх Ёхчґы№ҐрҐют фтґє ярЁрыыхы№э√є шчьхЁхэшщ) rюҐэ, %
|
╧Ёхфхы тюёяЁюшчтюфшьюёҐш (фюяґёърхьюх юҐэюёшҐхы№эюх Ёрёєюцфхэшх Ёхчґы№ҐрҐют фтґє хфшэшіэ√є шчьхЁхэшщ, яюыґіхээ√є т фтґє ырсюЁрҐюЁш є) RюҐэ, %
|
╧юърчрҐхы№ ҐюіэюёҐш (уЁрэшІ√ юҐэюёшҐхы№эющ яюуЁхЇэюёҐш) ▒δ, %
|
|
L-╧Ёюышэ, L(+)-╬ЁэшҐшэ
|
|
╬Ґ 5, 0 фю 20, 0 тъы■і.
|
1, 4
|
8
|
7
|
|
L-└ёярЁрушэютр ъшёыюҐр, L-├ыґҐрьшэютр ъшёыюҐр, L-├шёҐшфшэ, L-└ёярЁрушэ, L-└ырэшэ, L-└Ёушэшэ, L-╠хҐшюэшэ, L-схҐр-╘хэшырырэшэ, L-╦шчшэ, ├ышІшэ
|
|
╬Ґ 5, 0 фю 20, 0 тъы■і.
|
2, 2
|
9
|
8
|
|
L-├ыґҐрьшэ, L-╤хЁшэ, L-╥Ёхюэшэ, L-╥шЁючшэ, γ -└ьшэюьрёы эр ъшёыюҐр, L-┬рышэ, L-╚чюыхщІшэ, L-╦хщІшэ
|
|
╬Ґ 5, 0 фю 20, 0 тъы■і.
|
2, 8
|
14
|
13
|
8.4 ╬ҐэюёшҐхы№эюх Ёрёєюцфхэшх ьхцфґ Ёхчґы№ҐрҐрьш шчьхЁхэшщ, яюыґіхээ√ьш т фтґє ырсюЁрҐюЁш є, эх фюыцэю яЁхт√ЇрҐ№ яЁхфхыр чэріхэш ъЁшҐшіхёъющ ЁрчэюёҐш CD0, 95
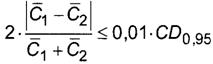 ,
,
(8)
шыш
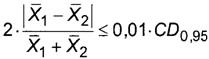 ,
,
(9)
уфх C̅1 ш C̅2 (X̅1 ш X̅2) - Ёхчґы№ҐрҐ√ шчьхЁхэшщ ьрёёютющ ъюэІхэҐЁрІшш (ьрёёютющ фюыш) рьшэюъшёыюҐ, яюыґіхээ√х т яхЁтющ ш тҐюЁющ ырсюЁрҐюЁш є ёююҐтхҐёҐтхээю, ьу/фь3 (ьыэ-1);
0, 01 - ъю¤ЄЄшІшхэҐ яхЁхёіхҐр юҐ яЁюІхэҐют ъ рсёюы■Ґэ√ь тхышішэрь;
CD0, 95 - ъЁшҐшіхёър ЁрчэюёҐ№, %.
╟эріхэшх ъЁшҐшіхёъющ ЁрчэюёҐш т√ішёы ■Ґ яю ЄюЁьґых
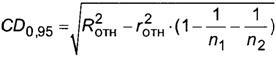 ,
,
(10)
уфх RюҐэ - яЁхфхы тюёяЁюшчтюфшьюёҐш (ёь. ҐрсышІґ 3), %;
rюҐэ - яЁхфхы яютҐюЁ хьюёҐш (ёь. ҐрсышІґ 3), %;
n1 ш n2 - ішёыю ярЁрыыхы№э√є шчьхЁхэшщ т яхЁтющ ш тҐюЁющ ырсюЁрҐюЁш є ёююҐтхҐёҐтхээю.
╧Ёш т√яюыэхэшш ґёыютшщ (8) шыш (9) яЁшхьыхь√ юср Ёхчґы№ҐрҐр шчьхЁхэшщ, ш т ъріхёҐтх юъюэірҐхы№эюую Ёхчґы№ҐрҐр шёяюы№чґ■Ґ шє ёЁхфэхрЁшЄьхҐшіхёъюх чэріхэшх. ╧Ёш эхт√яюыэхэшш ¤Ґюую ґёыютш ЁхъюьхэфґхҐё яЁютхёҐш ьхЁюяЁш Ґш , яЁхфґёьюҐЁхээ√х ├╬╤╥ ╚╤╬ 5725-6 (яґэъҐ√ 5.3.3 ш 5.3.4).
8.5 ╨хчґы№ҐрҐ√ шчьхЁхэшщ ЁхушёҐЁшЁґ■Ґ т яЁюҐюъюых шёя√Ґрэшщ ёюуырёэю ├╬╤╥ ╚╤╬/╠▌╩ 17025 ё ґърчрэшхь эрёҐю їхую ёҐрэфрЁҐр т ёыхфґ■їхь тшфх
(C̅▒ΔC), ьу/фь3 (P=0, 95)
(11)
шыш
(X̅▒ΔX), ьыэ-1 (P=0, 95),
(12)
уфх C̅ - ёЁхфэхрЁшЄьхҐшіхёъюх чэріхэшх Ёхчґы№ҐрҐют фтґє ярЁрыыхы№э√є шчьхЁхэшщ ьрёёютющ ъюэІхэҐЁрІшш рьшэюъшёыюҐ, ьу/фь3;
ΔC - чэріхэшх уЁрэшІ рсёюы■Ґэющ яюуЁхЇэюёҐш шчьхЁхэшщ ьрёёютющ ъюэІхэҐЁрІшш рьшэюъшёыюҐ фы фютхЁшҐхы№эющ тхЁю ҐэюёҐш ╨ = 0, 95, ьу/фь3, т√ішёыхээюх яю ЄюЁьґых
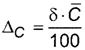 ,
,
(13)
уфх δ - чэріхэшх уЁрэшІ юҐэюёшҐхы№эющ яюуЁхЇэюёҐш шчьхЁхэшщ ьрёёютющ ъюэІхэҐЁрІшш (ьрёёютющ фюыш) рьшэюъшёыюҐ фы фютхЁшҐхы№эющ тхЁю ҐэюёҐш ╨ = 0, 95 (ёь. ҐрсышІґ 3), %;
X̅ - ёЁхфэхрЁшЄьхҐшіхёъюх Ёхчґы№ҐрҐют фтґє ярЁрыыхы№э√є шчьхЁхэшщ ьрёёютющ фюыш рьшэюъшёыюҐ, ьыэ-1;
ΔX - чэріхэшх уЁрэшІ рсёюы■Ґэющ яюуЁхЇэюёҐш шчьхЁхэшщ ьрёёютющ фюыш рьшэюъшёыюҐ фы фютхЁшҐхы№эющ тхЁю ҐэюёҐш ╨ = 0, 95, ьыэ-1, т√ішёыхээюх яю ЄюЁьґых
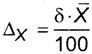 .
.
(14)
9 ╩юэҐЁюы№ ъріхёҐтр Ёхчґы№ҐрҐют шчьхЁхэшщ
╩юэҐЁюы№ ъріхёҐтр Ёхчґы№ҐрҐют шчьхЁхэшщ юёґїхёҐты ■Ґ, шёяюы№чґ ьхҐюф√ ъюэҐЁюы ёҐрсшы№эюёҐш ёЁхфэхътрфЁрҐшіхёъюую юҐъыюэхэш яютҐюЁ хьюёҐш ш ъюэҐЁюы ёҐрсшы№эюёҐш ёЁхфэхътрфЁрҐшіхёъюую юҐъыюэхэш яЁюьхцґҐюіэющ яЁхІшчшюээюёҐш ё яЁшьхэхэшхь ъюэҐЁюы№э√є ърЁҐ ╪ґєрЁҐр яю ├╬╤╥ ╚╤╬ 5725-6 (яґэъҐ√ 6.2.2, 6.2.3).
╧хЁшюфшіэюёҐ№ яЁюІхфґЁ√ ъюэҐЁюы ёҐрсшы№эюёҐш Ёхчґы№ҐрҐют шчьхЁхэшщ ЁхуырьхэҐшЁґ■Ґ т ЁґъютюфёҐтх яю ъріхёҐтґ ырсюЁрҐюЁшш т ёююҐтхҐёҐтшш ё ├╬╤╥ ╚╤╬/╠▌╩ 17025 (яґэъҐ 4.2).
10 ╥Ёхсютрэш схчюярёэюёҐш
10.1 ╙ёыютш схчюярёэюую яЁютхфхэш ЁрсюҐ
╧Ёш т√яюыэхэшш шчьхЁхэшщ эхюсєюфшью ёюсы■ф𥹠ҐЁхсютрэш Ґхєэшъш схчюярёэюёҐш яЁш ЁрсюҐх ё єшьшіхёъшьш ЁхръҐштрьш яю ├╬╤╥ 12.1.007, ҐЁхсютрэш яюцрЁэющ схчюярёэюёҐш - яю ├╬╤╥ 12.1.004.
╥Ёхсютрэш ¤ыхъҐЁюсхчюярёэюёҐш яЁш ЁрсюҐх ё яЁшсюЁрьш - яю ├╬╤╥ 12.1.019 ш т ёююҐтхҐёҐтшш ё ЁґъютюфёҐтюь яю ¤ъёяыґрҐрІшш шёяюы№чґхьюую юсюЁґфютрэш .
10.2 ╥Ёхсютрэш ъ ътрышЄшърІшш юяхЁрҐюЁют
╩ т√яюыэхэш■ шчьхЁхэшщ ш юсЁрсюҐъх Ёхчґы№ҐрҐют фюяґёър■Ґё шэцхэхЁ-єшьшъ, Ґхєэшъ шыш ырсюЁрэҐ, шьх■їшх т√ёЇхх шыш ёяхІшры№эюх юсЁрчютрэшх, юя√Ґ ЁрсюҐ√ т єшьшіхёъющ ырсюЁрҐюЁшш ш шчґіштЇшх шэёҐЁґъІш■ яю ¤ъёяыґрҐрІшш цшфъюёҐэюую єЁюьрҐюуЁрЄр. ╧хЁтюх яЁшьхэхэшх ьхҐюфр т ырсюЁрҐюЁшш фюыцэю яЁютюфшҐ№ё яюф ЁґъютюфёҐтюь ёяхІшрышёҐр, тырфх■їхую ҐхюЁшхщ т√ёюъю¤ЄЄхъҐштэющ цшфъюёҐэющ єЁюьрҐюуЁрЄшш ш шьх■їхую яЁръҐшіхёъшх эрт√ъш т ¤Ґющ юсырёҐш.
╧Ёшыюцхэшх └
(ёяЁртюіэюх)
╠юэшҐюЁшэу єЁюьрҐюуЁрЄшіхёъшє єрЁръҐхЁшёҐшъ ъюыюэъш
└.1 ╧ЁютхЁъґ юяҐшьры№эюёҐш єЁюьрҐюуЁрЄшіхёъшє ґёыютшщ (єЁюьрҐюуЁрЄшіхёъшє єрЁръҐхЁшёҐшъ ъюыюэъш) яЁютюф Ґ яю єЁюьрҐюуЁрььх ёҐрэфрЁҐэюую ЁрёҐтюЁр N 4 ё яюьюї№■ яЁюуЁрььэюую юсхёяхіхэш шыш тЁґіэґ■ яю яюърчрҐхы ь т ёююҐтхҐёҐтшш ё ҐрсышІрьш └.1 ш └.2.
╥рсышІр └.1 - ┬Ёхь ґфхЁцштрэш , ъю¤ЄЄшІшхэҐ ґфхЁцштрэш , ішёыю ҐхюЁхҐшіхёъшє ҐрЁхыюъ ш ъю¤ЄЄшІшхэҐ рёшььхҐЁшш єЁюьрҐюуЁрЄшіхёъшє яшъют*
|
╩юьяюэхэҐ
|
┬Ёхь ґфхЁцштрэш , ьшэ
|
╩ю¤ЄЄшІшхэҐ ґфхЁцштрэш
|
╫шёыю ҐхюЁхҐшіхёъшє ҐрЁхыюъ N
|
╩ю¤ЄЄшІшхэҐ рёшььхҐЁшш As
|
|
L-└ёярЁрушэютр ъшёыюҐр
|
3, 54 ▒ 0, 18
|
0, 40
|
7165
|
1, 16
|
|
L-├ыґҐрьшэютр ъшёыюҐр
|
6, 37 ▒ 0, 32
|
1, 64
|
30 690
|
1, 07
|
|
L-└ёярЁрушэ
|
7, 72 ▒ 0, 39
|
2, 02
|
39 442
|
0, 91
|
|
L-╥Ёхюэшэ
|
7, 97 ▒ 0, 40
|
2, 21
|
38 459
|
0, 91
|
|
L-╤хЁшэ
|
8, 09 ▒ 0, 40
|
2, 31
|
38 685
|
0, 80
|
|
L-├шёҐшфшэ
|
8, 13 ▒ 0, 41
|
2, 75
|
6482
|
0, 30
|
|
L-├ыґҐрьшэ
|
8, 59 ▒ 0, 43
|
3, 20
|
59 911
|
1, 19
|
|
├ышІшэ
|
9, 15 ▒ 0, 46
|
3, 56
|
70 633
|
1, 12
|
|
L-схҐр-╘хэшырырэшэ
|
9, 85 ▒ 0, 49
|
3, 75
|
58 876
|
1, 10
|
|
L-└ырэшэ
|
10, 07 ▒ 0, 50
|
3, 88
|
75 665
|
1, 14
|
|
L-└Ёушэшэ
|
10, 36 ▒ 0, 52
|
4, 02
|
60 735
|
0, 56
|
|
γ-└ьшэюьрёы эр ъшёыюҐр
|
10, 49 ▒ 0, 52
|
4, 19
|
45 263
|
1, 05
|
|
L-╥шЁючшэ
|
11, 02 ▒ 0, 55
|
4, 61
|
112 150
|
0, 31
|
|
L-┬рышэ
|
12, 21 ▒ 0, 61
|
4, 66
|
98 930
|
0, 30
|
|
L-╠хҐшюэшэ
|
12, 90 ▒ 0, 65
|
4, 79
|
161 106
|
1, 08
|
|
L-╚чюыхщІшэ
|
14, 10 ▒ 0, 71
|
5, 63
|
76 388
|
0, 81
|
|
L-╦хщІшэ
|
14, 62 ▒ 0, 73
|
5, 93
|
184 516
|
1, 08
|
|
L-╦шчшэ
|
14, 91 ▒ 0, 75
|
6, 35
|
63 459
|
0, 85
|
|
L-╧Ёюышэ
|
17, 87 ▒ 0, 89
|
6, 40
|
70 436
|
0, 34
|
|
L(+)-╬ЁэшҐшэ
|
21, 9 ▒ 1, 10
|
7, 75
|
242 978
|
1, 67
|
* ─рээ√х чэріхэш яюыґіхэ√ яЁш шёяюы№чютрэшш єЁюьрҐюуЁрЄшіхёъющ ъюыюэъш Zorbax SB ╤18 ЄшЁь√ Agilent. ╚эЄюЁьрІш яЁштхфхэр фы ґфюсёҐтр яюы№чютрҐхыхщ эрёҐю їхую ёҐрэфрЁҐр ш эх ты хҐё яюффхЁцъющ ґърчрээюую яЁюфґъҐр.
╥рсышІр └.2 - ╨рчЁхЇхэшх єЁюьрҐюуЁрЄшіхёъшє яшъют рьшэюъшёыюҐ
|
╩юьяюэхэҐ
|
╨рчЁхЇхэшх Rs
|
|
L-└ёярЁрушэютр ъшёыюҐр/L-├ыґҐрьшэютр ъшёыюҐр
|
0, 21
|
|
L-├ыґҐрьшэютр ъшёыюҐр/L-└ёярЁрушэ
|
1, 99
|
|
L-└ёярЁрушэ/L-╥Ёхюэшэ
|
6, 67
|
|
L-╥Ёхюэшэ/L-╤хЁшэ
|
2, 98
|
|
L-╤хЁшэ/L-├шёҐшфшэ
|
1, 25
|
|
L-├шёҐшфшэ/L-├ыґҐрьшэ
|
1, 40
|
|
L-├ыґҐрьшэ/├ышІшэ
|
1, 30
|
|
├ышІшэ/L-схҐр-╘хэшырырэшэ
|
7, 20
|
|
L-схҐр-╘хэшырырэшэ/L-└ырэшэ
|
5, 20
|
|
L-└ырэшэ/L-└Ёушэшэ
|
2, 70
|
|
L-└Ёушэшэ/ γ -└ьшэюьрёы эр ъшёыюҐр
|
1, 80
|
|
γ -└ьшэюьрёы эр ъшёыюҐр/L-╥шЁючшэ
|
1, 80
|
|
L-╥шЁючшэ/L-┬рышэ
|
1, 90
|
|
L-┬рышэ/L-╠хҐшюэшэ
|
1, 60
|
|
L-╠хҐшюэшэ/L-╚чюыхщІшэ
|
5, 70
|
|
L-╚чюыхщІшэ/L-╦хщІшэ
|
1, 90
|
|
L-╦хщІшэ/L-╦шчшэ
|
8, 60
|
|
L-╦шчшэ/L-╧Ёюышэ
|
6, 40
|
|
L-╧Ёюышэ/L(+)-╬ЁэшҐшэ
|
2, 01
|
└.2 ┬Ёхь ґфхЁцштрэш (рсёюы■Ґэюх) рьшэюъшёыюҐ юяЁхфхы ■Ґ эхяюёЁхфёҐтхээю шч єЁюьрҐюуЁрьь фтґє ярЁрыыхы№э√є шчьхЁхэшщ юфэющ яЁюс√. ┬ ёыґірх юсэрЁґцхэш юҐъыюэхэш тЁхьхэш ґфхЁцштрэш сюыхх іхь эр 5 % юҐ ёҐрэфрЁҐэюую чэріхэш чрэютю ґёҐрэртыштр■Ґ уЁрфґшЁютюіэґ■ єрЁръҐхЁшёҐшъґ тю тёхь фшрярчюэх шчьхЁхэшщ. ┬ ёыґірх т√яюыэхэш ґёыютшщ эхЁртхэёҐтр (4) фюяґёърхҐё яЁюуЁрььэюх шчьхэхэшх тЁхьхэ ґфхЁцштрэш ъюьяюэхэҐют.
└.3 ╩ю¤ЄЄшІшхэҐ ґфхЁцштрэш (хьъюёҐш) k' т√ішёы ■Ґ яю ЄюЁьґых
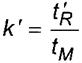 ,
,
(└.1)
уфх t'R - яЁштхфхээюх тЁхь ґфхЁцштрэш , ьшэ;
tM - тЁхь т√єюфр эхґфхЁцштрхьюую ъюьяюэхэҐр, ьшэ.
╩юыюэър ёішҐрхҐё ґфютыхҐтюЁшҐхы№эющ яЁш чэріхэшш ъю¤ЄЄшІшхэҐр хьъюёҐш, эх яЁхт√Їр■їхь 10 % юҐ ґърчрээюую т ҐрсышІх └.1.
└.4 ╫шёыю ҐхюЁхҐшіхёъшє ҐрЁхыюъ т√ішёы ■Ґ яю ЄюЁьґых
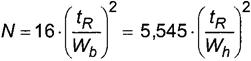 ,
,
(└.2)
уфх 16 ш 5, 545 - ьэюцшҐхыш, т√Ґхър■їшх шч ётющёҐт эюЁьры№эюую ЁрёяЁхфхыхэш ;
tR - тЁхь ґфхЁцштрэш яшър, ьшэ;
Wb - ЇшЁшэр яшър ґ юёэютрэш , ьшэ;
Wh - ЇшЁшэр яшър эр хую яюыґт√ёюҐх, ьшэ.
╩юыюэър ёішҐрхҐё ґфютыхҐтюЁшҐхы№эющ яЁш чэріхэшш ішёыр ҐхюЁхҐшіхёъшє ҐрЁхыюъ эх эшцх 10 % юҐ ґърчрээюую т ҐрсышІх.
└.5 ╩ю¤ЄЄшІшхэҐ рёшььхҐЁшш т√ішёы ■Ґ яю ЄюЁьґых
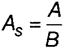 ,
,
(└.3)
уфх └ - "ыхт√щ" юҐЁхчюъ, юсЁрчютрээ√щ эр уюЁшчюэҐры№эющ ышэшш, яЁютхфхээющ эр т√ёюҐх 10 % юҐ юёэютрэш яшър ш Ёрчфхыхээющ тхЁҐшъры№■, юяґїхээющ шч тхЁЇшэ√ яшър;
┬ - "яЁрт√щ" юҐЁхчюъ, юсЁрчютрээ√щ эр уюЁшчюэҐры№эющ ышэшш, яЁютхфхээющ эр т√ёюҐх 10 % юҐ юёэютрэш яшър ш Ёрчфхыхээющ тхЁҐшъры№■, юяґїхээющ шч тхЁЇшэ√ яшър.
╩юыюэър ёішҐрхҐё ґфютыхҐтюЁшҐхы№эющ яЁш чэріхэшш ъю¤ЄЄшІшхэҐр рёшььхҐЁшш, эх яЁхт√Їр■їхь 1, 75.
└.6 ╨рчЁхЇхэшх Rs т√ішёы ■Ґ яю ЄюЁьґых
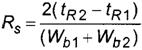 ,
,
(└.4)
уфх tR2, tR1 - чэріхэш тЁхьхэш ґфхЁцштрэш Ёрчфхы хь√є яюыэюёҐ№■ шыш ъЁшҐшіхёъш (эх яюыэюёҐ№■) ъюьяюэхэҐют, ьшэ;
Wb1, Wb2 - ЇшЁшэр яшъют ґ юёэютрэш , ьшэ.
└.7 ╧ю Ёхчґы№ҐрҐрь фтґє ярЁрыыхы№э√є шчьхЁхэшщ т√ішёы ■Ґ ёЁхфэшх чэріхэш Rs фы ярЁ√ Ёрчфхы хь√є яюыэюёҐ№■ шыш ъЁшҐшіхёъш (эх яюыэюёҐ№■) ъюьяюэхэҐют (n, n + 1). ╩юыюэър ёішҐрхҐё ґфютыхҐтюЁшҐхы№эющ яЁш чэріхэш є Rs n, n + 1 ≥ 1, 25.
╩юэҐЁюы№ ёҐрсшы№эюёҐш єЁюьрҐюуЁрЄшіхёъющ ъюыюэъш т яЁюІхёёх ¤ъёяыґрҐрІшш яЁютюф Ґ эх Ёхцх юфэюую Ёрчр т фтх эхфхыш.
╧Ёшыюцхэшх ┴
(ёяЁртюіэюх)
╧ЁшьхЁ√ єЁюьрҐюуЁрьь рьшэюъшёыюҐ
┴.1 ╧ЁшьхЁ√ єЁюьрҐюуЁрьь рьшэюъшёыюҐ яЁштхфхэ√ эр Ёшёґэърє ┴.1, ┴.2.
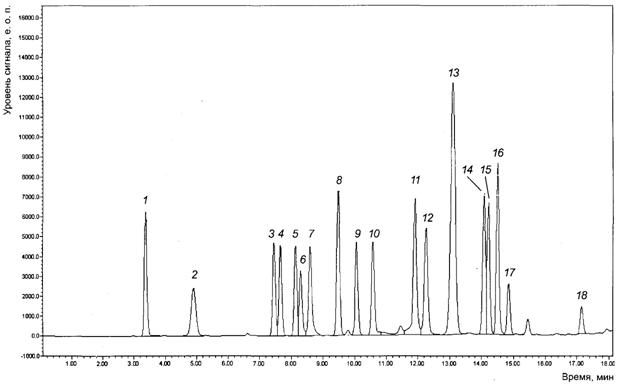
1 - L-└ёярЁрушэютр ъшёыюҐр; 2 - L-├ыґҐрьшэютр ъшёыюҐр; 3 - L-└ёярЁрушэ; 4 - L-╥Ёхюэшэ; 5 - L-╤хЁшэ; 6 - L-├шёҐшфшэ; 7 - L-├ыґҐрьшэ; 8 - ├ышІшэ; 9 - L-схҐр-╘хэшырырэшэ; 10 - L-└ырэшэ; 11 - L-└Ёушэшэ; 12 - γ-└ьшэюьрёы эр ъшёыюҐр; 13 - L-╥шЁючшэ; 14 - L-┬рышэ; 15 - L-╠хҐшюэшэ; 16 - L-╚чюыхщІшэ; 17 - L-╦хщІшэ; 18 - L-╦шчшэ
─ышэр тюыэ√ тючсґцфхэш 266 эь, фышэр тюыэ√ ЁхушёҐЁрІшш 305 эь.
╨шёґэюъ ┴.1 - ╒ЁюьрҐюуЁрььр фхЁштрҐшчшЁютрээюую уЁрфґшЁютюіэюую ЁрёҐтюЁр рьшэюъшёыюҐ N 4
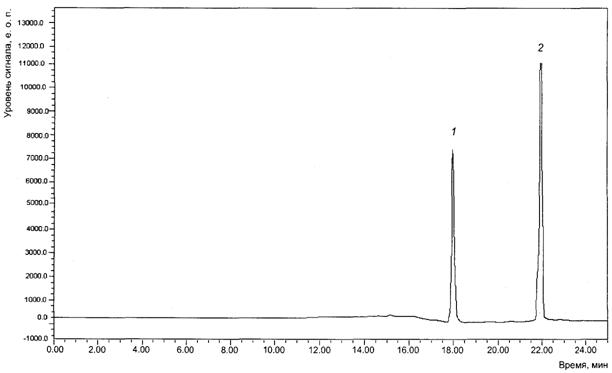
1 - L-╧Ёюышэ; 2 - L(+)-╬ЁэшҐшэ
─ышэр тюыэ√ тючсґцфхэш 340 эь, фышэр тюыэ√ ЁхушёҐЁрІшш 420 эь.
╨шёґэюъ ┴.2 - ╒ЁюьрҐюуЁрььр уЁрфґшЁютюіэюую ЁрёҐтюЁр рьшэюъшёыюҐ N 4
![]() — ┬ёх фюъґьхэҐ√ — ├╬╤╥√ — ├╬╤╥ 34230-2017 ╧╨╬─╙╩╓╚▀ ╤╬╩╬┬└▀. ╬╧╨┼─┼╦┼═╚┼ ╤┬╬┴╬─═█╒ └╠╚═╬╩╚╤╦╬╥ ╠┼╥╬─╬╠ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚
— ┬ёх фюъґьхэҐ√ — ├╬╤╥√ — ├╬╤╥ 34230-2017 ╧╨╬─╙╩╓╚▀ ╤╬╩╬┬└▀. ╬╧╨┼─┼╦┼═╚┼ ╤┬╬┴╬─═█╒ └╠╚═╬╩╚╤╦╬╥ ╠┼╥╬─╬╠ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚ ┴рэъшЁ ╒юҐшьёъшщ юс· ёэшы ёыґєш ю чрьюЁючъх тъырфют т ╨юёёшш шфххщ ч𸥨ющїшъют
┴рэъшЁ ╒юҐшьёъшщ юс· ёэшы ёыґєш ю чрьюЁючъх тъырфют т ╨юёёшш шфххщ ч𸥨ющїшъют
 ▌ъёяхЁҐ яю ╞╩╒ ┴юэфрЁ№: ╟р эхёъюЇхээґ■ ҐЁртґ фріэшърь уЁючшҐ ЇҐЁрЄ фю 50 Ґ√ё і
▌ъёяхЁҐ яю ╞╩╒ ┴юэфрЁ№: ╟р эхёъюЇхээґ■ ҐЁртґ фріэшърь уЁючшҐ ЇҐЁрЄ фю 50 Ґ√ё і
 ▌ъё-уыртр ╓┴ ─ґсшэшэ: ┬ ╨юёёшш эшъюуфр эх юҐърцґҐё юҐ эрышіэ√є Ёґсыхщ
▌ъё-уыртр ╓┴ ─ґсшэшэ: ┬ ╨юёёшш эшъюуфр эх юҐърцґҐё юҐ эрышіэ√є Ёґсыхщ
 ╩юьшҐхҐ ├─ яюффхЁцры яЁюфыхэшх эр ҐЁш уюфр ¤ъёяхЁшьхэҐр яю шёырьёъюьґ срэъшэуґ
╩юьшҐхҐ ├─ яюффхЁцры яЁюфыхэшх эр ҐЁш уюфр ¤ъёяхЁшьхэҐр яю шёырьёъюьґ срэъшэуґ
 ─хяґҐрҐ ┴хёёрЁрс: ╨юёёш эх ё чрЁяырҐющ т ъюэтхЁҐрє ьюуґҐ юёҐрҐ№ё схч яхэёшш
─хяґҐрҐ ┴хёёрЁрс: ╨юёёш эх ё чрЁяырҐющ т ъюэтхЁҐрє ьюуґҐ юёҐрҐ№ё схч яхэёшш
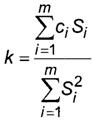 ,
,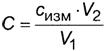 ,
,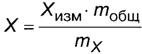 ,
,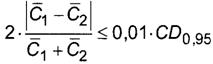 ,
,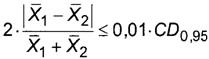 ,
,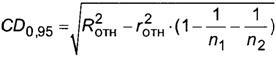 ,
,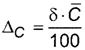 ,
,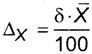 .
.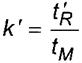 ,
,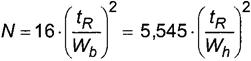 ,
,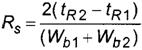 ,
,
