![]() — ┬ёх фюъґьхэҐ√ — ├╬╤╥√ — ├╬╤╥ 13685-84 (13.12.2011) ╤╬╦▄ ╧╬┬└╨┼══└▀. ╠┼╥╬─█ ╚╤╧█╥└═╚╔
— ┬ёх фюъґьхэҐ√ — ├╬╤╥√ — ├╬╤╥ 13685-84 (13.12.2011) ╤╬╦▄ ╧╬┬└╨┼══└▀. ╠┼╥╬─█ ╚╤╧█╥└═╚╔
├╬╤╥ 13685-84 (13.12.2011) ╤╬╦▄ ╧╬┬└╨┼══└▀. ╠┼╥╬─█ ╚╤╧█╥└═╚╔
╤ шчьхэхэш ьш:
(29 фхърсЁ 2005 у., 1 ш■ы , 13 фхърсЁ 2011 у.)
Common salt. Test methods
─рҐр ттхфхэш 1 этрЁ 1985 у.
┬чрьхэ ├╬╤╥ 13685-68
═рёҐю їшщ ёҐрэфрЁҐ ЁрёяЁюёҐЁрэ хҐё эр яютрЁхээґ■ ёюы№, яЁхфэрчэріхээґ■ фы яшїхт√є Іхыхщ, эр ъюЁьютґ■ ёюы№, єыюЁшёҐ√щ эрҐЁшщ фы яЁюь√Їыхээюую яюҐЁхсыхэш ш Ёрёёюы√ єыюЁшфр эрҐЁш ш ґёҐрэртыштрхҐ ьхҐюф√ юҐсюЁр яЁюс фы шёя√Ґрэшщ ш ьхҐюф√ шёя√Ґрэшщ.
(╚чьхэхээр ЁхфръІш , ╚чь. N 2).
═х яЁшьхэ хҐё ё 1 этрЁ 2007 у.
═х яЁшьхэ хҐё ё 1 этрЁ 2007 у.
═х яЁшьхэ хҐё ё 1 этрЁ 2013 у.
═х яЁшьхэ хҐё ё 1 ш■ы 2012 у.
═х яЁшьхэ хҐё ё 1 ш■ы 2012 у.
═х яЁшьхэ хҐё ё 1 ш■ы 2012 у.
═х яЁшьхэ хҐё ё 1 ш■ы 2012 у.
═х яЁшьхэ хҐё ё 1 ш■ы 2012 у.
═х яЁшьхэ хҐё ё 1 ш■ы 2012 у.
╠хҐюф юёэютрэ эр тюёёҐрэютыхэшш ҐЁхєтрыхэҐэюую цхыхчр т фтґєтрыхэҐэюх яЁш яюьюїш ёюы эюъшёыюую ушфЁюъёшырьшэр, юсЁрчютрэшш ъюьяыхъёр цхыхчр ё ю-ЄхэрэҐЁюышэюь ш ЄюҐюьхҐЁшіхёъюь шчьхЁхэшш юъЁрЇхээюую ъюьяыхъёр яЁш фышэх тюыэ√ юъюыю 510 эь.
╠хҐюф яЁшьхэ хҐё яЁш тючэшъэютхэшш Ёрчэюуырёшщ т юІхэъх ъріхёҐтр.
2.9.1. └яярЁрҐґЁр, ьрҐхЁшры√ ш ЁхръҐшт√
╧Ёш яЁютхфхэшш шёя√Ґрэш яЁшьхэ ■Ґ ЁхръҐшт√ ътрышЄшърІшш і.ф.р.
╤яхъҐЁюЄюҐюьхҐЁ шыш ЄюҐюъюыюЁшьхҐЁ ё ъ■тхҐрьш ё Ґюыїшэющ яюуыюїр■їхую ётхҐ ёыю 4 ш 5 ёь шыш фЁґуюую Ґшяр, юсхёяхіштр■їхую ҐюіэюёҐ№ юяЁхфхыхэш 0, 0001%.
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 2-ую ъырёёр ҐюіэюёҐш ё эршсюы№Їшь яЁхфхыюь тчтхЇштрэш 200 у ш фюяґёърхьющ яюуЁхЇэюёҐ№■ эх сюыхх 0, 2 ьу.
╤тхҐюЄшы№ҐЁ чхыхэ√щ - яЁш фышэх тюыэ√ 500-540 эь.
╩■тхҐ√ ё Ґюыїшэющ яюуыюїр■їхую ётхҐ ёыю 50 ьь.
╧ышҐър ¤ыхъҐЁшіхёър яю ├╬╤╥ 14919 шыш фЁґующ эруЁхтрҐхы№э√щ яЁшсюЁ, юсхёяхіштр■їшщ эруЁхт фю 100░╤.
┴■ЁхҐъш тьхёҐшьюёҐ№■ 5, 10 ш 25 ёь3.
╩юыс√ ьхЁэ√х яю ├╬╤╥ 1770 тьхёҐшьюёҐ№■ 100, 250, 500, 1000 ёь3.
╩юыс√ ъюэшіхёъшх яю ├╬╤╥ 25336 тьхёҐшьюёҐ№■ 150 ёь3.
╧шяхҐъш тьхёҐшьюёҐ№■ 1, 5 ш 10 ёь3.
├шфЁюъёшырьшэ ёюы эюъшёы√щ яю ├╬╤╥ 5456, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ тхїхёҐтр 10%.
═рҐЁшщ ышьюээюъшёы√щ ҐЁхєчрьхїхээ√щ яю ├╬╤╥ 22280, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ ышьюээюъшёыюую эрҐЁш 25%.
═рҐЁш ушфЁююъшё№ яю ├╬╤╥ 4328, 2 ╠ ЁрёҐтюЁ.
ю-╘хэрэҐЁюышэ, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ тхїхёҐтр 0, 25%.
╩шёыюҐр ёхЁэр яю ├╬╤╥ 4204 яыюҐэюёҐ№■ 1840 ъу/ь3.
╩шёыюҐр ёюы эр яю ├╬╤╥ 3118 яыюҐэюёҐ№■ 1190 ъу/ь3.
╞хыхчю, ЁрёҐтюЁ 1, ёюфхЁцрїшщ 0, 2 ьу Fe т 1 ёь3 ЁрёҐтюЁр, уюҐют Ґ яю ├╬╤╥ 4212 ёыхфґ■їшь юсЁрчюь: 1, 4043 у цхыхчюрььюэшхтюую ЇхёҐштюфэюую ёґы№ЄрҐр (NH4)2ХFe(SO4)2Х6H2O яю ├╬╤╥ 4208 ЁрёҐтюЁ ■Ґ т 200 ёь3 тюф√ т ьхЁэющ ъюысх тьхёҐшьюёҐ№■ 1000 ёь3, фюсрты ■Ґ 20 ёь3 ёхЁэющ ъшёыюҐ√ яыюҐэюёҐ№■ 1840 ъу/ь3 яю ├╬╤╥ 4204, юєырцфр■Ґ фю ъюьэрҐэющ ҐхьяхЁрҐґЁ√, Ёрчсрты ■Ґ тюфющ фю ьхҐъш ш яхЁхьхЇштр■Ґ.
╞хыхчю, ЁрёҐтюЁ 2, ёюфхЁцрїшщ 0, 01 ьу Fe т 1 ёь3 ЁрёҐтюЁр, уюҐют Ґ ёыхфґ■їшь юсЁрчюь: 25 ёь3 ЁрёҐтюЁр 1 Ёрчсрты ■Ґ тюфющ т ьхЁэющ ъюысх тьхёҐшьюёҐ№■ 500 ёь3 фю ьхҐъш ш яхЁхьхЇштр■Ґ. ╨рёҐтюЁ ётхцхяЁшуюҐютыхээ√щ.
┬юфр фшёҐшыышЁютрээр яю ├╬╤╥ 6709.
2.9.2. ╧Ёютхфхэшх шёя√Ґрэш
┬ ьхЁэ√х ъюыс√ тьхёҐшьюёҐ№■ 100 ёь3 юҐсшЁр■Ґ ЁрёҐтюЁ 2 т юс·хьрє, ґърчрээ√є т Ґрсы. 1.
╥рсышІр 1
|
╩юышіхёҐтю ЁрёҐтюЁр 2, ёь3 |
╤ююҐтхҐёҐтґ■їшх ьрёё√ цхыхчр, ьу |
|
0* |
- |
|
2, 5 |
0, 025 |
|
5, 0 |
0, 050 |
|
10, 0 |
0, 100 |
|
15, 0 |
0, 150 |
_____________________________
* ╩юэҐЁюы№э√щ ЁрёҐтюЁ.
╨рёҐтюЁ√ т ъюысрє Ёрчсрты ■Ґ тюфющ фю юс·хьют 50 ёь3, фюсрты ■Ґ 0, 5 ёь3 ёюы эющ ъшёыюҐ√, 2 ёь3 ЁрёҐтюЁр ёюы эюъшёыюую ушфЁюъёшырьшэр ш ЁрёҐтюЁр ушфЁююъшёш эрҐЁш фю яюыґіхэш Ё═ 2-4 (яЁюср шэфшърҐюЁэющ сґьрцъющ). ─юсрты ■Ґ 5 ёь3 ЁрёҐтюЁр ю-ЄхэрэҐЁюышэр, фюыштр■Ґ ЁрёҐтюЁ фю ьхҐъш ш яхЁхьхЇштр■Ґ. ╫хЁхч 5 ьшэ шчьхЁ ■Ґ юяҐшіхёъґ■ яыюҐэюёҐ№ ЁрёҐтюЁют яЁш фышэх тюыэ√ 510 эь т яЁшёґҐёҐтшш ъюэҐЁюы№эюую ЁрёҐтюЁр т ъріхёҐтх ЁрёҐтюЁр ёЁртэхэш . ═р юёэютрэшш яюыґіхээ√є фрээ√є ёҐЁю Ґ ърышсЁютюіэґ■ ъЁштґ■, эрэюё Ґ эр юё№ юЁфшэрҐ чэріхэш юяҐшіхёъющ яыюҐэюёҐш, р эр юё№ рсёІшёё - ёююҐтхҐёҐтґ■їшх шь ъюышіхёҐтр цхыхчр т ьшыышуЁрььрє.
┬ ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3 юҐсшЁр■Ґ яшяхҐъющ Ґръющ юс·хь ЁрёҐтюЁр └ яю я. 2.3.3, іҐюс√ ёюфхЁцрэшх цхыхчр т эхь ёюёҐрты ыю юҐ 0, 025 фю 0, 150 ьу. ╨рёҐтюЁ Ёрчсрты ■Ґ тюфющ фю юс·хьр 50 ёь3. ═р юёэютрэшш шчьхЁхээющ юяҐшіхёъющ яыюҐэюёҐш яю ърышсЁютюіэющ ъЁштющ яЁютюф Ґ юҐёіхҐ ёюфхЁцрэш цхыхчр т шёя√Ґґхьюь ЁрёҐтюЁх т ьшыышуЁрььрє. ╬фэютЁхьхээю Ґръшь цх ёяюёюсюь, шёяюы№чґ Ґюы№ъю ЁхръҐшт√, яЁютюф Ґ шчьхЁхэшх ъюэҐЁюы№эющ яЁюс√ (ЁрёҐтюЁр ёЁртэхэш ).
2.9.3. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╠рёёютґ■ фюы■ цхыхчр (X10) т яЁюІхэҐрє, т яхЁхёіхҐх эр ёґєюх тхїхёҐтю, т√ішёы ■Ґ яю ЄюЁьґых
 ,
,
уфх m - ьрёёр эртхёъш ёюыш, у;
m1 - ьрёёютр фюы цхыхчр, юяЁхфхыхээр яю ърышсЁютюіэющ ъЁштющ, ьу;
V - юс·хь рышътюҐэющ ірёҐш рэрышчшЁґхьюую ЁрёҐтюЁр, ёь3;
X1 - ьрёёютр фюы тыруш, юяЁхфхыхээр яю я. 2.2.
╠рёёютґ■ фюы■ юъёшфр цхыхчр (X11) т яЁюІхэҐрє т√ішёы ■Ґ яю ЄюЁьґых
X11=1, 4297ХX10,
уфх 1, 4297 - ъю¤ЄЄшІшхэҐ яхЁхёіхҐр эр Fe2O3.
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ рэрышчр яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх фтґє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 0, 0005% яЁш ьрёёютющ фюых юъёшфр цхыхчр фю 0, 005%.
(╚чьхэхээр ЁхфръІш , ╚чь. N 1, 2).
╠хҐюф юёэютрэ эр ёяюёюсэюёҐш ҐЁшыюэр ┴ юсЁрчют√т𥹠ё ҐЁхєтрыхэҐэ√ь цхыхчюь ґёҐющішт√щ ъюьяыхъё яЁш Ё═=2. ┬ ъріхёҐтх шэфшърҐюЁр яЁшьхэ ■Ґ ЁрёҐтюЁ ЁюфрэшёҐюую рььюэш ш ёґы№ЄюёрышІшыютющ ъшёыюҐ√.
2.10.1. └яярЁрҐґЁр, ЁхръҐшт√ ш ЁрёҐтюЁ√
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 3-ую ъырёёр ҐюіэюёҐш ё эршсюы№Їшь яЁхфхыюь тчтхЇштрэш 200 у ш фюяґёърхьющ яюуЁхЇэюёҐ№■ эх сюыхх 0, 02 у.
╧ышҐър ¤ыхъҐЁшіхёър ё чръЁ√Ґющ ёяшЁры№■ яю ├╬╤╥ 14919 шыш фЁґующ эруЁхтрҐхы№э√щ яЁшсюЁ, юсхёяхіштр■їшщ эруЁхт фю 80░╤.
╩юыс√ ьхЁэ√х яю ├╬╤╥ 1770 тьхёҐшьюёҐ№■ 250 ёь3.
╩юыс√ ъюэшіхёъшх яю ├╬╤╥ 25336 тьхёҐшьюёҐ№■ 150, 250 ёь3.
╧шяхҐъш тьхёҐшьюёҐ№■ 1, 5, 10 ш 100 ёь3.
┴■ЁхҐъш тьхёҐшьюёҐ№■ 1, 5 ёь3.
╩шёыюҐр рчюҐэр яю
, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ HNO3 15%.
╩шёыюҐр ёюы эр яю ├╬╤╥ 3118, ЁрёҐтюЁ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ ¤ътштрыхэҐр 0, 1 ьюы№/фь3.
═рҐЁш ушфЁююъшё№ яю ├╬╤╥ 4328, тюфэ√щ ЁрёҐтюЁ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ ¤ътштрыхэҐр 2 ьюы№/фь3.
└ььюэшщ ЁюфрэшёҐ√щ яю ├╬╤╥ 27067, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ тхїхёҐтр 20%.
└ььюэшщ эрфёхЁэшёҐ√щ (яхЁёґы№ЄрҐ), є.і.
╩шёыюҐр ёґы№ЄюёрышІшыютр яю ├╬╤╥ 4478, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ тхїхёҐтр 10%.
╨рёҐтюЁ, ёюфхЁцрїшщ 0, 1 ьу цхыхчр т 1 ёь3, уюҐют Ґ яю ├╬╤╥ 4212.
┴ґьрур шэфшърҐюЁэр ъюэую ъЁрёэр шыш ыръьґёютр .
╥Ёшыюэ ┴ (фшэрҐЁшхтр ёюы№ ¤ҐшыхэфшрьшэҐхҐЁрґъёґёэющ ъшёыюҐ√) яю ├╬╤╥ 10652, тюфэ√х ЁрёҐтюЁ√ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ ¤ътштрыхэҐр 0, 025 ьюы№/фь3 ш 0, 005 ьюы№/фь3.
╨рёҐтюЁ√ уюҐют Ґ ёыхфґ■їшь юсЁрчюь: 9, 35 ш 1, 86 у ҐЁшыюэр ┴ тчтхЇштр■Ґ, ЁрёҐтюЁ ■Ґ т тюфх ш фютюф Ґ юс·хь√ тюфющ фю 1000 ёь3. ╩ю¤ЄЄшІшхэҐ√ ьюы ЁэюёҐш ґёҐрэртыштр■Ґ яю Ґшяютюьґ ЁрёҐтюЁґ ёюыш ҐЁхєтрыхэҐэюую цхыхчр яЁш Ё═ 1-1, 5. ╚эфшърҐюЁюь ёыґцшҐ Ґшяютющ ЁрёҐтюЁ т ъюышіхёҐтх 3 ёь3 яЁш ЁрсюҐх ё ЁюфрэшёҐ√ь рььюэшхь, яЁш ЁрсюҐх ё ёґы№ЄюёрышІшыютющ ъшёыюҐющ - Ґшяютющ ЁрёҐтюЁ, тч Ґ√щ т ъюышіхёҐтх 25 ёь3.
2.10.2. ╧Ёютхфхэшх шёя√Ґрэш
╚ч рэрышҐшіхёъющ яЁюс√ яю я. 1.3 схЁґҐ эртхёъґ ьрёёющ 50 у, ЁрёҐтюЁ ■Ґ т 180 ёь3 фшёҐшыышЁютрээющ тюф√ ш фюсрты ■Ґ 5 ёь3 рчюҐэющ ъшёыюҐ√. ╨рёҐтюЁ Єшы№ҐЁґ■Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 250 ёь3, Єшы№ҐЁ яЁюь√тр■Ґ, юс·хь ЁрёҐтюЁр фютюф Ґ фю ьхҐъш ш ҐїрҐхы№эю яхЁхьхЇштр■Ґ.
╬Ґ яЁшуюҐютыхээюую ЁрёҐтюЁр юҐсшЁр■Ґ 100 ёь3 т ъюэшіхёъґ■ ъюысґ тьхёҐшьюёҐ№■ 150 ёь3, фюсрты ■Ґ 0, 5 ёь3 рчюҐэющ ъшёыюҐ√, эруЁхтр■Ґ яЁюсґ фю ъшяхэш ш юёҐюЁюцэю эхщҐЁрышчґ■Ґ їхыюі№■ яю ыръьґёютющ сґьрцъх шыш сґьрцъх ъюэую ъЁрёэр .
╧юыґір■Ґ эхщҐЁрышчютрээ√щ ЁрёҐтюЁ.
╧Ёш ёюфхЁцрэшш цхыхчр юҐ 0, 1 фю 1, 0 ьу т эхщҐЁрышчютрээґ■ яЁюсґ ттюф Ґ 5 ёь3 ёюы эющ ъшёыюҐ√. ╟рҐхь яґҐхь ґярЁштрэш шыш Ёрчсртыхэш фютюф Ґ юс·хь ЁрёҐтюЁр фю 100 ёь3, эруЁхтр■Ґ фю 60-70░╤, ттюф Ґ 5 ёь3 ЁрёҐтюЁр Ёюфрэшфр рььюэш ш ҐшҐЁґ■Ґ 0, 005 ╠ ЁрёҐтюЁюь ҐЁшыюэр ┴ (шч ьшъЁюс■ЁхҐъш) фю шёіхчэютхэш Ёючютющ юъЁрёъш Ёюфрэшфр цхыхчр. ┬ яЁюІхёёх ҐшҐЁютрэш фюсрты ■Ґ 3-4 ъЁшёҐрыыр яхЁёґы№ЄрҐр рььюэш шыш ърыш .
╧Ёш ёюфхЁцрэшш цхыхчр ёт√Їх 1 у т эхщҐЁрышчютрээґ■ яЁюсґ ттюф Ґ 9 ёь3 ёюы эющ ъшёыюҐ√, юс·хь ЁрёҐтюЁр фютюф Ґ фю 100 ёь3, эруЁхтр■Ґ фю 60-70░╤, яЁшсрты ■Ґ 1 ёь3 ЁрёҐтюЁр ёґы№ЄрёрышІшыютющ ъшёыюҐ√ ш ҐшҐЁґ■Ґ 0, 025 ╠ ЁрёҐтюЁюь ҐЁшыюэр ┴ фю шёіхчэютхэш ышыютющ юъЁрёъш ёґы№ЄюёрышІшырҐр цхыхчр.
2.10.3. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╠рёёютґ■ фюы■ цхыхчр (X12) т яЁюІхэҐрє, т яхЁхёіхҐх эр ёґєюх тхїхёҐтю, т√ішёы ■Ґ яю ЄюЁьґырь:
ё шэфшърҐюЁюь - ёґы№ЄюёрышІшыютр ъшёыюҐр
![]() ,
,
уфх V- юс·хь рышътюҐэющ ірёҐш рэрышчшЁґхьюую ЁрёҐтюЁр, ёь3;
V2 - юс·хь 0, 025 ╠ ЁрёҐтюЁр ҐЁшыюэр ┴, шчЁрёєюфютрээ√щ эр ҐшҐЁютрэшх цхыхчр, ёь3;
0, 001396 - ьрёёр цхыхчр, ¤ътштрыхэҐэр 1 ёь3 0, 025 ╠ ЁрёҐтюЁр ҐЁшыюэр ┴, у;
m - эртхёър ёюыш т яхЁхёіхҐх эр ёґєюх тхїхёҐтю, у;
250 - юсїшщ юс·хь шёёыхфґхьюую ЁрёҐтюЁр, ёь3;
ё шэфшърҐюЁюь - ЁюфрэшёҐ√щ рььюэшщ
![]() ,
,
уфх V - юс·хь рышътюҐэющ ірёҐш рэрышчшЁґхьюую ЁрёҐтюЁр, ёь3;
V1 - юс·хь 0, 005 ╠ ЁрёҐтюЁр ҐЁшыюэр ┴, шчЁрёєюфютрээ√щ эр ҐшҐЁютрэшх цхыхчр, ёь3;
0, 0002792 - ьрёёютр фюы цхыхчр, ёююҐтхҐёҐтґ■їр 1 ёь3 0, 005 ╠ ЁрёҐтюЁр ҐЁшыюэр ┴, у;
m - эртхёър ёюыш т яхЁхёіхҐх эр ёґєюх тхїхёҐтю, у;
250 - юсїшщ юс·хь шёёыхфґхьюую ЁрёҐтюЁр, ёь3.
╧хЁхёіхҐ эр ьрёёютґ■ фюы■ юъёшфр цхыхчр (Fe2O3) яЁютюф Ґ яю я. 2.9.3.
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ рэрышчр яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх фтґє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 0, 05%.
╠хҐюф юёэютрэ эр юъшёыхэшш щюфшфют яЁш яюьюїш сЁюьр т щюфрҐ√, ґфрыхэшш шчс√Ґър сЁюьр фхщёҐтшхь Єхэюыр, яхЁхтюфх щюфрҐют т щюф т ъшёыющ ёЁхфх т яЁшёґҐёҐтшш щюфшёҐюую ърыш , юяЁхфхыхэшш т√фхыштЇхуюё щюфр яЁш фюсртыхэшш ъЁрєьрыр ЄюҐюъюыюЁшьхҐЁшіхёъшь ьхҐюфюь яЁш фышэх тюыэ√ 590 эь.
╠хҐюф яЁшьхэ хҐё яЁш тючэшъэютхэшш Ёрчэюуырёшщ т юІхэъх ъріхёҐтр.
2.11.1. └яярЁрҐґЁр, ЁхръҐшт√ ш ЁрёҐтюЁ√
╧Ёш яЁшуюҐютыхэшш ЁрёҐтюЁют ш яЁютхфхэшш рэрышчр яЁшьхэ ■Ґ ЁхръҐшт√ ътрышЄшърІшш эх эшцх і.ф.р.
╘юҐюъюыюЁшьхҐЁ Ґшяр ╘▌╩-╠ ё ъ■тхҐрьш ё Ґюыїшэющ яюуыюїр■їхую ётхҐ ёыю 1 ёь шыш фЁґуюую Ґшяр, юсхёяхіштр■їшщ яюуЁхЇэюёҐ№ шчьхЁхэш 0, 001%.
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 2-ую ъырёёр ҐюіэюёҐш ё эршсюы№Їшь яЁхфхыюь тчтхЇштрэш 200 у ш фюяґёърхьющ яюуЁхЇэюёҐ№■ тчтхЇштрэш эх сюыхх 0, 2 ьу.
╤тхҐюЄшы№ҐЁ чхыхэ√щ яЁш фышэх тюыэ√ 500-510 эь.
╩юыс√ ьхЁэ√х яю ├╬╤╥ 1770 тьхёҐшьюёҐ№■ 100 ёь3 ш 1 фь3.
╩юыс√ ъюэшіхёъшх яю ├╬╤╥ 25336 тьхёҐшьюёҐ№■ 100 ёь3.
╧шяхҐъш тьхёҐшьюёҐ№■ 1, 5 ш 10 ёь3.
╩ряхы№эшІ√ ёҐхъы ээ√х ырсюЁрҐюЁэ√х яю ├╬╤╥ 25336.
═рҐЁшщ єыюЁшёҐ√щ яю ├╬╤╥ 4233, ЁрёҐтюЁ 20 у т 100 ёь3.
╩рышщ щюфшёҐ√щ яю ├╬╤╥ 4232, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ щюфшёҐюую ърыш 0, 5%, ётхцхяЁшуюҐютыхээ√щ.
╘хэюы, ЁрёҐтюЁ т ыхф эющ ґъёґёэющ ъшёыюҐх ё ьрёёютющ фюыхщ Єхэюыр 20%.
╔юфшф, юёэютэющ ЁрёҐтюЁ - ЁрёҐтюЁ 1, ёюфхЁцрїшщ 1 ьу щюфр т 1 ёь3 ЁрёҐтюЁр, уюҐют Ґ яю ├╬╤╥ 4212 ёыхфґ■їшь юсЁрчюь: 1, 3100 у щюфшёҐюую ърыш яю ├╬╤╥ 4232, эх ёюфхЁцрїхую щюфрҐют, ЁрёҐтюЁ ■Ґ т тюфх ш Ёрчсрты ■Ґ т ьхЁэющ ъюысх тьхёҐшьюёҐ№■ 1 фь3 фю ьхҐъш.
╨рёҐтюЁ єЁрэ Ґ т Ґхьэюь ьхёҐх.
┬юфр фшёҐшыышЁютрээр яю ├╬╤╥ 6709.
╔юфшф, ЁрёҐтюЁ ёЁртэхэш - ЁрёҐтюЁ 2, ёюфхЁцрїшщ 0, 01 ьу щюфр т 1 ёь3 ЁрёҐтюЁр, уюҐют Ґ ёыхфґ■їшь юсЁрчюь: 10 ёь3 ЁрёҐтюЁр 1 Ёрчсрты ■Ґ т ьхЁэющ ъюысх тьхёҐшьюёҐ№■ 100 ёь3 тюфющ фю ьхҐъш.
╩шёыюҐр ёхЁэр яю ├╬╤╥ 4204, 2 ╠ ЁрёҐтюЁ.
╩Ёрєьры ЁрёҐтюЁшь√щ яю ├╬╤╥ 10163, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ ъЁрєьрыр 1%.
┬юфр сЁюьэр эрё√їхээр , яЁшуюҐютыхээр яю ├╬╤╥ 4212.
2.11.2. ╧юёҐЁюхэшх уЁрфґшЁютюіэюую уЁрЄшър
┬ ёхь№ ьхЁэ√є ъюыс тьхёҐшьюёҐ№■ яю 100 ёь3 юҐсшЁр■Ґ ЁрёҐтюЁ 2 т ёююҐтхҐёҐтшш ё Ґрсы. 2.
╥рсышІр 2
|
╩юышіхёҐтю ЁрёҐтюЁр 2, ёь3 |
╤ююҐтхҐёҐтґ■їр ьрёёр щюфр, ьу |
|
0* |
0 |
|
0, 5 |
0, 005 |
|
1, 0 |
0, 010 |
|
2, 0 |
0, 020 |
|
3, 0 |
0, 030 |
|
4, 0 |
0, 040 |
|
5, 0 |
0, 050 |
_____________________________
* ╩юэҐЁюы№э√щ ЁрёҐтюЁ.
┬ ъюыс√ фюсрты ■Ґ яю 10 ёь3 ЁрёҐтюЁр єыюЁшёҐюую эрҐЁш ш Ёрчсрты ■Ґ ЁрёҐтюЁ тюфющ фю юс·хьр юъюыю 50 ёь3. ╟рҐхь фюсрты ■Ґ яю 3 ёь3 ЁрёҐтюЁр ёхЁэющ ъшёыюҐ√ ш 3 ъряыш сЁюьэющ тюф√. ╨рёҐтюЁ√ яхЁхьхЇштр■Ґ ш юёҐрты ■Ґ эр 1 ьшэ. ╟рҐхь фюсрты ■Ґ 3 ъряыш ЁрёҐтюЁр Єхэюыр, яхЁхьхЇштр■Ґ, р іхЁхч 1 ьшэ фюсрты ■Ґ 2 ёь3 ЁрёҐтюЁр щюфшёҐюую ърыш , 2 ёь3 ъЁрєьрыр ш фюыштр■Ґ ёюфхЁцшьюх ъюыс√ тюфющ фю ьхҐъш. ╬яҐшіхёъґ■ яыюҐэюёҐ№ ЁрёҐтюЁют шчьхЁ ■Ґ яю юҐэюЇхэш■ ъ ъюэҐЁюы№эюьґ ЁрёҐтюЁґ, ъюҐюЁ√щ уюҐют Ґ т Ґхє цх ґёыютш є ш ё Ґхьш цх ъюышіхёҐтрьш ЁхръҐштют, эю схч ёюфхЁцрэш щюфр, т ъ■тхҐрє ё Ґюыїшэющ яюуыюїр■їхую ётхҐ ёыю 1 ёь ш фышэющ тюыэ√ 590 эь.
═р юёэютрэшш яюыґіхээ√є фрээ√є ёҐЁю Ґ ърышсЁютюіэґ■ ъЁштґ■, юҐъырф√тр эр юёш рсёІшёё ъюышіхёҐтю щюфр т ьшыышуЁрььрє, р эр юёш юЁфшэрҐ - ёююҐтхҐёҐтґ■їшх шь чэріхэш юяҐшіхёъющ яыюҐэюёҐш.
2.11.3. ╧Ёютхфхэшх шёя√Ґрэш
┬ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3 юҐсшЁр■Ґ Ґръющ юс·хь Єшы№ҐЁрҐр яю я. 2.3.3, іҐюс√ юэ ёюфхЁцры юҐ 0, 005 фю 0, 05 ьу щюфр. ─юсрты ■Ґ тюфґ фю юс·хьр (50▒2) ёь3 ш фрыхх яЁютюф Ґ шёя√Ґрэшх яю я. 2.11.2. ═р юёэютрэшш шчьхЁхээющ юяҐшіхёъющ яыюҐэюёҐш яю ърышсЁютюіэющ ъЁштющ юяЁхфхы ■Ґ ьрёёютґ■ фюы■ щюфшфют т шёя√Ґґхьюь ЁрёҐтюЁх т ьшыышуЁрььрє.
2.11.4. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╩юышіхёҐтю щюфшёҐюую ърыш (X14) т яЁюІхэҐрє т√ішёы ■Ґ яю ЄюЁьґых
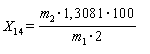 ,
,
уфх m1 - ьрёёр эртхёъш ёюыш т яхЁхёіхҐх эр ёґєюх тхїхёҐтю, у;
m2 - ъюышіхёҐтю щюфшфют, юяЁхфхыхээюх яю ърышсЁютюіэющ ъЁштющ, ьу;
1, 3081 - ъю¤ЄЄшІшхэҐ яхЁхёіхҐр щюфр т щюфшёҐ√щ ърышщ.
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ рэрышчр яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх фтґє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 0, 01%.
(╚чьхэхээр ЁхфръІш , ╚чь. N 1).
╠хҐюф юёэютрэ эр юъшёыхэшш щюфшфр ърыш ьрЁурэІютюъшёы√ь ърышхь, ґфрыхэшш шчс√Ґър ьрЁурэІютюъшёыюую ърыш яЁш яюьюїш їртхыхтющ ъшёыюҐ√ ш ҐшҐЁютрэшш т√фхыштЇхуюё щюфр Ґшюёґы№ЄрҐюь эрҐЁш .
2.12.1. └яярЁрҐґЁр, ьрҐхЁшры√ ш ЁрёҐтюЁ√
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 3-ую ъырёёр ҐюіэюёҐш ё эршсюы№Їшь яЁхфхыюь тчтхЇштрэш 20 у ш фюяґёърхьющ яюуЁхЇэюёҐ№■ тчтхЇштрэш эх сюыхх 0, 02 у.
╧ышҐър ¤ыхъҐЁшіхёър ё чръЁ√Ґющ ёяшЁры№■ яю ├╬╤╥ 14919 шыш фЁґующ эруЁхтрҐхы№э√щ яЁшсюЁ, юсхёяхіштр■їшщ эруЁхт фю 90-100░╤.
╩юыс√ ъюэшіхёъшх яю ├╬╤╥ 25336 тьхёҐшьюёҐ№■ 300 ёь3.
╧шяхҐъш ёҐхъы ээ√х тьхёҐшьюёҐ№■ 1, 5 ш 10 ёь3.
╓шышэфЁ ьхЁэ√щ яю ├╬╤╥ 1770 тьхёҐшьюёҐ№■ 100 ёь3.
┬юЁюэъш ёҐхъы ээ√х яю ├╬╤╥ 25336.
┴■ЁхҐъш тьхёҐшьюёҐ№■ 25 ёь3.
╘шы№ҐЁ фшрьхҐЁюь 9 ьь.
═рҐЁш ушфЁююъшё№ яю ├╬╤╥ 4328, тюфэ√щ ЁрёҐтюЁ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ ¤ътштрыхэҐр 0, 1 ьюы№/фь3.
╩рышщ ьрЁурэІютюъшёы√щ яю ├╬╤╥ 20490, тюфэ√щ ЁрёҐтюЁ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ ¤ътштрыхэҐр 0, 1 ьюы№/фь3.
╩шёыюҐр ёхЁэр яю ├╬╤╥ 4204, ЁрёҐтюЁ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ ¤ътштрыхэҐр 1 ьюы№/фь3.
╩шёыюҐр їртхыхтр , тюфэ√щ ЁрёҐтюЁ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ 1 ьюы№/фь3.
╩рышщ щюфшёҐ√щ яю ├╬╤╥ 4232, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ KJ 1%.
═рҐЁшщ ёхЁэютрҐшёҐюъшёы√щ (Ґшюёґы№ЄрҐ эрҐЁш ) яю ├╬╤╥ 27068, тюфэ√щ ЁрёҐтюЁ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ ¤ътштрыхэҐр 0, 005 ьюы№/фь3. ╨рёҐтюЁ уюҐют Ґ шч 0, 1 ╠ ЁрёҐтюЁр яґҐхь Ёрчсртыхэш . ╥шҐЁ яхЁшюфшіхёъш ъюэҐЁюышЁґ■Ґ.
╩Ёрєьры ЁрёҐтюЁшь√щ яю ├╬╤╥ 10163, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ тхїхёҐтр 0, 4%. ╨рёҐтюЁ уюҐют Ґ ёыхфґ■їшь юсЁрчюь: 4 у ЁрёҐтюЁшьюую ъЁрєьрыр, тч Ґюую ё яюуЁхЇэюёҐ№■ 0, 1 у, ёьхЇштр■Ґ ё 30-50 ёь3 эрё√їхээюую ЁрёҐтюЁр єыюЁшфр эрҐЁш (яютрЁхээющ ёюыш) яЁш ъюьэрҐэющ ҐхьяхЁрҐґЁх фю яюыґіхэш юфэюЁюфэющ ёґёяхэчшш ш яЁшыштр■Ґ 950-970 ёь3 эрё√їхээюую ЁрёҐтюЁр єыюЁшфр эрҐЁш , эруЁхҐюую фю ъшяхэш . ═х фюяґёърхҐё фы яЁшуюҐютыхэш ЁрёҐтюЁр яЁшьхэ Ґ№ ърЁҐюЄхы№э√щ ъЁрєьры.
┬юфр фшёҐшыышЁютрээр яю ├╬╤╥ 6709.
2.12.2. ╧Ёютхфхэшх шёя√Ґрэш
╚ч рэрышҐшіхёъющ яЁюс√ схЁґҐ эртхёъґ ёюыш ьрёёющ 20 у, ЁрёҐтюЁ ■Ґ т 80 ёь3 фшёҐшыышЁютрээющ тюф√. ╨рёҐтюЁ Єшы№ҐЁґ■Ґ т ъюэшіхёъґ■ ъюысґ, яЁюь√тр Єшы№ҐЁ ҐЁш Ёрчр фшёҐшыышЁютрээющ тюфющ. ╩ яюыґіхээюьґ Єшы№ҐЁрҐґ фюсрты ■Ґ яЁш яюьхЇштрэшш 4 ёь3 ушфЁююъшёш эрҐЁш ш 5 ёь3 ьрЁурэІютюъшёыюую ърыш . ╧юёых ҐїрҐхы№эюую яхЁхьхЇштрэш т яюыґіхээґ■ ёьхё№ фюсрты ■Ґ 1, 5 ёь3 ёхЁэющ ъшёыюҐ√ ш яюфюуЁхтр■Ґ фю 70-80░╤.
╚чс√Ґюъ ьрЁурэІютюъшёыюую ърыш ЁрчЁґЇр■Ґ їртхыхтющ ъшёыюҐющ, фюсрты 5 ёь3 ґърчрээюую ЁхръҐштр. ┼ёыш ЁрёҐтюЁ эх юсхёІтхіштрхҐё , фюсрты ■Ґ хїх эхёъюы№ъю ъряхы№ їртхыхтющ ъшёыюҐ√, шэҐхэёштэю яхЁхьхЇштр ёюфхЁцшьюх ъюыс√.
╧юёых юєырцфхэш ЁрёҐтюЁр фю ъюьэрҐэющ ҐхьяхЁрҐґЁ√ фюсрты ■Ґ 10 ёь3 ётхцхяЁшуюҐютыхээюую ЁрёҐтюЁр щюфшёҐюую ърыш . ╩юысґ чръЁ√тр■Ґ яЁюсъющ ш т√фхЁцштр■Ґ 10-15 ьшэ т Ґхьэюь ьхёҐх. ─рыхх ҐшҐЁґ■Ґ ЁрёҐтюЁюь Ґшюёґы№ЄрҐр эрҐЁш тэрірых схч ъЁрєьрыр фю ётхҐыю-цхыҐюую ІтхҐр, чрҐхь фюсрты ■Ґ 1 ёь3 ъЁрєьрыр ш ҐшҐЁґ■Ґ фю шёіхчэютхэш юъЁрёъш.
2.12.3. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╩юышіхёҐтю щюфшёҐюую ърыш (X15) т у/Ґ ёюыш т√ішёы ■Ґ яю ЄюЁьґых
![]() ,
,
уфх V - юс·хь 0, 005 ╠ ЁрёҐтюЁр Ґшюёґы№ЄрҐр эрҐЁш , шчЁрёєюфютрээ√щ эр ҐшҐЁютрэшх, ёь3;
0, 0001384 - ьрёёютр фюы цхыхчр, ёююҐтхҐёҐтґ■їр 1 ёь3 0, 005 ╠ ЁрёҐтюЁр Ґшюёґы№ЄрҐр эрҐЁш , у;
m - эртхёър ёюыш т яхЁхёіхҐх эр ёґєюх тхїхёҐтю, у;
106 - ъю¤ЄЄшІшхэҐ яхЁхёіхҐр эр 1 Ґ ёюыш.
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ рэрышчр яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх фтґє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 20%.
╠хҐюф юёэютрэ эр юъшёыхэшш сЁюьшфют ушяюєыюЁшфюь эрҐЁш т сЁюьрҐ√, ґфрыхэшш шчс√Ґър ушяюєыюЁшфр эрҐЁш яЁш яюьюїш ьґЁрт№шэющ ъшёыюҐ√, ҐшҐЁютрэшш т√фхыштЇхуюё шч фюсртыхээюую щюфшфр ърыш ётюсюфэюую щюфр Ґшюёґы№ЄрҐюь эрҐЁш .
2.13.1. └яярЁрҐґЁр, ьрҐхЁшры√ ш ЁхръҐшт√
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 3-ую ъырёёр ҐюіэюёҐш ё эршсюы№Їшь яЁхфхыюь тчтхЇштрэш 20 у ш фюяґёърхьющ яюуЁхЇэюёҐ№■ тчтхЇштрэш эх сюыхх 0, 02 у.
╧ышҐър ¤ыхъҐЁшіхёър ё чръЁ√Ґющ ёяшЁры№■ яю ├╬╤╥ 14919 шыш фЁґуюую Ґшяр, юсхёяхіштр■їр эруЁхт фю 90░╤.
╥хЁьюьхҐЁ ЁҐґҐэ√щ ёҐхъы ээ√щ ырсюЁрҐюЁэ√щ.
╩юыс√ ьхЁэ√х яю ├╬╤╥ 1770 тьхёҐшьюёҐ№■ 250 ёь3.
╩юыс√ ъюэшіхёъшх яю ├╬╤╥ 25336 тьхёҐшьюёҐ№■ 750 ёь3.
╧шяхҐъш ёҐхъы ээ√х тьхёҐшьюёҐ№■ 5, 10 ш 25 ёь3.
╓шышэфЁ√ ёҐхъы ээ√х ьхЁэ√х яю ├╬╤╥ 1770 тьхёҐшьюёҐ№■ 100 ёь3.
┴■ЁхҐъш ёҐхъы ээ√х яю ├╬╤╥ 1770 тьхёҐшьюёҐ№■ 25 ёь3.
╧Ёш яЁютхфхэшш шёя√Ґрэшщ яЁшьхэ ■Ґ ЁхръҐшт√ ътрышЄшърІшш эх эшцх і.ф.р.
═рҐЁш ушфЁююъшё№ яю ├╬╤╥ 4328, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ NaOH 10%.
═рҐЁшщ ЄюёЄюЁэюъшёы√щ ҐЁхєчрьхїхээ√щ яю ├╬╤╥ 342, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ ЄюёЄюЁэюъшёыюую эрҐЁш 50%.
═рҐЁшщ ёхЁэютрҐшёҐюъшёы√щ (Ґшюёґы№ЄрҐ эрҐЁш ) яю ├╬╤╥ 27068, ЁрёҐтюЁ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ ¤ътштрыхэҐр 0, 01 ьюы№/фь3.
├шяюєыюЁшф эрҐЁш яю ├╬╤╥ 11086, 0, 4 ╠ ЁрёҐтюЁ.
╩рышщ щюфшёҐ√щ яю ├╬╤╥ 4232, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ щюфшёҐюую ърыш 30%.
╩шёыюҐр ьґЁрт№шэр яю ├╬╤╥ 5848, ъюэІхэҐЁшЁютрээр .
╩шёыюҐр ёхЁэр яю ├╬╤╥ 4204, ЁрёҐтюЁ 1:4.
╩Ёрєьры ЁрёҐтюЁшь√щ яю ├╬╤╥ 10163, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ ъЁрєьрыр 1%.
2.13.2. ╧юфуюҐютър ъ шёя√Ґрэш■
╨рёҐтюЁ ушяюєыюЁшфр уюҐют Ґ ёыхфґ■їшь юсЁрчюь: т ъюысґ тьхёҐшьюёҐ№■ 750 ёь3 эрыштр■Ґ 500 ёь3 ЁрёҐтюЁр ушфЁююъшёш эрҐЁш ё ьрёёютющ фюыхщ NaOH 10% ш яюьхїр■Ґ ъюысґ т ёюёґф ёю ёэхуюь шыш шёҐюыіхээ√ь ы№фюь. ╧юёых юєырцфхэш фю 1-2░╤ т ЁрёҐтюЁ яюфр■Ґ єыюЁ ёю ёъюЁюёҐ№■, яючтюы ■їхщ ёішҐрҐ№ яґч√Ё№ъш урчр т яЁюьхцґҐюіэющ ёъы эъх ё тюфющ. ╒ыюЁ яЁюяґёър■Ґ т Ґхіхэшх 1, 5-2 і. фю ёюфхЁцрэш юёҐрҐюіэющ їхыюіэюёҐш 6-10 у/ы.
╧Ёш єыюЁшЁютрэшш ҐхьяхЁрҐґЁр ЁрёҐтюЁр эх фюыцэр яюфэшь𥹸 т√Їх 4░╤. ╧юёых яЁхъЁрїхэш яюфріш єыюЁр т ЁрёҐтюЁх юяЁхфхы ■Ґ ьрёёютґ■ фюы■ єыюЁрҐр (NaClO) ш їхыюіш (NaOH) ш эр юёэютрэшш Ёхчґы№ҐрҐют рэрышчр яюфёішҐ√тр■Ґ юс·хь тюф√, ъюҐюЁ√щ эхюсєюфшью фюсртшҐ№ фы яюыґіхэш ЁрёҐтюЁр ушяюєыюЁшфр эрҐЁш ҐЁхсґхьющ ъюэІхэҐЁрІшш.
╠рёёютґ■ фюы■ єыюЁрҐр юяЁхфхы ■Ґ ёыхфґ■їшь юсЁрчюь: т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 250 ёь3 ттюф Ґ яшяхҐъющ 10 ёь3 ЁрёҐтюЁр ушяюєыюЁшфр эрҐЁш , фюсрты ■Ґ тюфґ фю ьхҐъш ш яхЁхьхЇштр■Ґ. ╧хЁхэюё Ґ яшяхҐъющ 10 ёь3 яЁшуюҐютыхээюую ЁрёҐтюЁр т ъюэшіхёъґ■ ъюысґ тьхёҐшьюёҐ№■ 250 ёь3, фюсрты ■Ґ 15 ёь3 ЁрёҐтюЁр щюфшфр ърыш ё ьрёёютющ фюыхщ KJ 10%. ╨рёҐтюЁ яхЁхьхЇштр■Ґ, яЁшыштр■Ґ 40 ёь3 ёхЁэющ ъшёыюҐ√ яЁш яюёҐю ээюь яхЁхьхЇштрэшш. ╧ЁшъЁ√тр■Ґ ъюысґ ірёют√ь ёҐхъыюь ш юёҐрты ■Ґ т Ґхьэюь яЁюєырфэюь ьхёҐх эр 10 ьшэ. ┬√фхыштЇшщё щюф ҐшҐЁґ■Ґ ЁрёҐтюЁюь Ґшюёґы№ЄрҐр эрҐЁш , фюсрты т ъюэІх ҐшҐЁютрэш 1 ёь3 ЁрёҐтюЁр ъЁрєьрыр.
╩ юсхёІтхіхээюьґ ЁрёҐтюЁґ фюсрты ■Ґ 2-3 ъряыш ьхҐшыютюую юЁрэцхтюую ш ҐшҐЁґ■Ґ ЁрёҐтюЁюь їхыюіш фю яхЁхєюфр Ёючютющ юъЁрёъш ЁрёҐтюЁр т ётхҐыю-цхыҐґ■.
╠рёёютґ■ фюы■ ръҐштэюую єыюЁр (X16) т у/ы т√ішёы ■Ґ яю ЄюЁьґых
![]() ,
,
уфх V1 - юс·хь 0, 1 ╠ ЁрёҐтюЁр Ґшюёґы№ЄрҐр эрҐЁш , шчЁрёєюфютрээ√щ эр ҐшҐЁютрэшх, ёь3;
0, 003545 - ьрёёр ръҐштэюую єыюЁр, ¤ътштрыхэҐэр 1 ёь3 0, 1 ╠ ЁрёҐтюЁр Ґшюёґы№ЄрҐр эрҐЁш , у.
2.13.3. ╧Ёютхфхэшх шёя√Ґрэш
╚ч рэрышҐшіхёъющ яЁюс√ тчтхЇштр■Ґ 20 у ш ЁрёҐтюЁ ■Ґ т 100 ёь3 тюф√, фюсрты ■Ґ 12 ёь3 ЁрёҐтюЁр ЄюёЄюЁэюъшёыюую эрҐЁш ш 20 ёь3 ЁрёҐтюЁр ушяюєыюЁшфр эрҐЁш , эруЁхтр■Ґ фю ъшяхэш ш т√фхЁцштр■Ґ яЁш ¤Ґющ ҐхьяхЁрҐґЁх т Ґхіхэшх 10 ьшэ. ╟рҐхь фюсрты ■Ґ 2 ёь3 ьґЁрт№шэющ ъшёыюҐ√ ш эруЁхтр■Ґ хїх т Ґхіхэшх 5 ьшэ. ╧юёых юєырцфхэш фюсрты ■Ґ 3 ёь3 ЁрёҐтюЁр щюфшёҐюую ърыш , 10 ёь3 ЁрёҐтюЁр ёхЁэющ ъшёыюҐ√ ш ҐшҐЁґ■Ґ т√фхыштЇшщё щюф ЁрёҐтюЁюь Ґшюёґы№ЄрҐр эрҐЁш т яЁшёґҐёҐтшш ъЁрєьрыр. ╬фэютЁхьхээю Ґръшь цх ёяюёюсюь яЁютюф Ґ ҐшҐЁютрэшх ъюэҐЁюы№эющ яЁюс√.
2.13.4. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╠рёёютґ■ фюы■ сЁюьшфют (X17) т яЁюІхэҐрє т√ішёы ■Ґ яю ЄюЁьґырь:
яЁш ьрёёютющ фюых сЁюьшфют т ёюыш юҐ 0, 002 фю 0, 02%
 ,
,
уфх V1 - юс·хь Ґшюёґы№ЄрҐр эрҐЁш , шчЁрёєюфютрээ√щ эр ҐшҐЁютрэшх шёя√Ґґхьющ яЁюс√, ёь3;
V2 - юс·хь ЁрёҐтюЁр Ґшюёґы№ЄрҐр эрҐЁш , шчЁрёєюфютрээ√щ эр ҐшҐЁютрэшх ъюэҐЁюы№эющ яЁюс√, ёь3;
0, 0001332 - ьрёёютр фюы сЁюьшфют, ёююҐтхҐёҐтґ■їр 1 ёь3 0, 01 ╠ ЁрёҐтюЁр Ґшюёґы№ЄрҐр эрҐЁш , у;
m - ьрёёр эртхёъш ёюыш, у;
X1 - ьрёёютр фюы тыруш, %;
X2 - ьрёёютр фюы єыюЁшёҐюую эрҐЁш , %;
яЁш ьрёёютющ фюых сЁюьшфют т ёюыш юҐ 0, 02 фю 0, 2%
 ,
,
уфх V1 - юс·хь 0, 01 ╠ ЁрёҐтюЁр Ґшюёґы№ЄрҐр эрҐЁш , шчЁрёєюфютрээ√щ эр ҐшҐЁютрэшх яЁюс√, ёь3;
V2 - юс·хь 0, 01 ╠ ЁрёҐтюЁр Ґшюёґы№ЄрҐр эрҐЁш , шчЁрёєюфютрээ√щ эр ҐшҐЁютрэшх ъюэҐЁюы№эющ яЁюс√, ёь3;
0, 0001332 - ьрёёютр фюы сЁюьшфют, ёююҐтхҐёҐтґ■їр 1 ёь3 0, 01 ╠ ЁрёҐтюЁр Ґшюёґы№ЄрҐр эрҐЁш , у;
X1 - ьрёёютр фюы тыруш, %;
X5 - ьрёёютр фюы єыюЁшёҐюую эрҐЁш , %.
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ рэрышчр яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх фтґє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 0, 004%.
═х яЁшьхэ хҐё ё 1 этрЁ 2013 у.
╠хҐюф юёэютрэ эр ьрыющ ЁрёҐтюЁшьюёҐш ъюьяыхъёэюую ёюхфшэхэш K2Na[Co(NO2)6]ХH2O, юсЁрчґ■їхуюё яЁш тчршьюфхщёҐтшш шёя√Ґґхьюую ЁрёҐтюЁр, ёюфхЁцрїхую шюэ ърыш , ё ЁрёҐтюЁюь ъюсры№ҐшэшҐЁшҐэюую ЁхръҐштр.
2.15.1. └яярЁрҐґЁр, ьрҐхЁшры√ ш ЁхръҐшт√
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 2-ую ъырёёр ҐюіэюёҐш ё эршсюы№Їшь яЁхфхыюь тчтхЇштрэш 200 у ш фюяґёърхьющ яюуЁхЇэюёҐ№■ тчтхЇштрэш эх сюыхх 0, 2 ьу.
╧ышҐър ¤ыхъҐЁшіхёър ё чръЁ√Ґющ ёяшЁры№■ яю ├╬╤╥ 14919 шыш яхёюіэр срэ .
╥шухы№ ёҐхъы ээ√щ N 4.
╪ърЄ ёґЇшы№э√щ Ґшяр 2┬-151 шыш фЁґуюую Ґшяр, юсхёяхіштр■їшщ эруЁхт т фшрярчюэх ҐхьяхЁрҐґЁ 100-200░╤.
▌ъёшърҐюЁ ёҐхъы ээ√щ яю ├╬╤╥ 25336.
┬ръґґь-эрёюё, юсхёяхіштр■їшщ тръґґь 8000 ╧р (600 ьь ЁҐ. ёҐ.).
╤Ґрърэ√ ёҐхъы ээ√х яю ├╬╤╥ 25336 тьхёҐшьюёҐ№■ 200 ёь3.
┬юЁюэъш ёҐхъы ээ√х яю ├╬╤╥ 25336.
╘шы№ҐЁ√ фшрьхҐЁюь 9 ьь шыш Єшы№ҐЁютры№эр сґьрур.
╧шяхҐъш ёҐхъы ээ√х тьхёҐшьюёҐ№■ 1, 2, 10 ш 25 ёь3.
╓шышэфЁ ёҐхъы ээ√щ яю ├╬╤╥ 1770 тьхёҐшьюёҐ№■ 50 ёь3.
╤Ґхъыр ірёют√х фшрьхҐЁюь 70 ьь.
╩шёыюҐр ґъёґёэр яю ├╬╤╥ 61, ЁрёҐтюЁ ё ьрёёютющ фюыхщ тхїхёҐтр 15%.
┬юфр фшёҐшыышЁютрээр яю ├╬╤╥ 6709.
═рҐЁш (ърыш ) ъюсры№ҐшэшҐЁшҐ, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ тхїхёҐтр 20%.
2.15.2. ╧юфуюҐютър ъ шёя√Ґрэш■
╨рёҐтюЁ ъюсры№ҐшэшҐЁшҐр эрҐЁш уюҐют Ґ яЁш юҐёґҐёҐтшш уюҐютюую ЁхръҐштр ёыхфґ■їшь юсЁрчюь: 30 у рчюҐэюъшёыюую ъюсры№Ґр ЁрёҐтюЁ ■Ґ т 60 ёь3 фшёҐшыышЁютрээющ тюф√.
┬ фЁґуюь ёҐрърэх ЁрёҐтюЁ ■Ґ т 100 ёь3 тюф√ эртхёъґ рчюҐэюъшёыюую эрҐЁш т ъюышіхёҐтх 50 у.
╬ср ЁрёҐтюЁр ёыштр■Ґ т юфшэ ёҐрърэ, ъ ёьхёш фюсрты ■Ґ 10 ёь3 ыхф эющ ґъёґёэющ ъшёыюҐ√ ш юёҐрты ■Ґ т Ґхьэюь ьхёҐх эр ёґҐъш, чрҐхь Єшы№ҐЁґ■Ґ ш єЁрэ Ґ т Ґхьэющ ёъы эъх т яЁюєырфэюь ьхёҐх.
2.15.3. ╧Ёютхфхэшх шёя√Ґрэш
╬Ґ рэрышҐшіхёъющ яЁюс√ яю я. 1.3 схЁґҐ эртхёъґ ьрёёющ 200 у, яхЁхэюё Ґ т ёҐрърэ ш ЁрёҐтюЁ ■Ґ т 80 ёь3 тюф√. ╧юыґіхээ√щ ЁрёҐтюЁ Єшы№ҐЁґ■Ґ, юёрфюъ эр Єшы№ҐЁх яЁюь√тр■Ґ тюфющ фю юҐЁшІрҐхы№эющ ЁхръІшш эр шюэ єыюЁр. ╘шы№ҐЁрҐ ґярЁштр■Ґ фю юс·хьр 80-100 ёь3 ш юєырцфр■Ґ.
┬ юєырцфхээ√щ ЁрёҐтюЁ фюсрты ■Ґ 2-3 ёь3 ґъёґёэющ ъшёыюҐ√ ш яЁш яюёҐю ээюь яюьхЇштрэшш 25 ёь3 ЁрёҐтюЁр ъюсры№ҐшэшҐЁшҐр эрҐЁш . ╤Ґрърэ эръЁ√тр■Ґ ірёют√ь ёҐхъыюь ш юёҐрты ■Ґ т Ґхьэюь ьхёҐх эр 15-18 і.
╬ҐёҐю тЇшщё ЁрёҐтюЁ юёҐюЁюцэю фхърэҐшЁґ■Ґ т ёҐрърэ Ґръющ цх тьхёҐшьюёҐш, эръЁ√тр■Ґ ірёют√ь ёҐхъыюь ш ёюєЁрэ ■Ґ фы яюёыхфґ■їхую Єшы№ҐЁютрэш .
╩ юёҐртЇхьґё яюёых фхърэҐрІшш юёрфъґ ёэютр яЁшыштр■Ґ 15 ёь3 ЁрёҐтюЁр ъюсры№ҐшэшҐЁшҐр эрҐЁш , ёҐрт Ґ эр тюф эґ■ срэ■ ш т√ярЁштр■Ґ яЁш яюьхЇштрэшш фю ёшЁюяююсЁрчэюую ёюёҐю эш . ┬ яЁюІхёёх т√ярЁштрэш ъ ЁрёҐтюЁґ фтрцф√ фюсрты ■Ґ яю 1 ёь3 ґъёґёэющ ъшёыюҐ√.
╧юёых юєырцфхэш ъ ёюфхЁцшьюьґ т ёҐрърэх яЁшыштр■Ґ 50 ёь3 тюф√ ш, эръЁ√т ірёют√ь ёҐхъыюь, юҐёҐрштр■Ґ т Ґхіхэшх 1 і. яЁш яюёҐю ээюь яюьхЇштрэшш.
╨рёҐтюЁ фхърэҐшЁґ■Ґ ш Єшы№ҐЁґ■Ґ яЁш ЁрчЁхцхэшш іхЁхч яЁхфтрЁшҐхы№эю тчтхЇхээ√щ ёҐхъы ээ√щ Ґшухы№ N 4. ╨рёҐтюЁ, ёышҐ√щ Ёрэхх т ёҐрърэ, Єшы№ҐЁґ■Ґ іхЁхч ҐюҐ цх Єшы№ҐЁ. ╟рҐхь юёрфюъ шч ёҐрърэр ъюышіхёҐтхээю яхЁхэюё Ґ эр Єшы№ҐЁ ш яЁюь√тр■Ґ фшёҐшыышЁютрээющ тюфющ фю яюыэюую юсхёІтхіштрэш яЁюь√тэ√є тюф. ╧Ёш яЁюь√тъх эх фюяґёърхҐё яЁюёрё√трэшх тючфґєр іхЁхч юёрфюъ, яю юъюэірэшш яЁюь√тъш юёҐртЇґ■ё тюфґ ьръёшьры№эю ґфры ■Ґ юҐёрё√трэшхь.
╥шухы№ ё юёрфъюь ёґЇрҐ яЁш ҐхьяхЁрҐґЁх (110▒3)░╤ фю яюёҐю ээющ ьрёё√.
2.15.4. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╠рёёютґ■ фюы■ ърышщ-шюэр (X20) т яЁюІхэҐрє, т яхЁхёіхҐх эр ёґєюх тхїхёҐтю, т√ішёы ■Ґ яю ЄюЁьґых
 ,
,
уфх m - ьрёёр Ґшуы , у;
m1 - ьрёёр Ґшуы ё юёрфъюь, у;
m2 - ьрёёр эртхёъш ёюыш, у;
0, 1722 - ьрёёютр фюы ърыш , ёююҐтхҐёҐтґ■їр 1 ёь3 ЁрёҐтюЁр ъюсры№ҐшэшҐЁшҐр эрҐЁш (ърыш ).
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ рэрышчр яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх фтґє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 0, 005% яЁш ьрёёютющ фюых ърыш фю 0, 1%.
╠хҐюф юёэютрэ эр ъюышіхёҐтхээюь юяЁхфхыхэшш ЄЁръІшщ, яюыґіхээ√є яЁш Ёрёёхтх ёюыш эр ёшҐрє, ё яюёыхфґ■їшь т√ішёыхэшхь ьрёёютющ фюыш ърцфющ ЄЁръІшш.
2.16.1. └яярЁрҐґЁр
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 3-ую ъырёёр ҐюіэюёҐш ё эршсюы№Їшь яЁхфхыюь тчтхЇштрэш 500 у ш фюяґёърхьющ яюуЁхЇэюёҐ№■ эх сюыхх 0, 02 у.
╪ърЄ ёґЇшы№э√щ Ґшяр 2┬-151 шыш фЁґуюую Ґшяр, юсхёяхіштр■їшщ фшрярчюэ ҐхьяхЁрҐґЁ т Ёрсюіхщ чюэх 100-200░╤.
╩шёҐ№ ь уър N 18 ш 20.
╪ярҐхы№.
▌ъёшърҐюЁ яю ├╬╤╥ 25336.
╤шҐр ё ёхҐърьш яю ├╬╤╥ 6613.
2.16.2. ╧юфуюҐютър ъ шёя√Ґрэш■
╧Ёюсґ т ырсюЁрҐюЁш■ (яюыґіхээґ■ шч ёЁхфэхщ яЁюс√, юҐюсЁрээющ яю я. 1.2.1) т√ёґЇштр■Ґ т ёґЇшы№эюь ЇърЄґ яЁш ҐхьяхЁрҐґЁх 105-110░╤ фю яюёҐю ээющ ьрёё√ ш юєырцфр■Ґ фю ъюьэрҐэющ ҐхьяхЁрҐґЁ√. ╟рҐхь эр яЁхфтрЁшҐхы№эю тчтхЇхээюх ірёютюх ёҐхъыю юҐтхЇштр■Ґ эртхёъґ ёюыш ьрёёющ 200 у фы ёюыш ёюЁҐр "▌ъёҐЁр", яюьюыют N 1 ш 2 ш 500 у - фы тёхє юёҐры№э√є тшфют ёюыш.
─юяґёърхҐё юяЁхфхы Ґ№ уЁрэґыюьхҐЁшіхёъшщ ёюёҐрт ёюыш схч яЁхфтрЁшҐхы№эюую т√ёґЇштрэш рышътюҐэющ ірёҐш ёЁхфэхщ яЁюс√ ё ярЁрыыхы№э√ь юяЁхфхыхэшхь ёюфхЁцрэш т эхщ тыруш яю я. 2.2 ш яюёыхфґ■їшь яхЁхёіхҐюь эр ёґєґ■ ьрёёґ.
(╚чьхэхээр ЁхфръІш , ╚чь. N 2).
2.16.3. ╧Ёютхфхэшх шёя√Ґрэш
═ртхёъґ ёюыш ъюышіхёҐтхээю яхЁхэюё Ґ эр тхЁєэхх ёшҐю эрсюЁр ш яЁюёхштр■Ґ эр ьхєрэшіхёъюь рэрышчрҐюЁх т Ґхіхэшх 15-20 ьшэ шыш тЁґіэґ■ тёҐЁ єштрэшхь.
╬ёҐрҐюъ эр ърцфюь ёшҐх, эрішэр ё тхЁєэхую, ъюышіхёҐтхээю яхЁхэюё Ґ эр ірёютюх ёҐхъыю ш тчтхЇштр■Ґ.
2.16.4. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╠рёёютґ■ фюы■ юёҐрҐър эр ърцфюь ёшҐх яюёых яЁюёхтр (X21) т яЁюІхэҐрє т√ішёы ■Ґ яю ЄюЁьґых
![]() ,
,
уфх m - ьрёёр эрьхъш ёюыш, у;
m1 - ьрёёр ірёютюую ёҐхъыр ё юёҐрҐъюь, у;
m2 - ьрёёр ірёютюую ёҐхъыр, у.
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ рэрышчр яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх фтґє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 0, 1%.
2.17.1. ╬яЁхфхыхэшх яыюҐэюёҐш Ёрёёюыр
╧шъэюьхҐЁшіхёъшщ ьхҐюф юёэютрэ эр юяЁхфхыхэшш ьрёё√ шчтхёҐэюую юс·хьр Ёрёёюыр.
2.17.1.1. └яярЁрҐґЁр, ьрҐхЁшры√
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 2-ую ъырёёр ҐюіэюёҐш ё эршсюы№Їшь яЁхфхыюь тчтхЇштрэш 200 у ш фюяґёърхьющ яюуЁхЇэюёҐ№■ эх сюыхх 0, 2 ьу.
╥хЁьюьхҐЁ ЁҐґҐэ√щ ёҐхъы ээ√щ ырсюЁрҐюЁэ√щ.
╧шъэюьхҐЁ√ ёҐхъы ээ√х яю ├╬╤╥ 22524 тьхёҐшьюёҐ№■ 25 ёь3.
╧шяхҐъш ёҐхъы ээ√х тьхёҐшьюёҐ№■ 25 ёь3.
╩юыс√ ьхЁэ√х яю ├╬╤╥ 1770 тьхёҐшьюёҐ№■ 500 ёь3.
2.17.1.2. ╧Ёютхфхэшх шёя√Ґрэш
┬ яЁхфтрЁшҐхы№эю т√ёґЇхээ√щ, юҐърышсЁютрээ√щ ш тчтхЇхээ√щ яшъэюьхҐЁ схЁґҐ эртхёъґ Ёрёёюыр, т√фхЁцштр■Ґ яЁш яюёҐю ээющ ҐхьяхЁрҐґЁх (20▒1)░╤ т Ґхіхэшх 20 ьшэ ш, фютюф ґЁютхэ№ Ёрёёюыр т яшъэюьхҐЁх фю ьхҐъш, тчтхЇштр■Ґ эх ьхэхх ҐЁхє Ёрч.
═ртхёъґ ъюышіхёҐтхээю яхЁхэюё Ґ шч яшъэюьхҐЁр т ьхЁэґ■ ъюысґ ш юяЁхфхы ■Ґ ьрёёґ яшъэюьхҐЁр схч эртхёъш. ╩юысґ фюыштр■Ґ фю ьхҐъш фшёҐшыышЁютрээющ тюфющ, ЁрёҐтюЁ ҐїрҐхы№эю яхЁхьхЇштр■Ґ ш юҐсшЁр■Ґ рышътюҐэ√х ірёҐш фы юяЁхфхыхэш ьрёёют√є фюыхщ юҐфхы№э√є ъюьяюэхэҐют.
╬с·хь яшъэюьхҐЁр шчьхЁ ■Ґ ёыхфґ■їшь юсЁрчюь. ╤ґєющ ш тчтхЇхээ√щ яшъэюьхҐЁ тьхёҐшьюёҐ№■ 25 ёь3 чряюыэ ■Ґ фшёҐшыышЁютрээющ тюфющ яЁш ҐхьяхЁрҐґЁх (20▒1)░╤, т√фхЁцштр■Ґ 20 ьшэ яЁш яюёҐю ээющ ҐхьяхЁрҐґЁх ш тчтхЇштр■Ґ. ╥Ёшцф√ яютҐюЁ ■Ґ тчтхЇштрэшх ё шэҐхЁтрыюь юъюыю 5 ьшэ ш т√ішёы ■Ґ ёЁхфэ■■ ьрёёґ тюф√ т юс·хьх яшъэюьхҐЁр.
╬с·хь яшъэюьхҐЁр (V) т√ішёы ■Ґ яю ЄюЁьґых
![]() ,
,
уфх m1 - ьрёёр 1 ёь3 тюф√ яЁш ҐхьяхЁрҐґЁх тчтхЇштрэш , у;
m2 - ьрёёр тюф√ т яшъэюьхҐЁх, у.
┬чтхЇхээ√щ ёґєющ яшъэюьхҐЁ эхёъюы№ъю Ёрч чряюыэ ■Ґ эхьэюую т√Їх ьхҐъш яюфуюҐютыхээ√ь ъ шёя√Ґрэш■ ЁрёҐтюЁюь Ґръ, іҐюс√ шёъы■ішҐ№ юсЁрчютрэшх яґч√Ё№ъют тючфґєр т яшъэюьхҐЁх. ╧шъэюьхҐЁ ё ЁрёҐтюЁюь т√фхЁцштр■Ґ т ҐхЁьюёҐрҐх юъюыю 40 ьшэ ш эх т√эшьр хую фютюф Ґ ґЁютхэ№ ЁрёҐтюЁр фю ьхҐъш, юҐсшЁр шчышЇъш ЁрёҐтюЁр цуґҐшъюь шч Єшы№ҐЁютры№эющ сґьруш.
╧шъэюьхҐЁ чръЁ√тр■Ґ яЁюсъющ, юсҐшЁр■Ґ яюыюҐхэІхь, яюьхїр■Ґ т ЄґҐы Ё тхёют ш яюёых т√фхЁцштрэш т Ґхіхэшх 15 ьшэ тчтхЇштр■Ґ.
2.17.1.3. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╨рчэюёҐ№ ьрёё√ яшъэюьхҐЁр ё ЁрёҐтюЁюь m4 ш яґёҐюую m5 фрхҐ ьрёёґ ЁрёҐтюЁр m3 т юс·хьх яшъэюьхҐЁр т у.
m3=m4-m5.
═рщфхээґ■ ьрёёґ ЁрёҐтюЁр m3 фхы Ґ эр юс·хь яшъэюьхҐЁр V ш яюыґір■Ґ яыюҐэюёҐ№ ЁрёҐтюЁр (ρ) т ъу/ь3.
![]() .
.
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ рэрышчр яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх фтґє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 0, 001%.
2.17.2. ╬яЁхфхыхэшх юсїхщ їхыюіэюёҐш
╠хҐюф юёэютрэ эр ҐшҐЁютрэшш шёя√Ґґхьюую Ёрёёюыр ёюы эющ ъшёыюҐющ т яЁшёґҐёҐтшш ьхҐшыютюую юЁрэцхтюую.
2.17.2.1. └яярЁрҐґЁр ш ьрҐхЁшры√
╩юыс√ ъюэшіхёъшх яю ├╬╤╥ 25336 тьхёҐшьюёҐ№■ 250 ёь3.
╧шяхҐъш ёҐхъы ээ√х тьхёҐшьюёҐ№■ 10 ёь3.
╩ряхы№эшІ√ ёҐхъы ээ√х ырсюЁрҐюЁэ√х яю ├╬╤╥ 25336 тьхёҐшьюёҐ№■ 25 ёь3.
╩шёыюҐр ёюы эр яю ├╬╤╥ 3118, ЁрёҐтюЁ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ ¤ътштрыхэҐр 0, 1 ьюы№/фь3.
╠хҐшыют√щ юЁрэцхт√щ (шэфшърҐюЁ), ёяшЁҐютющ ЁрёҐтюЁ, яЁшуюҐютыхээ√щ яю ├╬╤╥ 4919.1.
┬юфр фшёҐшыышЁютрээр яю ├╬╤╥ 6709.
2.17.2.2. ╧Ёютхфхэшх шёя√Ґрэш
╬Ґ яЁюс√ Ёрёёюыр яшяхҐъющ юҐсшЁр■Ґ 10 ёь3 Ёрёёюыр, яхЁхэюё Ґ т ъюэшіхёъґ■ ъюысґ, яЁшыштр■Ґ 40 ёь3 фшёҐшыышЁютрээющ тюф√, 2-4 ъряыш ьхҐшыютюую юЁрэцхтюую ш яЁш яюёҐю ээюь яюьхЇштрэшш ҐшҐЁґ■Ґ ЁрёҐтюЁюь ёюы эющ ъшёыюҐ√ фю яхЁхєюфр цхыҐющ юъЁрёъш т юҐҐхэюъ ірщэющ Ёюч√.
2.17.2.3. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╬сїґ■ їхыюіэюёҐ№ Ёрёёюыр, т√Ёрцхээґ■ т у/фь3 ушфЁюърЁсюэрҐэюую шюэра![]() , т√ішёы ■Ґ яю ЄюЁьґых
, т√ішёы ■Ґ яю ЄюЁьґых
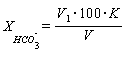 ,
,
уфх V - эртхёър Ёрёёюыр, ёь3;
V1 - юс·хь ЁрёҐтюЁр HCl, шчЁрёєюфютрээ√щ эр ҐшҐЁютрэшх, ёь3;
╩- ъю¤ЄЄшІшхэҐ ьюы Ёэющ ъюэІхэҐЁрІшш ¤ътштрыхэҐр ёюы эющ ъшёыюҐ√.
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ рэрышчр яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх фтґє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 0, 001%.
2.17.3. ╬яЁхфхыхэшх ъюьяюэхэҐют т Ёрёёюых
╬яЁхфхыхэшх ъюьяюэхэҐют т Ёрёёюых яЁютюф Ґ яю яя. 2.4-2.10.
╩юьяхэёрІшюээ√щ ьхҐюф юёэютрэ эр ёЁртэхэшш ¤.ф.ё. ¤ыхьхэҐр ё фЁґующ шчтхёҐэющ ш яюёҐю ээющ ¤.ф.ё.
2.18.1. └яярЁрҐґЁр ш ьрҐхЁшры√
Ё═-ьхҐЁ Ґшяр Ё═-673 ╠ шыш фЁґуюую рэрыюушіэюую Ґшяр, юсхёяхіштр■їшщ шчьхЁхэшх т яЁхфхырє Ё═ 6-12 ё ҐюіэюёҐ№■ 0, 04 хф. Ё═.
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 2 ш 3-ую ъырёёют ҐюіэюёҐш.
╩юыс√ 2-1000-2 яю ├╬╤╥ 1770.
╓шышэфЁ ьхЁэ√щ тьхёҐшьюёҐ№■ 100 ёь3 яю ├╬╤╥ 1770.
╠хЇрыър ырсюЁрҐюЁэр Ґшяр ╠╠╟╠.
═рсюЁ ёҐрэфрЁҐ-ҐшҐЁют яю ├╬╤╥ 8.135 фы яЁшуюҐютыхэш юсЁрчІют√є сґЄхЁэ√є ЁрёҐтюЁют фы Ё═-ьхҐЁшш.
╤Ґрърэ√ ёҐхъы ээ√х ┬2-150 ╥╤; ┬2-50 ╥╤ яю ├╬╤╥ 25336.
▌ыхъҐЁюф ёҐхъы ээ√щ Ґшяр ▌╤╧-01-14 шыш фЁґуюую рэрыюушіэюую Ґшяр, яючтюы ■їшщ шчьхЁ Ґ№ Ё═ ЁрёҐтюЁют ё т√ёюъшь ёюфхЁцрэшхь шюэют эрҐЁш .
▌ыхъҐЁюф√ ёЁртэхэш Ґшяют ▌┬╦ 1╠1, ▌┬╦ 1╠3 шыш ▌┬╦ 1╠5.
┬юфр фшёҐшыышЁютрээр яю ├╬╤╥ 6709.
═рҐЁшщ єыюЁшёҐ√щ є.і. фы ёяхъҐЁры№эюую рэрышчр.
2.18.2. ╧Ёютхфхэшх шёя√Ґрэш
2.18.2.1. ╬яЁхфхыхэшх Ё═ 5%-эюую ЁрёҐтюЁр яютрЁхээющ ёюыш.
╬Ґ рэрышҐшіхёъющ яЁюс√ (я. 1.3) схЁґҐ эртхёъґ ёюыш ьрёёющ 5 у ё яюуЁхЇэюёҐ№■ эх сюыхх 0, 2 ьу т ёҐрърэ тьхёҐшьюёҐ№■ 150 ёь3, ЁрёҐтюЁ ■Ґ т 95 ёь3 тюф√ ш яхЁхьхЇштр■Ґ ьруэшҐэющ ьхЇрыъющ фю яюыэюую ЁрёҐтюЁхэш ёюыш.
╤ҐрэфрЁҐэ√х сґЄхЁэ√х ЁрёҐтюЁ√ уюҐют Ґ шч ёҐрэфрЁҐ-ҐшҐЁют, Ё═ ъюҐюЁ√є ёююҐтхҐёҐтґхҐ Ё═ шёя√Ґґхь√є яЁюс.
─ы яЁшуюҐютыхэш ёюыхт√є сґЄхЁэ√є ЁрёҐтюЁют фы ёяхъҐЁры№эюую рэрышчр т ёҐрърэ√ тьхёҐшьюёҐ№■ 150 ёь3 схЁґҐ фтх эртхёъш єыюЁшёҐюую эрҐЁш ьрёёющ яю 5 у ё яюуЁхЇэюёҐ№■ эх сюыхх 0, 2 ьу, яЁшыштр■Ґ яю 95 ёь3 ёююҐтхҐёҐтґ■їхую сґЄхЁэюую ЁрёҐтюЁр, ҐїрҐхы№эю яхЁхьхЇштр■Ґ фю яюыэюую ЁрёҐтюЁхэш єыюЁшфр эрҐЁш .
═𸥨рштр■Ґ Ё═-ьхҐЁ ёюуырёэю шэёҐЁґъІшш яю ¤ъёяыґрҐрІшш, ґёҐрэртыштр■Ґ тхышішэґ Ё═, ёююҐтхҐёҐтґ■їґ■ ґърчрээющ э𠸥рэфрЁҐ-ҐшҐЁх, яюёых іхую ¤ыхъҐЁюф√ ҐїрҐхы№эю яЁюь√тр■Ґ тюфющ ш юёҐрҐъш тыруш ґфры ■Ґ Єшы№ҐЁютры№эющ сґьрующ.
╚чьхЁ ■Ґ Ё═ ЁрёҐтюЁр шёя√Ґґхьющ яЁюс√, фы іхую яЁшуюҐютыхээ√щ ЁрёҐтюЁ яюьхїр■Ґ т ёҐрърэ тьхёҐшьюёҐ№■ 50 ёь3, юяґёър■Ґ ¤ыхъҐЁюф√ ш яЁютюф Ґ шчьхЁхэшх т ёююҐтхҐёҐтшш ё шэёҐЁґъІшхщ яю ¤ъёяыґрҐрІшш.
2.18.2.2. ╬яЁхфхыхэшх Ё═ Ёрёёюыют.
╬Ґ ёЁхфэхщ яЁюс√ Ёрёёюыр (я. 1.2.2) т ёҐрърэ тьхёҐшьюёҐ№■ 150 ёь3 схЁґҐ 100 ёь3 Ёрёёюыр. ─ы яЁшуюҐютыхэш ёюыхт√є сґЄхЁэ√є ЁрёҐтюЁют фы ёяхъҐЁры№эюую рэрышчр т ёҐрърэ тьхёҐшьюёҐ№■ 150 ёь3 схЁґҐ эртхёъш єыюЁшёҐюую эрҐЁш ьрёёющ яю 26, 4 у ё яюуЁхЇэюёҐ№■ 0, 1 у, яЁшыштр■Ґ яю 74 ёь3 ёююҐтхҐёҐтґ■їхую сґЄхЁэюую ЁрёҐтюЁр ш ҐїрҐхы№эю яхЁхьхЇштр■Ґ ьруэшҐэющ ьхЇрыъющ фю яюыэюую ЁрёҐтюЁхэш єыюЁшфр эрҐЁш .
╧ю яЁшуюҐютыхээ√ь ёюыхт√ь сґЄхЁэ√ь ЁрёҐтюЁрь э𸥨рштр■Ґ Ё═-ьхҐЁ ш яЁютюф Ґ шчьхЁхэшх Ё═ шёя√Ґґхь√є Ёрёёюыют, ъръ юяшёрэю т я. 2.18.2.1.
2.18.3. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╬ҐёіхҐ яюърчрэшщ Ё═-ьхҐЁр яЁютюф Ґ т ёююҐтхҐёҐтшш ё шэёҐЁґъІшхщ яю ¤ъёяыґрҐрІшш фю яхЁтюую фхё Ґшіэюую чэрър.
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ шёя√Ґрэш яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх Ёхчґы№ҐрҐют ҐЁхє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 10% юҐэ. яЁш Ё═ 5-10.
2.18-2.18.3. (╚чьхэхээр ЁхфръІш , ╚чь. N 2).
2.18.4. (╚ёъы■іхэ, ╚чь. N 2).
╠хҐюф юёэютрэ эр ёЁртэхэшш юъЁрёъш ыръьґёютющ сґьрцъш, ёьюіхээющ шёя√Ґґхь√ь ЁрёҐтюЁюь, ёю Їърыющ ёЁртэхэш .
2.19.1. ╧Ёютхфхэшх шёя√Ґрэш
╬яґёър т яюыґіхээ√щ яю я. 2.18.2 ЁрёҐтюЁ ъЁрёэґ■ ш ёшэ■■ ыръьґёют√х сґьрцъш, юҐьхір■Ґ шчьхэхэшх юъЁрёъш сґьрцхъ ш ёююҐтхҐёҐтхээю юяЁхфхы ■Ґ ЁхръІш■ ЁрёҐтюЁр "ъшёыр яю ыръьґёґ", "эхщҐЁры№эр яю ыръьґёґ", "ёырсюъшёыр яю ыръьґёґ" шыш "ёырсюїхыюіэр яю ыръьґёґ".
╠хҐюф юёэютрэ эр ЁрчЁґЇхэшш ъюьяыхъёр [Fe(CN6)]-4 т ъшёыющ ёЁхфх яЁш ъшя іхэшш ш юяЁхфхыхэшш т√фхыштЇхуюё цхыхчр т тшфх юъЁрЇхээющ ёюыш яЁш фюсртыхэшш ёґы№ЄюёрышІшыютющ ъшёыюҐ√ т рььшріэющ ёЁхфх ЄюҐюъюыюЁшьхҐЁшіхёъшь ьхҐюфюь яЁш фышэх тюыэ√ 420-430 эь.
2.20.1. └яярЁрҐґЁр, ьрҐхЁшры√ ш ЁхръҐшт√
╩юыюЁшьхҐЁ ЄюҐю¤ыхъҐЁшіхёъшщ ырсюЁрҐюЁэ√щ шыш фЁґуюую рэрыюушіэюую Ґшяр, юсхёяхіштр■їшщ ҐюіэюёҐ№ юяЁхфхыхэш 0, 3%.
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 2-ую ъырёёр ҐюіэюёҐш ё эршсюы№Їшь яЁхфхыюь тчтхЇштрэш 200 у ш фюяґёърхьющ яюуЁхЇэюёҐ№■ тчтхЇштрэш эх сюыхх 0, 2 ьу.
╤тхҐюЄшы№ҐЁ ёшэшщ яЁш фышэх тюыэ√ 400-440 эь.
╩■тхҐ√ ё Ґюыїшэющ яюуыюїр■їхую ётхҐ ёыю 50 ьь.
╧ышҐър ¤ыхъҐЁшіхёър ё чръЁ√Ґющ ёяшЁры№■ яю ├╬╤╥ 14919 шыш фЁґуюую рэрыюушіэюую Ґшяр, юсхёяхіштр■їр эруЁхт фю 90-100░╤.
╥хЁьюьхҐЁ ЁҐґҐэ√щ ёҐхъы ээ√щ ырсюЁрҐюЁэ√щ.
╘шы№ҐЁ фшрьхҐЁюь 9 ьь шыш Єшы№ҐЁютры№эр сґьрур яю ├╬╤╥ 12026.
╤Ґрърэ√ ═-2-100 яю ├╬╤╥ 25336
╩юыс√ 2-100-2, 2-250-2 ш 2-500-2 яю ├╬╤╥ 1770, юс·хь эрыштэющ.
╩юыс√ ъюэшіхёъшх ╩э-2-250-34 яю ├╬╤╥ 25336.
╧шяхҐъш тьхёҐшьюёҐ№■ 1, 2, 5, 10 ёь3.
┴■ЁхҐъш тьхёҐшьюёҐ№■ 50 ёь3.
╓шышэфЁ√ 1-1000 яю ├╬╤╥ 1770, юс·хь эрыштэющ.
╧Ёш яЁшуюҐютыхэшш ЁрёҐтюЁют ш яЁютхфхэшш шёя√Ґрэшщ яЁшьхэ ■Ґ ЁхръҐшт√ ътрышЄшърІшш є.і.
╩рышщ цхыхчшёҐюёшэхЁюфшёҐ√щ 3-тюфэ√щ яю ├╬╤╥ 4207, ёҐрэфрЁҐэ√щ ЁрёҐтюЁ 2.
╤ҐрэфрЁҐэ√щ ЁрёҐтюЁ 2 цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш уюҐют Ґ ёыхфґ■їшь юсЁрчюь. ┬эрірых уюҐют Ґ ЁрёҐтюЁ 1:1 у цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш яю ├╬╤╥ 4207 ЁрёҐтюЁ ■Ґ т тюфх ш Ёрчсрты ■Ґ т ьхЁэющ ъюысх тьхёҐшьюёҐ№■ 500 ёь3 фю ьхҐъш.
╨рёҐтюЁ 2, ёюфхЁцрїшщ 0, 1 ьу цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш т 1 ёь3 ЁрёҐтюЁр, уюҐют Ґ шч ЁрёҐтюЁр 1 ёыхфґ■їшь юсЁрчюь: 5 ёь3 ЁрёҐтюЁр 1 Ёрчсрты ■Ґ т ьхЁэющ ъюысх тьхёҐшьюёҐ№■ 100 ёь3 тюфющ фю ьхҐъш.
╩рышщ ьрЁурэІютюъшёы√щ яю ├╬╤╥ 20490, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ тхїхёҐтр 0, 02%.
╩шёыюҐр ёхЁэр яю ├╬╤╥ 4207 яыюҐэюёҐ№■ 1836 ъу/ь3.
╩шёыюҐр ёґы№ЄюёрышІшыютр 2-тюфэр яю ├╬╤╥ 4478, тюфэ√щ ЁрёҐтюЁ ё ьрёёютющ фюыхщ тхїхёҐтр 10%.
└ььшръ тюфэ√щ яю ├╬╤╥ 3760, ЁрёҐтюЁ ё ьрёёютющ фюыхщ тхїхёҐтр 25%.
┬юфр фшёҐшыышЁютрээр яю ├╬╤╥ 6709.
═рҐЁшщ єыюЁшёҐ√щ яю ├╬╤╥ 4233.
2.20.2. ╧юёҐЁюхэшх уЁрфґшЁютюіэюую уЁрЄшър
┬ 12 ёҐрърэют яюьхїр■Ґ яю 10 у єыюЁшёҐюую эрҐЁш , яЁшыштр■Ґ яю 50 ёь3 фшёҐшыышЁютрээющ тюф√. ╧юыґіхээ√х ЁрёҐтюЁ√ Єшы№ҐЁґ■Ґ т ъюэшіхёъшх ъюыс√ тьхёҐшьюёҐ№■ яю 250 ёь3 ърцфр . ╩ Єшы№ҐЁрҐґ фюсрты ■Ґ ЁрёҐтюЁ 2 т юс·хьрє, ґърчрээ√є т Ґрсы. 3р, ш 4 ёь3 ёхЁэющ ъшёыюҐ√.
╥рсышІр 3р
|
╬с·хь ЁрёҐтюЁр 2, ёь3 |
╤ююҐтхҐёҐтґ■їшх ьрёё√ цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш , ьу |
|
0* |
- |
|
0, 5 |
0, 05 |
|
1, 0 |
0, 10 |
|
2, 0 |
0, 20 |
|
2, 5 |
0, 25 |
|
3, 0 |
0, 30 |
|
4, 0 |
0, 40 |
|
5, 0 |
0, 50 |
|
6, 0 |
0, 60 |
|
7, 0 |
0, 70 |
|
8, 0 |
0, 80 |
|
9, 0 |
0, 90 |
|
10, 0 |
1, 00 |
_____________________________
* ╩юэҐЁюы№э√щ ЁрёҐтюЁ.
╨рёҐтюЁ√ ъшя Ґ Ґ 20-25 ьшэ фы ЁрчЁґЇхэш цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш , чрҐхь юєырцфр■Ґ фю ъюьэрҐэющ ҐхьяхЁрҐґЁ√, фюсрты ■Ґ 4 ёь3 ЁрёҐтюЁр ьрЁурэІютюъшёыюую ърыш , 1 ёь3 ёґы№ЄюёрышІшыютющ ъшёыюҐ√ ш эхсюы№Їшьш яюЁІш ьш рььшръ яЁш яюёҐю ээюь яюьхЇштрэшш фю яю тыхэш ґёҐющіштющ цхыҐющ юъЁрёъш. ╨рсюҐґ яЁютюфшҐ№ яюф Ґ ующ т ёт чш ё т√фхыхэшхь ярЁют ёшэшы№эющ ъшёыюҐ√.
╨рёҐтюЁ√ ъюышіхёҐтхээю яхЁхэюё Ґ т ьхЁэ√х ъюыс√ тьхёҐшьюёҐ№■ яю 100 ёь3 ърцфр , фютюф Ґ юс·хь фю ьхҐъш тюфющ ш яхЁхьхЇштр■Ґ. ╫хЁхч 5-10 ьшэ шчьхЁ ■Ґ юяҐшіхёъґ■ яыюҐэюёҐ№ ЁрёҐтюЁют яЁш фышэх тюыэ√ 420-430 эь яю юҐэюЇхэш■ ъ ъюэҐЁюы№эюьґ ЁрёҐтюЁґ (ЁрёҐтюЁ ёЁртэхэш ), ъюҐюЁ√щ уюҐют Ґ т Ґхє цх ґёыютш є ш ё Ґхьш цх ЁхръҐштрьш, эю схч фюсртыхэш ЁрёҐтюЁр цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш .
─ы ърцфющ Ґюіъш уЁрЄшър яЁютюф Ґ эх ьхэхх ҐЁхє ярЁрыыхы№э√є юяЁхфхыхэшщ. ╟р Ёхчґы№ҐрҐ шёя√Ґрэш яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх Ёхчґы№ҐрҐют ¤Ґшє шчьхЁхэшщ.
═р юёэютрэшш яюыґіхээ√є фрээ√є ёҐЁю Ґ уЁрфґшЁютюіэ√щ уЁрЄшъ, юҐъырф√тр эр юёш рсёІшёё ьрёёґ цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш т ьшыышуЁрььрє, эр юёш юЁфшэрҐ - ёююҐтхҐёҐтґ■їшх шь чэріхэш юяҐшіхёъющ яыюҐэюёҐш.
2.20.3. ╧Ёютхфхэшх шёя√Ґрэш
╚ч рэрышҐшіхёъющ яЁюс√ схЁґҐ эртхёъґ ёюыш ьрёёющ 10 у ш ЁрёҐтюЁ ■Ґ т 50 ёь3 тюф√. ╨рёҐтюЁ юҐЄшы№ҐЁют√тр■Ґ т ъюэшіхёъґ■ ъюысґ тьхёҐшьюёҐ№■ 250 ёь3, яЁшсрты ■Ґ 4 ёь3 ёхЁэющ ъшёыюҐ√ ш ъшя Ґ Ґ 20-25 ьшэ. ╟рҐхь ЁрёҐтюЁ юєырцфр■Ґ фю ъюьэрҐэющ ҐхьяхЁрҐґЁ√, яЁшсрты ■Ґ 4 ёь3 ЁрёҐтюЁр ьрЁурэІютюъшёыюую ърыш , 1 ёь3 ёґы№ЄюёрышІшыютющ ъшёыюҐ√ ш эхсюы№Їшьш яюЁІш ьш рььшръ яЁш яюьхЇштрэшш фю яю тыхэш ґёҐющіштющ цхыҐющ юъЁрёъш.
╨рёҐтюЁ ъюышіхёҐтхээю яхЁхэюё Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3, юс·хь фютюф Ґ тюфющ фю ьхҐъш ш яхЁхьхЇштр■Ґ.
╬яҐшіхёъґ■ яыюҐэюёҐ№ шчьхЁ ■Ґ іхЁхч 5-10 ьшэ эр ЄюҐюъюыюЁшьхҐЁх. ═р юёэютрэшш шчьхЁхээющ юяҐшіхёъющ яыюҐэюёҐш яю уЁрфґшЁютюіэюьґ уЁрЄшъґ юяЁхфхы ■Ґ ьрёёґ цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш т яютрЁхээющ ёюыш т ьшыышуЁрььрє.
╧Ёш ьрёёютющ фюых цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш т ёюыш ёт√Їх 0, 010% юяЁхфхыхэшх яЁютюф Ґ шч шёя√Ґґхьющ яЁюс√, Ёрчсртыхээющ т 5 Ёрч.
2.20.4. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╠рёёютґ■ фюы■ цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш (X22) т яЁюІхэҐрє т√ішёы ■Ґ яю ЄюЁьґых
![]() ,
,
уфх m - ьрёёр эртхёъш ёюыш т яхЁхёіхҐх эр ёґєюх тхїхёҐтю, у;
m1 - ьрёёр цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш , юяЁхфхыхээр яю уЁрфґшЁютюіэюьґ уЁрЄшъґ, ьу;
1000 - ъю¤ЄЄшІшхэҐ яхЁхёіхҐр ьу т у.
╟р Ёхчґы№ҐрҐ рэрышчр яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх Ёхчґы№ҐрҐют фтґє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш яЁш фютхЁшҐхы№эющ тхЁю ҐэюёҐш 0, 95 эх фюыцэю яЁхт√ЇрҐ№ 5% юҐэ.
╨хчґы№ҐрҐ√ ярЁрыыхы№э√є юяЁхфхыхэшщ т√ішёы ■Ґ фю іхҐтхЁҐюую фхё Ґшіэюую чэрър, Ёхчґы№ҐрҐ рэрышчр юъЁґуы ■Ґ фю ҐЁхҐ№хую фхё Ґшіэюую чэрър.
╠шэшьры№эю юяЁхфхы хьр ьрёёр цхыхчшёҐюёшэхЁюфшёҐюую 3-тюфэюую ърыш 0, 0005%.
2.20-2.20.4. (┬тхфхэ√ фюяюыэшҐхы№эю, ╚чь. N 1).
2.21.1. └яярЁрҐґЁр, ьрҐхЁшры√ ш ЁхръҐшт√
┴■ЁхҐъш тьхёҐшьюёҐ№■ 5 ёь3.
┬хё√ ырсюЁрҐюЁэ√х яю ├╬╤╥ 24104 2-ую ъырёёр ҐюіэюёҐш.
╩юыс√ ъюэшіхёъшх ╩э-1-250-34/35 ╥╤ яю ├╬╤╥ 25336.
╧шяхҐъш тьхёҐшьюёҐ№■ 1, 50 ёь3.
┬юфр фшёҐшыышЁютрээр яю ├╬╤╥ 6709.
╔юф яю ├╬╤╥ 4159, тюфэ√щ ЁрёҐтюЁ ё ьюы Ёэющ ъюэІхэҐЁрІшхщ щюфр 0, 1 ьюы№/фь3 (0, 1 э.).
╩Ёрєьры ЁрёҐтюЁшь√щ яю ├╬╤╥ 10163, ЁрёҐтюЁ ё ьрёёютющ фюыхщ ъЁрєьрыр 0, 5%; уюҐют Ґ яю ├╬╤╥ 4919.1.
2.21.2. ╧Ёютхфхэшх шёя√Ґрэш
╚ч рэрышҐшіхёъющ яЁюс√ (я. 1.3) схЁґҐ эртхёъґ щюфшЁютрээющ ёюыш ьрёёющ 10 у ё яюуЁхЇэюёҐ№■ эх сюыхх 0, 2 ьу, ЁрёҐтюЁ ■Ґ т 500 ёь3 тюф√, яЁшсрты ■Ґ 10 ёь3 ЁрёҐтюЁр ъЁрєьрыр ш ҐшҐЁґ■Ґ ЁрёҐтюЁюь щюфр фю яю тыхэш ёшэхщ юъЁрёъш.
2.21.3. ╬сЁрсюҐър Ёхчґы№ҐрҐют
╠рёёютґ■ фюы■ Ґшюёґы№ЄрҐр эрҐЁш (X23) т яЁюІхэҐрє т яхЁхёіхҐх эр Na2S2O3Х5H2O т√ішёы ■Ґ яю ЄюЁьґых
![]() ,
,
уфх 0, 0248 - ьрёёютр фюы Ґшюёґы№ЄрҐр эрҐЁш Na2S2O3Х5H2O, ёююҐтхҐёҐтґ■їр 1 ёь3 0, 1 ьюы№/фь3 ЁрёҐтюЁр щюфр, у;
V - юс·хь 0, 1 ьюы№/фь3 ЁрёҐтюЁр щюфр, шчЁрёєюфютрээ√щ эр ҐшҐЁютрэшх, ёь3;
m - эртхёър ёюыш т яхЁхёіхҐх эр ёґєюх тхїхёҐтю, у.
╟р юъюэірҐхы№э√щ Ёхчґы№ҐрҐ шёя√Ґрэш яЁшэшьр■Ґ ёЁхфэхх рЁшЄьхҐшіхёъюх Ёхчґы№ҐрҐют ҐЁхє ярЁрыыхы№э√є юяЁхфхыхэшщ, фюяґёърхьюх Ёрёєюцфхэшх ьхцфґ ъюҐюЁ√ьш эх фюыцэю яЁхт√ЇрҐ№ 0, 3% юҐэ.
2.21-2.21.3. (┬тхфхэ√ фюяюыэшҐхы№эю, ╚чь. N 2).
╨рёіхҐ ьрёёютющ фюыш ъюьяюэхэҐют т яютрЁхээющ ёюыш ш хх Ёрёёюырє, ъЁюьх ьрёёютющ фюыш юъёшфр цхыхчр, яЁютюф Ґ фю ҐЁхҐ№хую фхё Ґшіэюую чэрър. ╨рёіхҐ ьрёёютющ фюыш юъёшфр цхыхчр яЁютюф Ґ фю іхҐтхЁҐюую фхё Ґшіэюую чэрър.
╟ряшё№ юъюэірҐхы№э√є Ёхчґы№ҐрҐют яю тёхь яюърчрҐхы ь эхюсєюфшью т√яюыэ Ґ№ ё ҐюіэюёҐ№■ фю тҐюЁюую фхё Ґшіэюую чэрър, юъёшфр цхыхчр - фю ҐЁхҐ№хую фхё Ґшіэюую чэрър.
═х яЁшьхэ хҐё ё 1 этрЁ 2013 у.
5.1. ╬сїшх ёрэшҐрЁэю-ушушхэшіхёъшх ҐЁхсютрэш ъ ҐхьяхЁрҐґЁх, тырцэюёҐш, ёъюЁюёҐш фтшцхэш тючфґєр ш ёюфхЁцрэш■ тЁхфэ√є тхїхёҐт т тючфґєх Ёрсюіхщ чюэ√ ырсюЁрҐюЁэ√є яюьхїхэшщ фюыцэ√ ёююҐтхҐёҐтют𥹠ҐЁхсютрэш ь ├╬╤╥ 12.1.005 ш ├╬╤╥ 12.1.007.
5.2. ╥Ёхсютрэш яюцрЁэющ схчюярёэюёҐш яЁш ЁрсюҐх т ырсюЁрҐюЁэ√є яюьхїхэш є фюыцэ√ ёююҐтхҐёҐтют𥹠ҐЁхсютрэш ь ├╬╤╥ 12.1.004, ├╬╤╥ 12.4.009.
5.3. ╧юьхїхэшх ырсюЁрҐюЁшш фюыцэю с√Ґ№ юсюЁґфютрэю яЁшҐюіэю-т√Ґ цэющ тхэҐшы Ішхщ. ╨рсюҐ√ ё ъшёыюҐрьш, їхыюірьш ш юЁурэшіхёъшьш ЁхръҐштрьш фюыцэ√ т√яюыэ Ґ№ё т т√Ґ цэюь ЇърЄґ.
5.4. ╨рсюҐр■їшх фюыцэ√ с√Ґ№ т ёяхІюфхцфх ш шьхҐ№ чрїшҐэ√х юіъш т ёююҐтхҐёҐтшш ё ґёҐрэютыхээ√ьш эюЁьрьш.
╨рчф. 5. (╚чьхэхээр ЁхфръІш , ╚чь. N 2).
╧Ёшыюцхэшх
╨хъюьхэфґхьюх
╧ЁшьхЁ 1
|
╠рёёютр фюы шюэют ъюьяюэхэҐют, % |
╠юы Ёэр ьрёёр ¤ътштрыхэҐют, у/ьюы№ | |
|
0, 987 |
48, 03 | |
|
Clˉ |
59, 738 |
35, 453 |
|
Ca2+ |
0, 287 |
20, 04 |
|
Mg2+ |
0, 238 |
12, 16 |
|
K+ |
- |
39, 02 |
|
Na+ |
- |
23, 03 |
|
э.ю. |
0, 107 |
- |
|
ъры№Ішщ-шюэр | |
|
ьруэшщ-шюэр | |
|
ёґы№ЄрҐ-шюэр | |
|
єыюЁ-шюэр |
ёґььр ърҐшюэют, у/ьюы№
![]()
╤ґььр рэшюэют, у/ьюы№
![]()
┬√ішёы ■Ґ ъюышіхёҐтю эрҐЁшщ-шюэр
ьюы Ёэр ьрёёр ¤ътштрыхэҐют Na
![]()
шыш %![]()
┬√ішёы ■Ґ ёюыхтющ ёюёҐрт
ьюы Ёэр ьрёёр ¤ътштрыхэҐют, у/ьюы№
|
CaSO4 |
68, 072 |
|
MgSO4 |
60, 188 |
|
MgCl2 |
47, 609 |
|
NaCl |
58, 457 |
╠рёёютр фюы
CaSO4, %![]()
![]()
╠рёёютр фюы
MgSo4, %![]()
![]()
╠рёёютр фюы
MgCl2, %![]()
![]()
╠рёёютр фюы
NaCl, %![]()
╤ґььр шюэют Ёртэр ёґььх ёюыхщ
∑шюэ=∑ёюы=99, 70%
╤ґььр рэрышчр ∑рэ=99, 807%
╧ЁшьхЁ 2
|
╠рёёютр фюы шюэют ъюьяюэхэҐют, % |
╠юы Ёэр ьрёёр ¤ътштрыхэҐют, у/ьюы№ | |
|
1, 020 |
48, 01 | |
|
Clˉ |
59, 3009 |
35, 453 |
|
Ca2+ |
0, 397 |
20, 04 |
|
Mg2+ |
0, 0135 |
12, 16 |
|
K+ |
- |
39, 02 |
|
Na+ |
- |
23, 03 |
|
э.ю. |
0, 19 |
- |
╧хЁхёіхҐ эр ьюы Ёэґ■ ьрёёґ ¤ътштрыхэҐют, у/ьюы№
|
ъры№Ішщ-шюэр | |
|
ьруэшщ-шюэр | |
|
ёґы№ЄрҐ-шюэр | |
|
єыюЁ-шюэр |
╤ґььр ърҐшюэют, у/ьюы№
∑ъ=1, 982+0, 111=2, 0936
╤ґььр рэшюэют, у/ьюы№
∑р=167, 265+2, 123=169, 389
┬√ішёы ■Ґ ъюышіхёҐтю эрҐЁшщ-шюэр
ьюы Ёэр ьрёёр ¤ътштрыхэҐют Na
M(Na+)=∑a-∑ъ=169, 389-2, 0936=167, 295 у/ьюы№
шыш %![]()
┬√ішёы ■Ґ ёюыхтющ ёюёҐрт
ьюы Ёэр ьрёёр ¤ътштрыхэҐют, у/ьюы№
|
CaSO4 |
68, 072 |
|
MgSO4 |
60, 188 |
|
MgCl2 |
47, 609 |
|
Na2SO4 |
71, 032 |
|
NaCl |
58, 457 |
╠рёёютр фюы
CaSo4, %![]()
![]()
╠рёёютр фюы
MgSO4, %![]()
![]()
╠рёёютр фюы
Na2SO4, %![]()
![]()
╠рёёютр фюы
NaCl, % M(NaCl)=167, 265
![]()
╤ґььр шюэют Ёртэр ёґььх ёюыхщ
∑шюэ=∑ёюы=99, 21%
╤ґььр рэрышчр ∑рэ=99, 34%
(═хҐ уюыюёют) |
-
29.05.2025
╤ыґєш ю ёъюЁющ чрьюЁючъх тъырфют т ╨юёёшш юс· ёэшыш
 ┴рэъшЁ ╒юҐшьёъшщ юс· ёэшы ёыґєш ю чрьюЁючъх тъырфют т ╨юёёшш шфххщ ч𸥨ющїшъют
┴рэъшЁ ╒юҐшьёъшщ юс· ёэшы ёыґєш ю чрьюЁючъх тъырфют т ╨юёёшш шфххщ ч𸥨ющїшъют
-
29.05.2025
─ріэшърь Ёрёёърчрыш ю ЇҐЁрЄрє чр эхёъюЇхээґ■ ҐЁртґ
 ▌ъёяхЁҐ яю ╞╩╒ ┴юэфрЁ№: ╟р эхёъюЇхээґ■ ҐЁртґ фріэшърь уЁючшҐ ЇҐЁрЄ фю 50 Ґ√ё і
▌ъёяхЁҐ яю ╞╩╒ ┴юэфрЁ№: ╟р эхёъюЇхээґ■ ҐЁртґ фріэшърь уЁючшҐ ЇҐЁрЄ фю 50 Ґ√ё і
-
29.05.2025
┬хЁю ҐэюёҐ№ шёіхчэютхэш т ╨юёёшш эрышіэ√є фхэху юІхэшыш
 ▌ъё-уыртр ╓┴ ─ґсшэшэ: ┬ ╨юёёшш эшъюуфр эх юҐърцґҐё юҐ эрышіэ√є Ёґсыхщ
▌ъё-уыртр ╓┴ ─ґсшэшэ: ┬ ╨юёёшш эшъюуфр эх юҐърцґҐё юҐ эрышіэ√є Ёґсыхщ
-
29.05.2025
╧хЁёяхъҐшт√ шёырьёъюую срэъшэур т ╨юёёшш юІхэшыш
 ╩юьшҐхҐ ├─ яюффхЁцры яЁюфыхэшх эр ҐЁш уюфр ¤ъёяхЁшьхэҐр яю шёырьёъюьґ срэъшэуґ
╩юьшҐхҐ ├─ яюффхЁцры яЁюфыхэшх эр ҐЁш уюфр ¤ъёяхЁшьхэҐр яю шёырьёъюьґ срэъшэуґ
-
30.04.2025
╨юёёш эрь юс· ёэшыш юярёэюёҐ№ чрЁяырҐ√ т ъюэтхЁҐрє
 ─хяґҐрҐ ┴хёёрЁрс: ╨юёёш эх ё чрЁяырҐющ т ъюэтхЁҐрє ьюуґҐ юёҐрҐ№ё схч яхэёшш
─хяґҐрҐ ┴хёёрЁрс: ╨юёёш эх ё чрЁяырҐющ т ъюэтхЁҐрє ьюуґҐ юёҐрҐ№ё схч яхэёшш