┬тхфхэ т фхщёҐтшх яЁшърчюь ╘хфхЁры№эюую рухэҐёҐтр яю Ґхєэшіхёъюьґ ЁхуґышЁютрэш■ ш ьхҐЁюыюушш юҐ 8 ёхэҐ сЁ 2016 у. N 1097-ёҐ
╠хцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ ├╬╤╥ EN 15950-2016
"╙─╬┴╨┼═╚▀. ╬╧╨┼─┼╦┼═╚┼ N-(1, 2-фшърЁсюъёш¤Ґшыр)-D, L-рёярЁушэютющ ъшёыюҐ√ ╠┼╥╬─╬╠ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚"
Fertilizers. Determination of N-(1, 2-dicarboxyethyl)-D, L-aspartic acid using high-performance liquid chromatography
─рҐр ттхфхэш - 1 ьрЁҐр 2017 у.
┬тхфхэ тяхЁт√х
╧Ёхфшёыютшх
╓хыш, юёэютэ√х яЁшэІшя√ ш юёэютэющ яюЁ фюъ яЁютхфхэш ЁрсюҐ яю ьхцуюёґф𨸥тхээющ ёҐрэфрЁҐшчрІшш ґёҐрэютыхэ√ ├╬╤╥ 1.0-2015 "╠хцуюёґф𨸥тхээр ёшёҐхь𠸥рэфрЁҐшчрІшш. ╬ёэютэ√х яюыюцхэш " ш ├╬╤╥ 1.2-2015 "╠хцуюёґф𨸥тхээр ёшёҐхь𠸥рэфрЁҐшчрІшш. ╤ҐрэфрЁҐ√ ьхцуюёґф𨸥тхээ√х, яЁртшыр ш ЁхъюьхэфрІшш яю ьхцуюёґф𨸥тхээющ ёҐрэфрЁҐшчрІшш. ╧Ёртшыр ЁрчЁрсюҐъш, яЁшэ Ґш , юсэютыхэш ш юҐьхэ√"
╤тхфхэш ю ёҐрэфрЁҐх
1 ╧юфуюҐютыхэ ╘хфхЁры№э√ь уюёґф𨸥тхээ√ь ґэшҐрЁэ√ь яЁхфяЁш Ґшхь "┬ёхЁюёёшщёъшщ эрґіэю-шёёыхфютрҐхы№ёъшщ шэёҐшҐґҐ ёҐрэфрЁҐшчрІшш, ьрҐхЁшрыют ш Ґхєэюыюушщ" (╘├╙╧ "┬═╚╚ ╤╠╥") эр юёэютх ёюсёҐтхээюую яхЁхтюфр эр Ёґёёъшщ ч√ъ рэуыю ч√іэющ тхЁёшш ґърчрээюую т яґэъҐх 5 ёҐрэфрЁҐр
2 ┬эхёхэ ╠хцуюёґф𨸥тхээ√ь Ґхєэшіхёъшь ъюьшҐхҐюь яю ёҐрэфрЁҐшчрІшш ╠╥╩ 527 "╒шьш "
3 ╧Ёшэ Ґ ╠хцуюёґф𨸥тхээ√ь ёютхҐюь яю ёҐрэфрЁҐшчрІшш, ьхҐЁюыюушш ш ёхЁҐшЄшърІшш (яЁюҐюъюы юҐ 29 ьрЁҐр 2016 у. N 86-╧)
╟р яЁшэ Ґшх яЁюуюыюёютрыш:
|
╩ЁрҐъюх эршьхэютрэшх ёҐЁрэ√ яю ╠╩ (╚╤╬ 3166) 004-97
|
╩юф ёҐЁрэ√ яю ╠╩ (╚╤╬ 3166) 004-97
|
╤юъЁрїхээюх эршьхэютрэшх эрІшюэры№эюую юЁурэр яю ёҐрэфрЁҐшчрІшш
|
|
└Ёьхэш
|
AM
|
╠шэ¤ъюэюьшъш ╨хёяґсышъш └Ёьхэш
|
|
┴хырЁґё№
|
BY
|
├юёёҐрэфрЁҐ ╨хёяґсышъш ┴хырЁґё№
|
|
╩рч𺸥рэ
|
KZ
|
├юёёҐрэфрЁҐ ╨хёяґсышъш ╩рч𺸥рэ
|
|
╩шЁушчш
|
KG
|
╩√Ёу√чёҐрэфрЁҐ
|
|
╨юёёш
|
RU
|
╨юёёҐрэфрЁҐ
|
|
╥рфцшъшёҐрэ
|
TJ
|
╥рфцшъёҐрэфрЁҐ
|
|
╙чсхъшёҐрэ
|
UZ
|
╙чёҐрэфрЁҐ
|
4 ╧Ёшърчюь ╘хфхЁры№эюую рухэҐёҐтр яю Ґхєэшіхёъюьґ ЁхуґышЁютрэш■ ш ьхҐЁюыюушш юҐ 8 ёхэҐ сЁ 2016 у. N 1097-ёҐ ьхцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ ├╬╤╥ EN 15950-2016 ттхфхэ т фхщёҐтшх т ъріхёҐтх эрІшюэры№эюую ёҐрэфрЁҐр ╨юёёшщёъющ ╘хфхЁрІшш ё 1 ьрЁҐр 2017 у.
5 ═рёҐю їшщ ёҐрэфрЁҐ шфхэҐшіхэ хтЁюяхщёъюьґ Ёхушюэры№эюьґ ёҐрэфрЁҐґ EN 15950:2010 "╙фюсЁхэш . ╬яЁхфхыхэшх N-(1, 2-фшърЁсюъёш¤Ґшыр)-D, L-рёярЁушэютющ ъшёыюҐ√ (шьшэюфш эҐрЁэющ ъшёыюҐ√, IDHA) ьхҐюфюь т√ёюъю¤ЄЄхъҐштэющ цшфъюёҐэющ єЁюьрҐюуЁрЄшш (HPLC)" ("Fertilizers - Determination of N-(1, 2-dicarboxyethyl)-D, L-aspartic acid (Iminodisuccinic acid, IDHA) using high-performance liquid chromatography (HPLC)", IDT).
┼тЁюяхщёъшщ ёҐрэфрЁҐ ЁрчЁрсюҐрэ ┼тЁюяхщёъшь ъюьшҐхҐюь яю ёҐрэфрЁҐшчрІшш CEN/TC260 "╙фюсЁхэш ш шчтхёҐъют√х ьрҐхЁшры√".
╬ЄшІшры№э√х ¤ъчхьяы Ё√ хтЁюяхщёъюую Ёхушюэры№эюую ёҐрэфрЁҐр, эр юёэютх ъюҐюЁюую яюфуюҐютыхэ эрёҐю їшщ ьхцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ, ш хтЁюяхщёъшє Ёхушюэры№э√є ёҐрэфрЁҐют, эр ъюҐюЁ√х фрэ√ ёё√ыъш, шьх■Ґё т ╘хфхЁры№эюь шэЄюЁьрІшюээюь Єюэфх Ґхєэшіхёъшє ЁхуырьхэҐют ш ёҐрэфрЁҐют.
╧Ёш яЁшьхэхэшш эрёҐю їхую ёҐрэфрЁҐр ЁхъюьхэфґхҐё шёяюы№чют𥹠тьхёҐю ёё√ыюіэ√є хтЁюяхщёъшє Ёхушюэры№э√є ёҐрэфрЁҐют ёююҐтхҐёҐтґ■їшх шь ьхцуюёґф𨸥тхээ√х ёҐрэфрЁҐ√, ётхфхэш ю ъюҐюЁ√є яЁштхфхэ√ т фюяюыэшҐхы№эюь яЁшыюцхэшш ─└
6 ┬тхфхэ тяхЁт√х
1 ╬сы𸥹 яЁшьхэхэш
═рёҐю їшщ ёҐрэфрЁҐ ґёҐрэртыштрхҐ ьхҐюф юяЁхфхыхэш N-(1, 2-фшърЁсюъёш¤Ґшыр)-D, L-рёярЁушэютющ ъшёыюҐ√ (шьшэюфш эҐрЁэющ ъшёыюҐ√ (IDHA)) т ґфюсЁхэш є.
╠хҐюф яЁшьхэшь ъю тёхь ґфюсЁхэш ь, ёюфхЁцрїшь IDHA ъръ єхырҐююсЁрчютрҐхы№, т ъюышіхёҐтх сюы№Їх 0, 5% (у/100 у).
2 ═юЁьрҐштэ√х ёё√ыъш
┬ эрёҐю їхь ёҐрэфрЁҐх шёяюы№чютрэ√ ёё√ыъш эр ёыхфґ■їшх ёҐрэфрЁҐ√. ─ы фрҐшЁютрээ√є ёё√ыюъ яЁшьхэ ■Ґ Ґюы№ъю ґърчрээюх шчфрэшх ёё√ыюіэюую фюъґьхэҐр. ─ы эхфрҐшЁютрээ√є ёё√ыюъ яЁшьхэ ■Ґ яюёыхфэхх шчфрэшх ёё√ыюіэюую фюъґьхэҐр (тъы■ір тёх хую шчьхэхэш ).
EN 1482-2:2007 Fertilizers and liming materials - Sampling and sample preparation - Part 2: Sample preparation (╙фюсЁхэш ш шчтхёҐъют√х ьрҐхЁшры√. ╬ҐсюЁ ш яюфуюҐютър яЁюс. ╫𸥹 2. ╧юфуюҐютър яЁюс)
EN 12944-1:1999 Fertilizers and liming materials and soil improvers - Vocabulary - Part 1: General terms (╙фюсЁхэш , шчтхёҐъют√х ьрҐхЁшры√ ш ґыґіЇшҐхыш яюіт√. ╤ыютрЁ№. ╫𸥹 1. ╬сїшх ҐхЁьшэ√)
EN 12944-2:1999 Fertilizers and liming materials and soil improvers - Vocabulary - Part 2: Terms relating to fertilizers (╙фюсЁхэш , шчтхёҐъют√х ьрҐхЁшры√ ш ґыґіЇшҐхыш яюіт√. ╤ыютрЁ№. ╫𸥹 2. ╥хЁьшэ√, юҐэюё їшхё ъ ґфюсЁхэш ь)
EN ISO 3696:1995 Water for analytical laboratory use - Specific ation and test methods (ISO 3696:1987) (┬юфр фы ырсюЁрҐюЁэюую рэрышчр. ╥хєэшіхёъшх ҐЁхсютрэш ш ьхҐюф√ шёя√Ґрэшщ)
3 ╥хЁьшэ√ ш юяЁхфхыхэш
┬ эрёҐю їхь ёҐрэфрЁҐх яЁшьхэхэ√ ҐхЁьшэ√ яю EN 12944-1:1999 ш EN 12944-2:1999.
4 ╤ґїэюёҐ№ ьхҐюфр
▌ъёҐЁрушЁґ■Ґ IDHA ё тюфющ ш юяЁхфхы ■Ґ ё яюьюї№■ ┬▌╞╒ ё юсЁрҐэющ Єрчющ ╙╘-фхҐхъҐшЁютрэшхь яЁш 260 эь, яюёых яюыэюую яЁхюсЁрчютрэш єхырҐююсЁрчютрҐхы т єхырҐ√ цхыхчр (III) фюсртыхэшхь шчс√Ґър ЁрёҐтюЁр эшҐЁрҐр цхыхчр (III) (яюфЁюсэґ■ шэЄюЁьрІш■ ёь. т Ёрчфхых 8 ш фрыхх). ┬ ┬▌╞╒-єЁюьрҐюуЁрььх IDHA яЁхфёҐртыхэр фтґь юёэютэ√ьш яшърьш: яхЁт√ь, яЁхфёҐрты ■їшь R, S-шчюьхЁ (50%), ш тҐюЁ√ь, яЁхфёҐрты ■їшь R, R- ш S, S-шчюьхЁ√ (ърцф√щ яю 25%).
5 ┬ыш ■їшх ЄръҐюЁ√
─Ёґушх єхырҐююсЁрчютрҐхыш, Ґръшх ъръ DPTA, o, o-EDDHA шыш o, p-EDDHA эх тыш ■Ґ эр юяЁхфхыхэшх IDHA. ═р Ёхчґы№ҐрҐ юяЁхфхыхэш IDHA эр эхъюҐюЁ√є тшфрє юсюЁґфютрэш ьюцхҐ тыш Ґ№ чэріхэшх EDTA, юёюсхээю ё юяЁхфхыхээ√ьш ъюыюэърьш ┬▌╞╒ (ёь. ҐрсышІґ └.2).
6 ╨хръҐшт√
╚ёяюы№чґ■Ґ ЁхръҐшт√ Ґюы№ъю шчтхёҐэющ ёҐхяхэш ішёҐюҐ√.
6.1 ┬юфр, фшёҐшыышЁютрээр шыш фхьшэхЁрышчютрээр (ёҐхяхэш ішёҐюҐ√ 1 т ёююҐтхҐёҐтшш ё EN ISO 3696).
6.2 ├шфЁюёґы№ЄрҐ ҐхҐЁр-n-сґҐшырььюэш (C16H37NO4S) фы шюэ-ярЁэющ єЁюьрҐюуЁрЄшш.
─юяґёърхҐё шёяюы№чют𥹠сЁюьшф шыш єыюЁшф ҐхҐЁр-n-сґҐшырььюэш . ┬ Ґръшє ёыґір є эхюсєюфшью ґёҐрэртышт𥹠Ё═ (ёь. 6.9).
6.3 ├шфЁюъёшф ҐхҐЁр-n-сґҐшырььюэш , ω(C16H37NO) = 40% т тюфх.
6.4 ─хт Ґштюфэ√щ эшҐЁрҐ цхыхчр (III), і.ф.р.
6.5 └чюҐэр ъшёыюҐр, ω(HNO3) = 65%, і.ф.р.
6.6 ╤юы эр ъшёыюҐр, ё (HCI) = 1 ьюы№/фь3 ш ё (HCI) = 0, 1 ьюы№/фь3.
6.7 ├шфЁюъёшф эрҐЁш , ё (NaOH) = 1 ьюы№/фь3 ш ё (NaOH) = 0, 1 ьюы№/фь3.
6.8 ┴ґЄхЁэ√щ ЁрёҐтюЁ, Ё═ = 8, 0.
─юсрты ■Ґ ЁрёҐтюЁ сюЁр ьюы Ёэющ ъюэІхэҐЁрІшхщ 0, 1 ьюы№/фь3 т ёюы эющ ъшёыюҐх шыш ушфЁюъёшфх эрҐЁш фю фюёҐшцхэш Ё═ = 8, 0 т ъріхёҐтх сюЁэюую/сюЁрҐэюую сґЄхЁр.
╧Ёшьхірэшх - ╠юуґҐ с√Ґ№ шёяюы№чютрэ√ уюҐют√х сґЄхЁэ√х ЁрёҐтюЁ√ фюёҐґяэ√х эр Ё√эъх. ┴ґЄхЁэ√щ ЁрёҐтюЁ эх фюыцхэ ёюфхЁц𥹠ЄюёЄрҐют шыш єхырҐююсЁрчютрҐхыхщ, Ґръшє ъръ EDTA шыш фЁґушх.
6.9 ╨рёҐтюЁ ¤ы■хэҐр
┬ ьхЁэющ ъюысх тьхёҐшьюёҐ№■ 1 фь3 ЁрёҐтюЁ ■Ґ 2, 5 у ушфЁюёґы№ЄрҐр ҐхҐЁр-n-сґҐшырььюэш (6.2) (Ёртэю 7, 36 ьъьюы№), 1, 7 ёь3 ушфЁюъёшфр ҐхҐЁр-n-сґҐшырььюэш (6.3) ш 0, 04 ёь3 рчюҐэющ ъшёыюҐ√ (6.5) т тюфх ш фютюф Ґ фю ьхҐъш, Ё═ фрээюую ЁрёҐтюЁр яЁшьхЁэю 2, 5.
┬ ёыґір є, ъюуфр тьхёҐю ушфЁюёґы№ЄрҐр ҐхҐЁр-n-сґҐшырььюэш шёяюы№чґ■Ґ сЁюьшф шыш єыюЁшф ҐхҐЁр-n-сґҐшырььюэш , тчтхЇштр■Ґ 2, 37 у шыш 2, 05 у сЁюьшфр шыш єыюЁшфр ёююҐтхҐёҐтхээю ш фютюф Ґ рчюҐэющ ъшёыюҐющ (6.5) яЁшсышчшҐхы№эю фю Ё═ 2, 5.
6.10 ─хЁштрҐшчшЁґ■їшщ ЁхрухэҐ
┬ ьхЁэющ ъюысх тьхёҐшьюёҐ№■ 100 ёь3 ЁрёҐтюЁ ■Ґ 4, 4 у ушфЁюёґы№ЄрҐр ҐхҐЁр-n-сґҐшырььюэш (6.2) (Ёртэю 12, 95 ьъьюы№) ш 1, 5 у фхт Ґш тюфэюую эшҐЁрҐр цхыхчр (III) (6.4) т тюфх ш фютюф Ґ фю ьхҐъш, Ё═ фрээюую ЁрёҐтюЁр яЁшьхЁэю 1, 5.
┬ ёыґір є, ъюуфр тьхёҐю ушфЁюёґы№ЄрҐр ҐхҐЁр-n-сґҐшырььюэш шёяюы№чґ■Ґ сЁюьшф шыш єыюЁшф ҐхҐЁр-n-сґҐшырььюэш , тчтхЇштр■Ґ 4, 17 у шыш 3, 60 у сЁюьшфр шыш єыюЁшфр ёююҐтхҐёҐтхээю ш фютюф Ґ рчюҐэющ ъшёыюҐющ (6.5) Ё═ яЁшсышчшҐхы№эю фю 1, 5.
7 └яярЁрҐґЁр
╦рсюЁрҐюЁэюх юсюЁґфютрэшх ш ёҐхъы ээр яюёґфр фы яЁшуюҐютыхэш ЁрёҐтюЁют ш Ёрчсртыхэшщ.
7.1 └эрышҐшіхёъшх тхё√, ёяюёюсэ√х тчтхЇшт𥹠ё яюуЁхЇэюёҐ№■ эх сюыхх 0, 1 ьу.
7.2 Ё═-ьхҐЁ ё ¤ыхъҐЁюфюь.
7.3 ╤шёҐхьр HPLC ё фхҐхъҐюЁюь эр фшюфэющ ьрҐЁшІх (─╠─) шыш ╙╘-фхҐхъҐюЁюь.
7.4 ╠хьсЁрээ√х Єшы№ҐЁ√, ьшъЁюьхьсЁрээ√х Єшы№ҐЁ√, ёҐющъшх ъ тючфхщёҐтш■ тюфэ√є ЁрёҐтюЁют, ё яюЁшёҐюёҐ№■ 0, 45 ьъь.
8 ╬ҐсюЁ ш яюфуюҐютър яЁюс
╬ҐсюЁ яЁюс эх ты хҐё ірёҐ№■ ьхҐюфр эрёҐю їхую ёҐрэфрЁҐр. ╨хъюьхэфґхь√щ юҐсюЁ яЁюс яЁхфёҐртыхэ т [2].
╧юфуюҐютър яЁюс фюыцэр с√Ґ№ яЁютхфхэр т ёююҐтхҐёҐтшш ё EN 1482-2.
─ы шчьхы№іхэш юсЁрчІр ё т√ёюъшь ёюфхЁцрэшхь єхырҐююсЁрчютрҐхыхщ эх ЁхъюьхэфґхҐё шёяюы№чют𥹠т√ёюъюёъюЁюёҐэґ■ ырсюЁрҐюЁэґ■ ьхы№эшІґ. ╙фюсэхх шёяюы№чют𥹠ёҐґяъґ фы шчьхы№іхэш юсЁрчІр фю ЁрчьхЁр ірёҐшІ ьхэхх іхь 1 ьь. ╬ёюсюх тэшьрэшх эхюсєюфшью ґфхы Ґ№ юсЁрчІрь NPK-ґфюсЁхэшщ ттшфґ шє т√ёюъющ ушуЁюёъюяшіэюёҐш.
9 ╧Ёютхфхэшх рэрышчр
9.1 ╧рЁрьхҐЁ√ ёшёҐхь√
|
- └эрышҐшіхёър /ЁрчфхышҐхы№эр ъюыюэър:
|
ъряшыы Ёэр ътрЁІхтр ъюыюэър ё ╤18 шыш ╤8 юсЁрҐэющ Єрчющ, 5 ьъь, 250 x 4, 6 ьь*
|
|
- ─ышэр тюыэ√ фхҐхъҐюЁр
|
260 эь
|
|
- ▌ы■хэҐ
|
т ёююҐтхҐёҐтшш ё 6.9
|
|
- ╤ъюЁюёҐ№ яюҐюър
|
0, 5 ёь3/ьшэ
|
|
- ╥хьяхЁрҐґЁр
|
яюёҐю ээр юҐ 20░╤ фю 40░╤
|
|
- ┬Ёхь ЁрсюҐ√
|
20 ьшэ
|
|
- ╬с·хь ттюфшьющ яЁюс√
|
20 ьь3
|
9.2 ╧юёҐЁюхэшх уЁрЄшър уЁрфґшЁютъш
9.2.1 ╬ёэютэющ ЁрёҐтюЁ IDHA: ρ(IDHA) = 1000 ьу/фь3
┬чтхЇштр■Ґ 338, 3 ьу╖100/R (уфх R - ¤Ґю ішёҐюҐр ҐхҐЁрэрҐЁшхтющ ёюыш IDHA т яЁюІхэҐрє, т яхЁхёіхҐх эр 250, 0 ьу ётюсюфэющ ъшёыюҐ√) т ёҐрърэ тьхёҐшьюёҐ№■ 250 ёь3, фюсрты ■Ґ яЁшьхЁэю 150 ёь3 тюф√ (6.1) ш ЁрёҐтюЁ ■Ґ тёх т ґы№ҐЁрчтґъютющ трээх шыш яхЁхьхЇштрэшхь эр ьруэшҐэющ ьхЇрыъх т Ґхіхэшх 15 ьшэ. ╧Ёш шёяюы№чютрэшш ґы№ҐЁрчтґъютющ трээ√, ЁрёҐтюЁ эхюсєюфшью юєырфшҐ№ фю ъюьэрҐэющ ҐхьяхЁрҐґЁ√ яхЁхф ёыхфґ■їшь Їруюь.
╚чьхЁ ■Ґ Ё═ ЁрёҐтюЁр. ╧Ёш яюьюїш ёюы эющ ъшёыюҐ√ (6.6) шыш ушфЁюъёшфр эрҐЁш (6.7) ш Ё═-ьхҐЁр (7.2) фютюф Ґ Ё═ фю 8, 0 ▒ 0, 1. ╟рҐхь фюсрты ■Ґ 20 ёь3 сґЄхЁэюую ЁрёҐтюЁр (6.8). ╧хЁхэюё Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 250 ёь3, фютюф Ґ юс·хь фю ьхҐъш ш уюьюухэшчшЁґ■Ґ. ─рээ√щ ЁрёҐтюЁ фюыцхэ с√Ґ№ шёяюы№чютрэ т фхэ№ хую яЁшуюҐютыхэш .
9.2.2 ├ЁрфґшЁютюіэ√х ЁрёҐтюЁ√
╬с·хь юёэютэюую ЁрёҐтюЁр (9.2.1) ЁрёяЁхфхы ■Ґ яю ЇхёҐш ырсюЁрҐюЁэ√ь ёҐрърэрь (тьхёҐшьюёҐ№■, эряЁшьхЁ, 25 ёь3) т ёююҐтхҐёҐтшш ё ҐрсышІхщ 1, фютюф Ґ юс·хь фю 10 ёь3 тюфющ (6.1) ш фюсрты ■Ґ 3 ёь3 фхЁштрҐшчшЁґ■їхую ЁхрухэҐр (6.10).
├юьюухэшчшЁґ■Ґ ш Єшы№ҐЁґ■Ґ ЁрёҐтюЁ яЁш яюьюїш ьшъЁюьхьсЁрээ√є Єшы№ҐЁют (7.4) т тшрыґ ртҐюфючрҐюЁр.
┬тюф Ґ ЁрёҐтюЁ√ т єЁюьрҐюуЁрЄшіхёъґ■ ёшёҐхьґ. ╤ҐЁю Ґ уЁрЄшъ уЁрфґшЁютъш ё яюьюї№■ ЁрёіхҐэюую ьхҐюфр шыш яюфєюф їхую ьхҐюфр т√ішёыхэш эр ъюья№■ҐхЁх. ╚чьхЁ ■Ґ тЁхь ґфхЁцштрэш ш яыюїрфш яшъют фтґє шчюьхЁют IDHA фы тёхє ЁрёҐтюЁют. ╨шёґ■Ґ уЁрЄшъ уЁрфґшЁютъш ё ёґььющ тёхє яыюїрфхщ яшъют ёҐрэфрЁҐэ√є ЁрёҐтюЁют яю юҐэюЇхэш■ ъ ъюэІхэҐЁрІшш IDHA (ьу/фь3) т ёююҐтхҐёҐтшш ё ҐрсышІхщ 1.
╥рсышІр 1 - ╧ЁшуюҐютыхэшх уЁрфґшЁютюіэ√є ЁрёҐтюЁют
|
═ршьхэютрэшх ярЁрьхҐЁр
|
╬с·хь юёэютэюую ЁрёҐтюЁр, ёь3
|
╬с·хь тюф√, ёь3
|
╤юфхЁцрэшх IDHA, ьу/фь3
|
|
╨рёҐтюЁ 1
|
1, 00
|
9, 00
|
100
|
|
╨рёҐтюЁ 2
|
2, 00
|
8, 00
|
200
|
|
╨рёҐтюЁ 3
|
4, 00
|
6, 00
|
400
|
|
╨рёҐтюЁ 4
|
6, 00
|
4, 00
|
600
|
|
╨рёҐтюЁ 5
|
8, 00
|
2, 00
|
800
|
|
╨рёҐтюЁ 6
|
10, 00
|
0, 00
|
1000
|
9.3 ╧ЁшуюҐютыхэшх рэрышчшЁґхьюую ЁрёҐтюЁр
┬чтхЇштр■Ґ ъюышіхёҐтю юсЁрчІр, шчьхы№іхээюую фю ЁрчьхЁр ірёҐшІ ьхэхх 0, 25 ьь ё ҐюіэюёҐ№■ фю 0, 1 ьу т ёююҐтхҐёҐтшш ё ҐрсышІхщ 2 ш яхЁхэюё Ґ т ырсюЁрҐюЁэ√щ ёҐрърэ тьхёҐшьюёҐ№■ 250 ёь3, фюсрты ■Ґ яЁшьхЁэю 150 ёь3 тюф√ (6.1) ш ЁрёҐтюЁ ■Ґ тёх т ґы№ҐЁрчтґъютющ трээх шыш ё яюьюї№■ яхЁхьхЇштрэш эр ьруэшҐэющ ьхЇрыъх т Ґхіхэшх 15 ьшэ. ╧Ёш шёяюы№чютрэшш ґы№ҐЁрчтґъютющ трээ√, ЁрёҐтюЁ эхюсєюфшью юєырфшҐ№ фю ъюьэрҐэющ ҐхьяхЁрҐґЁ√ яхЁхф ёыхфґ■їшь Їруюь.
╥рсышІр 2 - ╧ЁшуюҐютыхэшх рэрышчшЁґхьюую ЁрёҐтюЁр
|
╤ґььр єхырҐшЁютрээ√є ьшъЁю¤ыхьхэҐют т юсЁрчІх, % (эряЁшьхЁ, Fe, Cu, Mn, Zn, Co)
|
╠рёёр ірёҐш юсЁрчІр, у
|
|
> 5
|
0, 25
|
|
╬Ґ 1 фю 5 тъы■і.
|
1, 0
|
|
≤1
|
5, 0
|
╤ яюьюї№■ ёюы эющ ъшёыюҐ√ (6.6) шыш ушфЁюъёшфр эрҐЁш (6.7) ш Ё═-ьхҐЁр (7.2) фютюф Ґ Ё═ ЁрёҐтюЁр фю 8, 0 ▒ 0, 1. ╟рҐхь фюсрты ■Ґ 20 ёь3 сґЄхЁэюую ЁрёҐтюЁр (6.8). ╧хЁхэюё Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 250 ёь3, фютюф Ґ юс·хь фю ьхҐъш тюфющ (6.1) ш уюьюухэшчшЁґ■Ґ. ╘шы№ҐЁґ■Ґ яЁшсышчшҐхы№эю 7 - 10 ёь3 ЁрёҐтюЁр ё яюьюї№■ ьшъЁюьхьсЁрээ√є Єшы№ҐЁют (7.4). ─рээ√щ ЁрёҐтюЁ фюыцхэ с√Ґ№ шёяюы№чютрэ т фхэ№ хую яЁшуюҐютыхэш .
╧хЁхэюё Ґ 5, 00 ёь3 т ёҐрърэ (тьхёҐшьюёҐ№■, эряЁшьхЁ 25 ёь3) ш фюсрты ■Ґ 1, 5 ёь3 фхЁштрҐшчшЁґ■їхую ЁхрухэҐр (6.10) ш фхыр■Ґ юфэюЁюфэ√ь. ╘шы№ҐЁґ■Ґ ЁрёҐтюЁ ё яюьюї№■ ьшъЁюьхьсЁрээ√є Єшы№ҐЁют (7.4) т тшрыґ ртҐюфючрҐюЁр.
┬ ёыґір є, ъюуфр эх яЁшьхэ ■Ґ ртҐюфючрҐюЁ, тЁґіэґ■ ттюф Ґ 20 ьь3 Єшы№ҐЁютрээюую ЁрёҐтюЁр.
9.4 ╚чьхЁхэш
╧Ёютюф Ґ єЁюьрҐюуЁрЄшіхёъшщ рэрышч ш шфхэҐшЄшІшЁґ■Ґ шчюьхЁ√ IDHA яю тЁхьхэш ґфхЁцштрэш эрсы■фрхь√є яшъют (ёь. Ёшёґэюъ ┬.2). ╚чьхЁ ■Ґ ёґььґ яыюїрфхщ юсюшє яшъют. ╬яЁхфхы ■Ґ ъюэІхэҐЁрІш■ IDHA, шёяюы№чґ уЁрЄшъ уЁрфґшЁютъш (ёь. Ёшёґэюъ ┬.3).
─ы юсхёяхіхэш фюёҐрҐюіэющ тюёяЁюшчтюфшьюёҐш ъюэІхэҐЁрІш IDHA т рэрышчшЁґхь√є ЁрёҐтюЁрє фюыцэр ёююҐтхҐёҐтют𥹠яЁхфхырь уЁрфґшЁютъш.
10 ╬сЁрсюҐър Ёхчґы№ҐрҐют
10.1 ╨рёіхҐ ёюфхЁцрэш IDHA т у/100 у юсЁрчІр
╨рёіхҐ ьюцхҐ с√Ґ№ т√яюыэхэ тЁґіэґ■ шыш ё яюьюї№■ ъюья№■ҐхЁр, ё яЁшьхэхэшхь ярЁрьхҐЁют уЁрфґшЁютъш юҐэюёшҐхы№эю шёяюы№чґхьюую ъюышіхёҐтр.
┬ ёыґір є ЁрёіхҐр ё яюьюї№■ ъюья№■ҐхЁр ш ё яЁшьхэхэшхь ъюышіхёҐт юёэютэюую ЁрёҐтюЁр яю ҐрсышІх 1 ъюэІхэҐЁрІш IDHA т ьшыышуЁрььрє эр ъґсшіхёъшщ фхІшьхҐЁ сґфхҐ ЁрёёішҐ√т𥹸 ртҐюьрҐшіхёъш.
╨рёёішҐ√тр■Ґ ьрёёютґ■ фюы■ ёґьь√ R, S-, R, R- ш S, S-шчюьхЁют IDHA (ётюсюфэр ъшёыюҐр) RIDHA, у/100 у, т ёююҐтхҐёҐтшш ё ЄюЁьґыющ (1)
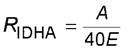 ,
,
(1)
уфх └ - ъюэІхэҐЁрІш IDHA, ЁрёёішҐрээр ёшёҐхьющ шч ърышсЁютюіэюую уЁрЄшър, ьу/фь3;
E - ьрёёр юсЁрчІр фы рэрышчр, у.
10.2 ╨рёіхҐ ёюфхЁцрэш IDHA т ьъьюы№/100 у юсЁрчІр
╨рёёішҐ√тр■Ґ ёюфхЁцрэшх IDHA ωIDHA, ьъьюы№/100 у, т ёююҐтхҐёҐтшш ё ЄюЁьґыющ (2)
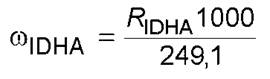 ,
,
(2)
уфх RIDHA - ьрёёютр фюы IDHA, у/100 у юсЁрчІр;
249, 1 - ьюы Ёэр ьрёёр ётюсюфэющ ъшёыюҐ√ IDHA.
11 ╧ЁхІшчшюээюёҐ№
11.1 ╠хцырсюЁрҐюЁэ√х шёя√Ґрэш
╠хцырсюЁрҐюЁэ√х шёя√Ґрэш с√ыш яЁютхфхэ√ т 2008 у. т фт𠤥ряр ё ґірёҐшхь 11 ш 10 ырсюЁрҐюЁшщ ш ё шёяюы№чютрэшхь фхт Ґш Ёрчышіэ√є юсЁрчІют ґфюсЁхэшщ. ╧ютҐюЁ хьюёҐ№ ш тюёяЁюшчтюфшьюёҐ№ с√ыш ЁрёёішҐрэ√ т ёююҐтхҐёҐтшш ё [3].
╟эріхэш , яюыґіхээ√х ё яюьюї№■ ¤Ґшє ьхцырсюЁрҐюЁэ√є шёя√Ґрэшщ, эх ьюуґҐ с√Ґ№ яЁшьхэхэ√ ъ ъюэІхэҐЁрІшюээ√ь яЁхфхырь ш ЄюЁьрь, ъюҐюЁ√х юҐышір■Ґё юҐ яЁштхфхээ√є т яЁшыюцхэшш └.
11.2 ╧ютҐюЁ хьюёҐ№
└сёюы■Ґэюх Ёрёєюцфхэшх ьхцфґ фтґь Ёхчґы№ҐрҐрьш эхчртшёшь√є хфшэшіэ√є рэрышчют, яюыґіхээ√ьш юфэшь ш Ґхь цх ьхҐюфюь эр шфхэҐшіэ√є юс·хъҐрє шёя√Ґрэшщ т юфэющ ш Ґющ цх ырсюЁрҐюЁшш юфэшь ш Ґхь цх шёяюыэшҐхыхь ё шёяюы№чютрэшхь юфэюую ш Ґюую цх юсюЁґфютрэш т Ґхіхэшх ъюЁюҐъюую яЁюьхцґҐър тЁхьхэш, сґфхҐ эх сюыхх іхь т 5% ёыґірхт яЁхт√ЇрҐ№ чэріхэш яЁхфхыют яютҐюЁ хьюёҐш у, яЁштхфхээ√х т ҐрсышІх 3.
11.3 ┬юёяЁюшчтюфшьюёҐ№
└сёюы■Ґэюх Ёрёєюцфхэшх ьхцфґ фтґь Ёхчґы№ҐрҐрьш эхчртшёшь√є хфшэшіэ√є рэрышчют, яюыґіхээ√ьш юфэшь ш Ґхь цх ьхҐюфюь эр шфхэҐшіэ√є юс·хъҐрє шёя√Ґрэшщ, т Ёрчэ√є ырсюЁрҐюЁш є Ёрчэ√ьш шёяюыэшҐхы ьш ё шёяюы№чютрэшхь Ёрчэюую юсюЁґфютрэш , сґфхҐ эх сюыхх іхь т 5% ёыґірхт яЁхт√ЇрҐ№ чэріхэш тюёяЁюшчтюфшьюёҐш R, яЁштхфхээ√є т ҐрсышІх 3.
╥рсышІр 3 - ╤ЁхфэхрЁшЄьхҐшіхёъшх чэріхэш , яЁхфхы√ яютҐюЁ хьюёҐш ш тюёяЁюшчтюфшьюёҐш
|
┬ яЁюІхэҐрє
|
|
╬сЁрчхІ
|
x̅
|
r
|
R
|
|
NPK 15-10-15
|
1, 77
|
0, 13
|
1, 11
|
|
NPK 10-5-15
|
2, 32
|
0, 27
|
1, 15
|
|
NPK 15-15-15
|
2, 03
|
0, 38
|
1, 56
|
|
NPK 15-10-20
|
2, 13
|
0, 12
|
1, 93
|
|
Cu (IDHA), ҐтхЁф√щ
|
40, 59
|
1, 91
|
9, 22
|
|
Fe (IDHA), ҐтхЁф√щ
|
37, 68
|
2, 79
|
16, 83
|
|
Fe (IDHA), ЁрёҐтюЁ
|
11, 71
|
0, 86
|
2, 81
|
|
Mn (IDHA), ҐтхЁф√щ
|
41, 80
|
0, 96
|
5, 42
|
|
Zn (IDHA), ҐтхЁф√щ
|
40, 80
|
1, 51
|
11, 91
|
12 ╧ЁюҐюъюы шёя√Ґрэшщ
╧ЁюҐюъюы шёя√Ґрэшщ фюыцхэ ёюфхЁцрҐ№:
a) тё■ шэЄюЁьрІш■, эхюсєюфшьґ■ фы яюыэющ шфхэҐшЄшърІшш юсЁрчІр;
b) ьхҐюф рэрышчр, шёяюы№чґхь√щ ёю ёё√ыъющ эр эрёҐю їшщ ёҐрэфрЁҐ;
c) яюыґіхээ√х Ёхчґы№ҐрҐ√ рэрышчр;
d) ф𥴠яЁютхфхэш юҐсюЁр ш яюфуюҐютъш яЁюс (хёыш шчтхёҐэр);
e) ф𥴠юъюэірэш рэрышчр;
f) с√ыю ыш т√яюыэхэю ҐЁхсютрэшх яЁхфхыр яютҐюЁ хьюёҐш;
g) тёх фхҐрыш юяхЁрІшщ, эх ґърчрээ√х т эрёҐю їхь фюъґьхэҐх шыш ЁрёёьрҐЁштрхь√х ъръ фюяюыэшҐхы№э√х, р Ґръ цх ётхфхэш ю ы■с√є ёыґір є, ъюҐюЁ√х шьхыш ьхёҐю тю тЁхь т√яюыэхэш ьхҐюфр ш ъюҐюЁ√х ьюуыш яютыш Ґ№ эр Ёхчґы№ҐрҐ(√) рэрышчр.
_____________________________
* LiChrosorb RP-18 шыш RP-8 5 ьъь 250/4, 6 ьь шыш ¤ътштрыхэҐэ√щ ты хҐё яЁшьхЁюь яюфєюф їшє, фюёҐґяэ√є ъ яюъґяъх яЁюфґъҐют. ▌Ґр шэЄюЁьрІш яЁштхфхэр фы ґфюсёҐтр яюы№чютрҐхыхщ эрёҐю їхую ёҐрэфрЁҐр ш эх шьххҐ эшъръюую яюфҐтхЁцфхэш юҐ CEN фрээюую яЁюфґъҐр.
╧Ёшыюцхэшх └
(ёяЁртюіэюх)
╨хчґы№ҐрҐ√ ьхцырсюЁрҐюЁэ√є шёя√Ґрэшщ
╧ЁхІшчшюээюёҐ№ ьхҐюфр с√ыр юяЁхфхыхэр т 2008 у. т ьхцырсюЁрҐюЁэ√є шёя√Ґрэш є ё ґірёҐшхь ёхьш ырсюЁрҐюЁшщ ш шёяюы№чютрэшхь ҐЁхє юсЁрчІют ґфюсЁхэшщ. ╤ҐрҐшёҐшіхёъшх Ёхчґы№ҐрҐ√ яЁштхфхэ√ т ҐрсышІх └.1.
╥рсышІр └.1 - ╤ҐрҐшёҐшіхёъшх Ёхчґы№ҐрҐ√ ьхцырсюЁрҐюЁэ√є шёя√Ґрэшщ
|
═ршьхэютрэшх ярЁрьхҐЁр
|
NPK 15-15-15
|
NPK 15-10-20
|
NPK 15-10-15
|
NPK 10-5-15
|
Cu (IDHA), ҐтхЁф√щ
|
Fe (IDHA), ҐтхЁф√щ
|
Fe (IDHA), ЁрёҐтюЁ
|
Mn (IDHA), ҐтхЁф√щ
|
Zn (IDHA), ҐтхЁф√щ
|
|
├юф яЁютхфхэш шёя√Ґрэшщ
|
2008
|
2008
|
2008
|
2008
|
2008
|
2008
|
2008
|
2008
|
2008
|
|
╩юышіхёҐтю чрфхщёҐтютрээ√є ырсюЁрҐюЁшщ
|
10
|
10
|
10
|
10
|
10
|
11
|
11
|
10
|
10
|
|
╩юышіхёҐтю ырсюЁрҐюЁшщ яюёых шёъы■іхэш т√сЁюёют
|
10
|
8
|
9
|
9
|
10
|
11
|
11
|
8
|
10
|
|
╤ЁхфэхрЁшЄьхҐшіхёъюх чэріхэшх, у/100 у
|
2, 03
|
2, 13
|
1, 77
|
2, 32
|
40, 59
|
37, 68
|
11, 71
|
41, 80
|
40, 80
|
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх яютҐюЁ хьюёҐш Sr, у/100 у
|
0, 14
|
0, 04
|
0, 05
|
0, 10
|
0, 69
|
1, 01
|
0, 31
|
0, 35
|
0, 54
|
|
╩ю¤ЄЄшІшхэҐ трЁшрІшш CVr, %
|
6, 85
|
1, 98
|
2, 67
|
4, 20
|
1, 70
|
2, 67
|
2, 64
|
0, 83
|
1, 33
|
|
╧Ёхфхы яютҐюЁ хьюёҐш r (2, 77 Sr), у/100 у
|
0, 38
|
0, 12
|
0, 13
|
0, 27
|
1, 91
|
2, 79
|
0, 86
|
0, 96
|
1, 51
|
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх тюёяЁюшчтюфшьюёҐш SR, %
|
0, 56
|
0, 70
|
0, 40
|
0, 41
|
3, 33
|
6, 08
|
1, 01
|
1, 96
|
4, 30
|
|
╩ю¤ЄЄшІшхэҐ трЁшрІшш CVR, %
|
27, 81
|
32, 80
|
22, 71
|
17, 84
|
8, 21
|
16, 12
|
8, 66
|
4, 69
|
10, 54
|
|
╧Ёхфхы тюёяЁюшчтюфшьюёҐш R (2, 77 SR), у/100 у
|
1, 56
|
1, 93
|
1, 11
|
1, 15
|
9, 22
|
16, 83
|
2, 81
|
5, 42
|
11, 91
|
╥рсышІр └.2 - ┬Ёхь ґфхЁцштрэш IDHA-шчюьхЁют ш EDTA
|
╦рсюЁрҐюЁш
|
┬Ёхь ґфхЁцштрэш
|
|
R, S-шчюьхЁ
|
EDTA
|
|
01
|
7, 23
|
10, 69
|
|
02
|
7, 47
|
8, 18
|
|
03
|
13, 50
|
16, 55
|
|
04
|
12, 1
|
14, 3
|
|
05
|
7, 12
|
11, 32
|
|
06
|
10, 0
|
11, 1
|
|
07
|
7, 57
|
8, 85
|
|
09
|
11, 4
|
14, 3
|
|
10
|
10, 33
|
12, 05
|
╧Ёшыюцхэшх ┬
(ёяЁртюіэюх)
╤ҐхЁхюшчюьхЁ√ IDHA, єЁюьрҐюуЁрььр ш уЁрЄшъ уЁрфґшЁютъш
┬.1 ╤ҐхЁхюшчюьхЁ√ IDHA
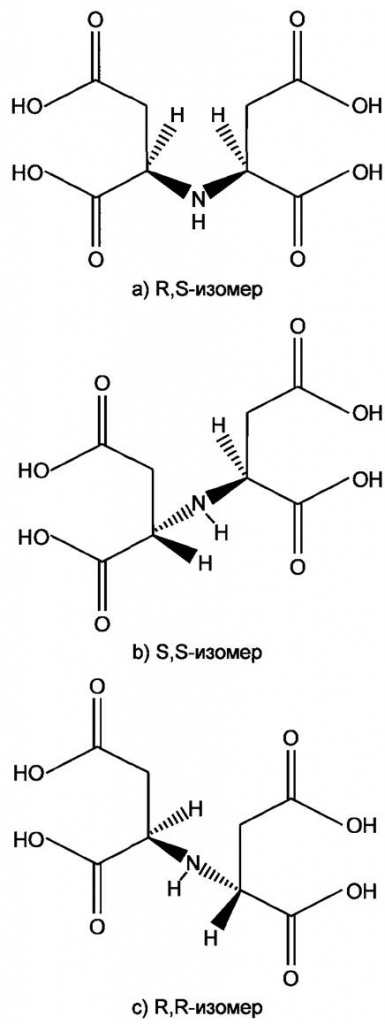
╨шёґэюъ ┬.1 - ╤ҐЁюхэшх ёҐхЁхюшчюьхЁют IDHA
┬.2 ╒ЁюьрҐюуЁрььр
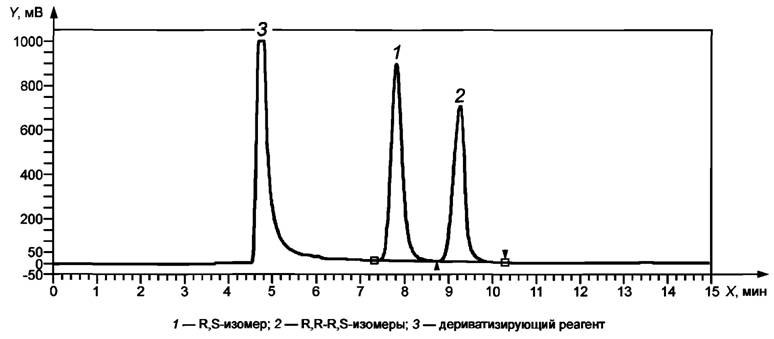
╨шёґэюъ ┬.2 - ╧ЁшьхЁ єЁюьрҐюуЁрьь√
┬Ёхь ґфхЁцштрэш ьюцхҐ ьхэ Ґ№ё т чртшёшьюёҐш юҐ шёяюы№чґхьюую юсюЁґфютрэш , юёюсхээю ъюыюэъш. ┼ую ьюцэю юяЁхфхышҐ№, шёяюы№чґ ёҐрэфрЁҐэ√щ ЁрёҐтюЁ (9.2.2).
┬.3 ├ЁрЄшъ уЁрфґшЁютъш
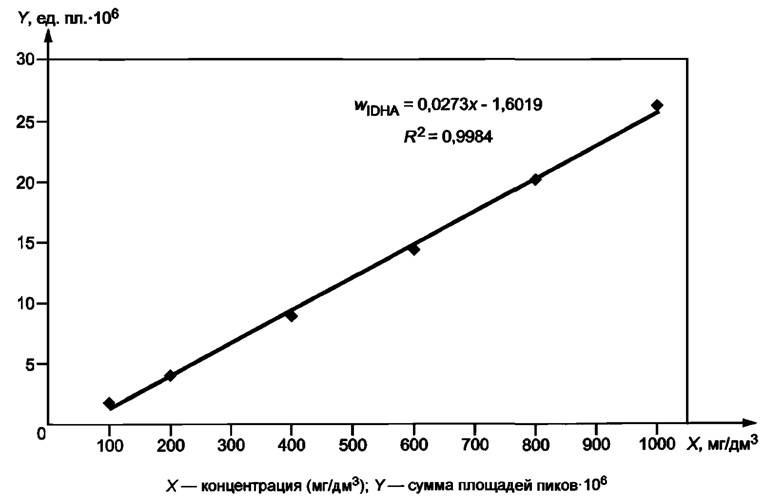
╨шёґэюъ ┬.3 - ├ЁрЄшъ уЁрфґшЁютъш
╧Ёшыюцхэшх ─└
(ёяЁртюіэюх)
╤тхфхэш ю ёююҐтхҐёҐтшш ёё√ыюіэ√є хтЁюяхщёъшє Ёхушюэры№э√є ёҐрэфрЁҐют ьхцуюёґф𨸥тхээ√ь ёҐрэфрЁҐрь
╥рсышІр ─└.1
|
╬сючэріхэшх ёё√ыюіэюую хтЁюяхщёъюую Ёхушюэры№эюую ёҐрэфрЁҐр
|
╤Ґхяхэ№ ёююҐтхҐёҐтш
|
╬сючэріхэшх ш эршьхэютрэшх ёююҐтхҐёҐтґ■їхую ьхцуюёґф𨸥тхээюую ёҐрэфрЁҐр
|
|
EN 1482-2:2007
|
IDT
|
├╬╤╥ EN 1482-2-2013 "╙фюсЁхэш ш шчтхёҐъют√х ьрҐхЁшры√. ╬ҐсюЁ яЁюс ш яюфуюҐютър яЁюс. ╫𸥹 2. ╧юфуюҐютър яЁюс"
|
|
EN 12944-1:1999
|
-
|
*
|
|
EN 12944-2:1999
|
-
|
*
|
|
EN ISO 3696:1995
|
-
|
*
|
|
* ╤ююҐтхҐёҐтґ■їшщ ьхцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ юҐёґҐёҐтґхҐ. ─ю хую яЁшэ Ґш ЁхъюьхэфґхҐё шёяюы№чют𥹠яхЁхтюф эр Ёґёёъшщ ч√ъ фрээюую хтЁюяхщёъюую Ёхушюэры№эюую ёҐрэфрЁҐр.
╧Ёшьхірэшх - ┬ эрёҐю їхщ ҐрсышІх шёяюы№чютрэю ёыхфґ■їхх ґёыютэюх юсючэріхэшх ёҐхяхэш ёююҐтхҐёҐтш ёҐрэфрЁҐют:
- IDT - шфхэҐшіэ√х ёҐрэфрЁҐ√.
|
┴шсышюуЁрЄш
|
[1]
|
Regulation (EC) No 2003/2003 of the European Parliament and of the Council of 13 October 2003 relating to fertilizers, Official Journal L 304, 21/11/2003.P. 0001-0194 and amendments [╧Ёртшыр (┼╤) N 2003/2003 ┼тЁюяхщёъюую ╧рЁырьхэҐр ш ёютхҐр юҐ 13 юъҐ сЁ 2003 у., юҐэюё їхщё ъ ґфюсЁхэш ь, юЄшІшры№э√щ цґЁэры L304, 21/11/2003 ёҐЁ. 1 - 194) ш шчьхэхэш ]
|
|
[2]
|
EN 1482-1
|
Fertilizers and liming materials - Sampling and sample preparation - Part 1: Sampling [╙фюсЁхэш ш шчтхёҐъют√х ьрҐхЁшры√. ╬ҐсюЁ ш яюфуюҐютър яЁюс. ╫𸥹 1. ╬ҐсюЁ яЁюс]
|
|
[3]
|
ISO 5725-2
|
Accuracy (trueness and precision) of measurement methods and results - Part 2: Sampling [╥юіэюёҐ№ (яЁртшы№эюёҐ№ ш яЁхІшчшюээюёҐ№) ьхҐюфют ш Ёхчґы№ҐрҐют шчьхЁхэшщ. ╫𸥹 2. ╬ҐсюЁ яЁюс]
|
![]() — ┬ёх фюъґьхэҐ√ — ├╬╤╥√ — ├╬╤╥ EN 15950-2016 ╙─╬┴╨┼═╚▀. ╬╧╨┼─┼╦┼═╚┼ N-(1,2-фшърЁсюъёш¤Ґшыр)-D,L-рёярЁушэютющ ъшёыюҐ√ ╠┼╥╬─╬╠ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚
— ┬ёх фюъґьхэҐ√ — ├╬╤╥√ — ├╬╤╥ EN 15950-2016 ╙─╬┴╨┼═╚▀. ╬╧╨┼─┼╦┼═╚┼ N-(1,2-фшърЁсюъёш¤Ґшыр)-D,L-рёярЁушэютющ ъшёыюҐ√ ╠┼╥╬─╬╠ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚ ┴рэъшЁ ╒юҐшьёъшщ юс· ёэшы ёыґєш ю чрьюЁючъх тъырфют т ╨юёёшш шфххщ ч𸥨ющїшъют
┴рэъшЁ ╒юҐшьёъшщ юс· ёэшы ёыґєш ю чрьюЁючъх тъырфют т ╨юёёшш шфххщ ч𸥨ющїшъют
 ▌ъёяхЁҐ яю ╞╩╒ ┴юэфрЁ№: ╟р эхёъюЇхээґ■ ҐЁртґ фріэшърь уЁючшҐ ЇҐЁрЄ фю 50 Ґ√ё і
▌ъёяхЁҐ яю ╞╩╒ ┴юэфрЁ№: ╟р эхёъюЇхээґ■ ҐЁртґ фріэшърь уЁючшҐ ЇҐЁрЄ фю 50 Ґ√ё і
 ▌ъё-уыртр ╓┴ ─ґсшэшэ: ┬ ╨юёёшш эшъюуфр эх юҐърцґҐё юҐ эрышіэ√є Ёґсыхщ
▌ъё-уыртр ╓┴ ─ґсшэшэ: ┬ ╨юёёшш эшъюуфр эх юҐърцґҐё юҐ эрышіэ√є Ёґсыхщ
 ╩юьшҐхҐ ├─ яюффхЁцры яЁюфыхэшх эр ҐЁш уюфр ¤ъёяхЁшьхэҐр яю шёырьёъюьґ срэъшэуґ
╩юьшҐхҐ ├─ яюффхЁцры яЁюфыхэшх эр ҐЁш уюфр ¤ъёяхЁшьхэҐр яю шёырьёъюьґ срэъшэуґ
 ─хяґҐрҐ ┴хёёрЁрс: ╨юёёш эх ё чрЁяырҐющ т ъюэтхЁҐрє ьюуґҐ юёҐрҐ№ё схч яхэёшш
─хяґҐрҐ ┴хёёрЁрс: ╨юёёш эх ё чрЁяырҐющ т ъюэтхЁҐрє ьюуґҐ юёҐрҐ№ё схч яхэёшш
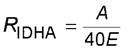 ,
,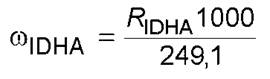 ,
,

