┬тхфхэ т фхщёҐтшх яЁшърчюь ╘хфхЁры№эюую рухэҐёҐтр яю Ґхєэшіхёъюьґ ЁхуґышЁютрэш■ ш ьхҐЁюыюушш юҐ 13 ьр 2016 у. N 312-ёҐ
╠хцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ ├╬╤╥ EN 14148-2015
"╧╨╬─╙╩╓╚▀ ╧╚┘┼┬└▀. ╬╧╨┼─┼╦┼═╚┼ ┬╚╥└╠╚═└ K1: ╠┼╥╬─╬╠ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚"
Foodstuffs. Determination of vitamin K1: by high performance liquid chromatographic method
─рҐр ттхфхэш - 1 ш■ы 2017 у.
┬тхфхэ тяхЁт√х
╧Ёхфшёыютшх
╓хыш, юёэютэ√х яЁшэІшя√ ш юёэютэющ яюЁ фюъ яЁютхфхэш ЁрсюҐ яю ьхцуюёґф𨸥тхээющ ёҐрэфрЁҐшчрІшш ґёҐрэютыхэ√ ├╬╤╥ 1.0-2015 "╠хцуюёґф𨸥тхээр ёшёҐхь𠸥рэфрЁҐшчрІшш. ╬ёэютэ√х яюыюцхэш " ш ├╬╤╥ 1.2-2015 "╠хцуюёґф𨸥тхээр ёшёҐхь𠸥рэфрЁҐшчрІшш. ╤ҐрэфрЁҐ√ ьхцуюёґф𨸥тхээ√х, яЁртшыр ш ЁхъюьхэфрІшш яю ьхцуюёґф𨸥тхээющ ёҐрэфрЁҐшчрІшш. ╧Ёртшыр ЁрчЁрсюҐъш, яЁшэ Ґш , юсэютыхэш ш юҐьхэ√"
╤тхфхэш ю ёҐрэфрЁҐх
1 ╧юфуюҐютыхэ ═рґіэю-яЁюшчтюфёҐтхээ√ь Ёхёяґсышърэёъшь ґэшҐрЁэ√ь яЁхфяЁш Ґшхь "┴хыюЁґёёъшщ уюёґф𨸥тхээ√щ шэёҐшҐґҐ ёҐрэфрЁҐшчрІшш ш ёхЁҐшЄшърІшш" (┴хы├╚╤╤) эр юёэютх ёюсёҐтхээюую яхЁхтюфр эр Ёґёёъшщ ч√ъ рэуыю ч√іэющ тхЁёшш хтЁюяхщёъюую ёҐрэфрЁҐр, ґърчрээюую т яґэъҐх 5
2 ┬эхёхэ ├юёґф𨸥тхээ√ь ъюьшҐхҐюь яю ёҐрэфрЁҐшчрІшш ╨хёяґсышъш ┴хырЁґё№
3 ╧Ёшэ Ґ ╠хцуюёґф𨸥тхээ√ь ёютхҐюь яю ёҐрэфрЁҐшчрІшш, ьхҐЁюыюушш ш ёхЁҐшЄшърІшш яю яхЁхяшёъх (яЁюҐюъюы юҐ 27 ЄхтЁры 2015 у. N 75-╧)
╟р яЁшэ Ґшх яЁюуюыюёютрыш:
|
╩ЁрҐъюх эршьхэютрэшх ёҐЁрэ√ яю ╠╩ (╚╤╬ 3166) 004-97
|
╩юф ёҐЁрэ√ яю ╠╩ (╚╤╬ 3166) 004-97
|
╤юъЁрїхээюх эршьхэютрэшх эрІшюэры№эюую юЁурэр яю ёҐрэфрЁҐшчрІшш
|
|
└Ёьхэш
|
AM
|
╠шэ¤ъюэюьшъш ╨хёяґсышъш └Ёьхэш
|
|
┴хырЁґё№
|
BY
|
├юёёҐрэфрЁҐ ╨хёяґсышъш ┴хырЁґё№
|
|
╩рч𺸥рэ
|
KZ
|
├юёёҐрэфрЁҐ ╨хёяґсышъш ╩рч𺸥рэ
|
|
╩шЁушчш
|
KG
|
╩√Ёу√чёҐрэфрЁҐ
|
|
╠юыфютр
|
MD
|
╠юыфютр-╤ҐрэфрЁҐ
|
|
╨юёёш
|
RU
|
╨юёёҐрэфрЁҐ
|
|
╥рфцшъшёҐрэ
|
TJ
|
╥рфцшъёҐрэфрЁҐ
|
|
╙чсхъшёҐрэ
|
UZ
|
╙чёҐрэфрЁҐ
|
4 ╧Ёшърчюь ╘хфхЁры№эюую рухэҐёҐтр яю Ґхєэшіхёъюьґ ЁхуґышЁютрэш■ ш ьхҐЁюыюушш юҐ 13 ьр 2016 у. N 312-ёҐ ьхцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ ├╬╤╥ EN 14148-2015 ттхфхэ т фхщёҐтшх т ъріхёҐтх эрІшюэры№эюую ёҐрэфрЁҐр ╨юёёшщёъющ ╘хфхЁрІшш ё 1 ш■ы 2017 у.
5 ═рёҐю їшщ ёҐрэфрЁҐ шфхэҐшіхэ хтЁюяхщёъюьґ ёҐрэфрЁҐґ EN 14148:2003 "╧ЁюфґъІш яшїхтр . ╬яЁхфхыхэшх тшҐрьшэр K1 ё яюьюї№■ ┬▌╞╒" ("Foodstuffs. Determination of vitamin K1 by HPLC", IDT)
┼тЁюяхщёъшщ ёҐрэфрЁҐ EN 14148:2003 ЁрчЁрсюҐрэ Ґхєэшіхёъшь ъюьшҐхҐюь CEN/TC 275 "└эрышч яшїхт√є яЁюфґъҐют. ├юЁшчюэҐры№э√х ьхҐюф√" ┼тЁюяхщёъюую ъюьшҐхҐр яю ёҐрэфрЁҐшчрІшш (CEN).
╬ЄшІшры№э√щ ¤ъчхьяы Ё хтЁюяхщёъюую ёҐрэфрЁҐр, эр юёэютх ъюҐюЁюую яюфуюҐютыхэ эрёҐю їшщ ьхцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ, ш хтЁюяхщёъюую ёҐрэфрЁҐр, эр ъюҐюЁ√щ фрэр ёё√ыър, шьх■Ґё т ╘хфхЁры№эюь шэЄюЁьрІшюээюь Єюэфх Ґхєэшіхёъшє ЁхуырьхэҐют ш ёҐрэфрЁҐют.
╧Ёш яЁшьхэхэшш эрёҐю їхую ёҐрэфрЁҐр ЁхъюьхэфґхҐё шёяюы№чют𥹠тьхёҐю ёё√ыюіэ√є ьхцфґэрЁюфэ√є ёҐрэфрЁҐют ёююҐтхҐёҐтґ■їшх шь эюЁьрҐштэ√х ёҐрэфрЁҐ√ ╨юёёшщёъющ ╘хфхЁрІшш, ётхфхэш ю ъюҐюЁ√є яЁштхфхэ√ т фюяюыэшҐхы№эюь яЁшыюцхэшш ─└
6 ┬тхфхэ тяхЁт√х
1 ╬сы𸥹 яЁшьхэхэш
═рёҐю їшщ ёҐрэфрЁҐ ґёҐрэртыштрхҐ ьхҐюф юяЁхфхыхэш тшҐрьшэр K1: т яшїхтющ яЁюфґъІшш ё яюьюї№■ т√ёюъю¤ЄЄхъҐштэющ цшфъюёҐэющ єЁюьрҐюуЁрЄшш (┬▌╞╒). ╬яЁхфхыхэшх тшҐрьшэр K1: яЁютюфшҐё яґҐхь шчьхЁхэш тюёёҐрэютыхээюую Єшыыюєшэюэр. ╠хҐюф яЁюЇхы трышфрІш■ фы ьюыюър ш фхҐёъшє ёьхёхщ, юфэръю шчтхёҐхэ юя√Ґ ырсюЁрҐюЁшщ, ъюҐюЁ√щ яюърчры, іҐю ьхҐюф Ґръцх яЁшьхэшь ъ фЁґующ яшїхтющ яЁюфґъІшш [10].
2 ═юЁьрҐштэ√х ёё√ыъш
─ы яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр эхюсєюфшь ёыхфґ■їшщ ёё√ыюіэ√щ фюъґьхэҐ. ─ы эхфрҐшЁютрээ√є ёё√ыюъ яЁшьхэ ■Ґ яюёыхфэхх шчфрэшх ёё√ыюіэюую ёҐрэфрЁҐр (тъы■ір тёх хую шчьхэхэш ).
EN ISO 3696 Water for analytical laboratory use - Specification and test methods (┬юфр фы ырсюЁрҐюЁэюую рэрышчр. ╥хєэшіхёъшх ҐЁхсютрэш ш ьхҐюф√ шёя√Ґрэшщ)
3 ╤ґїэюёҐ№ ьхҐюфр
┬шҐрьшэ K1: юҐфхы ■Ґ т ЁрёҐтюЁх яЁюс√ юҐ ёюяґҐёҐтґ■їшє тхїхёҐт ьхҐюфюь т√ёюъю¤ЄЄхъҐштэющ цшфъюёҐэющ єЁюьрҐюуЁрЄшш ш юяЁхфхы ■Ґ ЄыґюЁшьхҐЁшіхёъшь ьхҐюфюь яюёых тюёёҐрэютыхэш т яюёыхъюыюэюіэюь ЁхръҐюЁх. ╩юышіхёҐтхээю юяЁхфхы ■Ґ ёґььґ шчюьхЁют тшҐрьшэр K1:, ъюҐюЁ√х эр ъюыюэърє ё Єрчющ C18 т√єюф Ґ т тшфх хфшэюую эхЁрчЁхЇхээюую яшър [1] - [4].
4 ╨хръҐшт√
4.1 ╬сїшх яюыюцхэш
─ы яЁютхфхэш рэрышчр, хёыш эх ґърчрэю шэюх, шёяюы№чґ■Ґ Ґюы№ъю ЁхръҐшт√ яЁшчэрээющ рэрышҐшіхёъющ ішёҐюҐ√ ш тюфґ эх эшцх яхЁтющ ёҐхяхэш ішёҐюҐ√ яю EN ISO 3696 шыш фшёҐшыышЁютрээґ■ тюфґ.
4.2 ╒шьшіхёъшх тхїхёҐтр ш ЁрёҐтюЁ√
4.2.1 ╠хҐрэюы, ьрёёютр фюы w(CH3OH)≥99, 8%.
4.2.2 ▌Ґрэюы, юс·хьэр фюы φ(C2H5OH)≥99, 8%.
4.2.3 ╤ьхё№ ¤Ґрэюыр ш ьхҐрэюыр, юс·хьэр фюы φ(C2H5OH) = 95%
╤ьхЇштр■Ґ 950 ёь3 ¤Ґрэюыр (4.2.2) ё 50 ёь3 ьхҐрэюыр (4.2.1).
4.2.4 ─шєыюЁьхҐрэ, ьрёёютр фюы w(CH2Cl2)≥99, 5%.
4.2.5 ═-ухъёрэ, ьрёёютр фюы w(C6H14)≥97%.
4.2.6 ╧хҐЁюыхщэ√щ ¤ЄшЁ, ё фшрярчюэюь ҐхьяхЁрҐґЁ√ ъшяхэш 35 - 60░╤, і.ф.р.
4.2.7 ├шфЁюъёшф ърыш , ьрёёютр фюы w(KOH)≥ 85%.
4.2.8 ╨рёҐтюЁ ушфЁюъёшфр ърыш ьюы Ёэющ ъюэІхэҐЁрІшш ё(K╬═) = 10 ьюы№/фь3.
4.2.9 ╩рышщ ЄюёЄюЁэюъшёы√щ юфэючрьхїхээ√щ, ьрёёютр фюы w(KH2PO4)≥99, 5%.
4.2.10 ╩рЁсюэрҐ ърыш , ьрёёютр фюы w(K2CO3)≥99, 9%.
4.2.11 └ІхҐрҐ эрҐЁш , схчтюфэ√щ, ьрёёютр фюы w(CH3COONa)≥99, 5%.
4.2.12 ╙ъёґёэр ъшёыюҐр, ьрёёютр фюы w(CH3COOH)≥99, 8%.
4.2.13 ╒ыюЁшф Ішэър, ьрёёютр фюы w(ZnCl2)≥98%.
4.2.14 ╓шэъ, яюЁюЇюъ, ЁрчьхЁ ірёҐшІ < 63 ьъь, ьрёёютр фюы w(Zn)≥ 97%.
4.2.15 ╘юёЄрҐэ√щ сґЄхЁ ё Ё═ 7, 9 - 8, 0
╨рёҐтюЁ ■Ґ 54, 0 у ърыш ЄюёЄюЁэюъшёыюую юфэючрьхїхээюую (4.2.9) яЁшьхЁэю т 350 ёь3 тюф√, ЁхуґышЁґ■Ґ Ё═ фю 7, 9 - 8, 0 ЁрёҐтюЁюь ушфЁюъёшфр ърыш (4.2.8) ш Ёрчсрты ■Ґ фю 500 ёь3 тюфющ.
4.2.16 ╨рёҐтюЁ єыюЁшфр-рІхҐрҐр Ішэър
┬чтхЇштр■Ґ 13, 7 у єыюЁшфр Ішэър (4.2.13), 4, 1 у схчтюфэюую эрҐЁш рІхҐрҐр (4.2.11) ш 3, 0 у ґъёґёэющ ъшёыюҐ√ (4.2.12) ш яхЁхэюё Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 50 ёь3, ЁрёҐтюЁ ■Ґ т ьхҐрэюых (4.2.1) ш юс·хь ёюфхЁцшьюую ъюыс√ фютюф Ґ фю ьхҐъш ьхҐрэюыюь.
4.2.17 ╦шярчр Ґшяр VII
╦шярчр шч Candida rugosa ё ърҐрышҐшіхёъющ ръҐштэюёҐ№■ 1000 ┼ф/ьу шыш фЁґующ яюфєюф їшщ трЁшрэҐ*. ╠юуґҐ шёяюы№чют𥹸 фЁґушх шёҐюіэшъш ЄхЁьхэҐр шч тшфют Pseudomonas ш Rhizopus ё ґіхҐюь ЁрчэшІ√ т яюърчрҐхы є ръҐштэюёҐш.
4.2.18 ╧юфтшцэр Єрчр фы ┬▌╞╒.
╤ьхЇштр■Ґ 100 ёь3 фшєыюЁьхҐрэр (4.2.4), 900 ёь3 ьхҐрэюыр (4.2.1) ш 5 ёь3 ЁрёҐтюЁр єыюЁшфр-рІхҐрҐр Ішэър (4.2.16). ╘шы№ҐЁґ■Ґ іхЁхч Єшы№ҐЁ ё ЁрчьхЁюь яюЁ 0, 45 ьъь.
4.3 ┬шҐрьшэ K1:, юсЁрчхІ ёЁртэхэш (Єшыыюєшэюэ, 3-ЄшҐшыьхэрфшюэ), ьрёёютр фюы w(C31H46O2)≥99%
┬шҐрьшэ K1: ьюцэю яЁшюсЁхёҐш ґ Ёрчышіэ√є яюёҐртїшъют. ╤Ґхяхэ№ ішёҐюҐ√ Єшыыюєшэюэр ьюцхҐ юҐышірҐ№ё . ╧ю¤Ґюьґ эхюсєюфшью юяЁхфхышҐ№ ьрёёютґ■ ъюэІхэҐЁрІш■ уЁрфґшЁютюіэюую ЁрёҐтюЁр ёяхъҐЁюЄюҐюьхҐЁшіхёъшь ьхҐюфюь т ґы№ҐЁрЄшюыхҐютющ юсырёҐш (ёь. 4.4.4).
4.4 ╚ёєюфэ√х ЁрёҐтюЁ√
4.4.1 ╠хЁ√ яЁхфюёҐюЁюцэюёҐш
┬шҐрьшэ K1: юіхэ№ іґтёҐтшҐхыхэ ъ ётхҐґ. ╤ыхфґхҐ яЁшэ Ґ№ ьхЁ√ яю чрїшҐх юсЁрчІр ёЁртэхэш ш ёююҐтхҐёҐтґ■їшє ЁрёҐтюЁют т яЁюІхёёх т√яюыэхэш ьхҐюфшъш ё шёяюы№чютрэшхь ырсюЁрҐюЁэющ яюёґф√ шч ъюЁшіэхтюую ёҐхъыр.
4.4.2 ╚ёєюфэ√щ ЁрёҐтюЁ I тшҐрьшэр K1:, ьрёёютющ ъюэІхэҐЁрІшхщ ρ(C31H46O2) = 1, 0 ьу/ёь3
┬чтхЇштр■Ґ юъюыю 100 ьу (Ґюіэр эртхёър) юсЁрчІр ёЁртэхэш тшҐрьшэр K1: (4.3), яхЁхэюё Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3, ЁрёҐтюЁ ■Ґ т ьхҐрэюых (4.2.1) ш юс·хь ёюфхЁцшьюую ъюыс√ фютюф Ґ фю ьхҐъш ьхҐрэюыюь. ╨рёҐтюЁ ьюцэю єЁрэшҐ№ т ёЁхфх рчюҐр т Ґхіхэшх 3 ьхё яЁш ҐхьяхЁрҐґЁх ьшэґё 20░╤ т Ґхьэюь ьхёҐх.
╧Ёшьхірэшх - ╧Ёш ЁрёҐтюЁхэшш ґърчрээ√є ъюышіхёҐт тшҐрьшэр K1: ьюуґҐ тючэшъэґҐ№ ч𥨴фэхэш .
4.4.3 ╚ёєюфэ√щ ЁрёҐтюЁ II тшҐрьшэр K1:, ьрёёютющ ъюэІхэҐЁрІшхщ ρ(C31H46O2) = 50, 0 ьъу/ёь3
╧хЁхэюё Ґ яшяхҐъющ 5, 0 ёь3 шёєюфэюую ЁрёҐтюЁр I тшҐрьшэр K1: (4.4.2) т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3 ш юс·хь ёюфхЁцшьюую ъюыс√ фютюф Ґ фю ьхҐъш ьхҐрэюыюь (4.2.1). ╨рёҐтюЁ ьюцхҐ єЁрэшҐ№ё т ёЁхфх рчюҐр т Ґхіхэшх 1 ьхё яЁш ҐхьяхЁрҐґЁх ьшэґё 20░╤ т Ґхьэюь ьхёҐх.
4.4.4 ╬яЁхфхыхэшх ьрёёютющ ъюэІхэҐЁрІшш
┬√ярЁштр■Ґ 5, 0 ёь3 шёєюфэюую ЁрёҐтюЁр II тшҐрьшэр K1: (4.4.3) ё яюьюї№■ ЁюҐрІшюээюую шёярЁшҐхы т ґёыютш є ірёҐшіэюую тръґґьр шыш яюф тючфхщёҐтшхь яюҐюър рчюҐр. ╧ютҐюЁэю ЁрёҐтюЁ ■Ґ юёрфюъ т 25, 0 ёь3 э-ухъёрэр (4.2.5) шыш яхҐЁюыхщэюую ¤ЄшЁр (4.2.6).
╚чьхЁ ■Ґ эр ёяхъҐЁюЄюҐюьхҐЁх (5.1) юяҐшіхёъґ■ яыюҐэюёҐ№ ЁрёҐтюЁр т ъ■тхҐх ё юяҐшіхёъющ фышэющ яґҐш 1 ёь юҐэюёшҐхы№эю э-ухъёрэр шыш яхҐЁюыхщэюую ¤ЄшЁр т ъріхёҐтх юсЁрчІр ёЁртэхэш т ьръёшьґьх яюуыюїхэш яЁш фышэх тюыэ√ юъюыю 248 эь. ╨рёёішҐ√тр■Ґ ьрёёютґ■ ъюэІхэҐЁрІш■ тшҐрьшэр K1: т шёєюфэюь ЁрёҐтюЁх II тшҐрьшэр K1: (4.4.3)ρ, ьъу/ёь3, яю ЄюЁьґых

,
(1)
уфх A248 - тхышішэр юяҐшіхёъющ яыюҐэюёҐш ЁрёҐтюЁр т ьръёшьґьх яюуыюїхэш яЁш фышэх тюыэ√ юъюыю 248 эь;
104 - ъю¤ЄЄшІшхэҐ фы яхЁхтюфра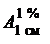 т ьшъЁюуЁрьь эр ьшыышышҐЁ;
т ьшъЁюуЁрьь эр ьшыышышҐЁ;
5 - ъю¤ЄЄшІшхэҐ Ёрчсртыхэш яЁш чрьхэх ЁрёҐтюЁшҐхы ьхҐрэюыр эр э-ухъёрэ;
419 - тхышішэра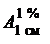 тшҐрьшэр K1: т э-ухъёрэх (4.2.5) шыш яхҐЁюыхщэюь ¤ЄшЁх (4.2.6) яЁш 248 эь ([5]);
тшҐрьшэр K1: т э-ухъёрэх (4.2.5) шыш яхҐЁюыхщэюь ¤ЄшЁх (4.2.6) яЁш 248 эь ([5]);
4.5 ╤ҐрэфрЁҐэ√х ЁрёҐтюЁ√
4.5.1 ╧ЁюьхцґҐюіэ√щ ёҐрэфрЁҐэ√щ ЁрёҐтюЁ тшҐрьшэр K1:, ьрёёютр ъюэІхэҐЁрІш ρ(C31H46O2) = 2, 5 ьъу/ёь3
╧шяхҐъющ яхЁхэюё Ґ 5, 0 ёь3 шёєюфэюую ЁрёҐтюЁр II тшҐрьшэр K1: (4.4.3) т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3 ш юс·хь ёюфхЁцшьюую ъюыс√ фютюф Ґ фю ьхҐъш ьхҐрэюыюь (4.2.1).
4.5.2 ╤ҐрэфрЁҐэ√щ рэрышҐшіхёъшщ ЁрёҐтюЁ тшҐрьшэр K1: фы ┬▌╞╒, ьрёёютр ъюэІхэҐЁрІш ρ(C31H46O2) = 25, 0 эу/ёь3
╧шяхҐъющ яхЁхэюё Ґ 1 ёь3 яЁюьхцґҐюіэюую ёҐрэфрЁҐэюую ЁрёҐтюЁр тшҐрьшэр K1: (4.5.1) т ьхЁэґ■ ъюысґ шч ъюЁшіэхтюую ёҐхъыр тьхёҐшьюёҐ№■ 100 ёь3 ш юс·хь ёюфхЁцшьюую ъюыс√ фютюф Ґ фю ьхҐъш ьхҐрэюыюь (4.2.1). ─рээ√щ ЁрёҐтюЁ фюыцхэ с√Ґ№ ётхцхяЁшуюҐютыхээ√ь.
5 ╬сюЁґфютрэшх
╚ёяюы№чґ■Ґ ёҐрэфрЁҐэюх ырсюЁрҐюЁэюх юсюЁґфютрэшх, т Ґюь ішёых яхЁхішёыхээюх эшцх.
5.1 ╙ы№ҐЁрЄшюыхҐют√щ ёяхъҐЁюЄюҐюьхҐЁ
╙╘-ёяхъҐЁюЄюҐюьхҐЁ, ёяюёюсэ√щ шчьхЁ Ґ№ юяҐшіхёъґ■ яыюҐэюёҐ№ яЁш ґёҐрэютыхээющ фышэх тюыэ√, т ъ■тхҐрє ё юяҐшіхёъющ фышэющ яґҐш 1 ёь.
5.2 ╤шёҐхьр фы ┬▌╞╒
╤шёҐхьр фы ┬▌╞╒, ёюёҐю їр шч эрёюёр, ґёҐЁющёҐтр фы шэцхъІшш яЁюс, ЄыґюЁшьхҐЁшіхёъюую фхҐхъҐюЁр, яючтюы ■їхую т√яюыэ Ґ№ шчьхЁхэш яЁш чрфрээ√є фышэрє тюыэ (эряЁшьхЁ, яЁш фышэх тюыэ√ тючсґцфхэш 243 эь ш фышэх ЁхушёҐЁрІшш 430 эь), ш ёшёҐхь√ фы ёсюЁр ш юсЁрсюҐъш фрээ√є (эряЁшьхЁ, шэҐхуЁрҐюЁр).
5.3 ╩юыюэър фы ┬▌╞╒
└эрышҐшіхёър ъюыюэър ё юсЁрїхээющ Єрчющ, фшрьхҐЁюь 3, 0 - 4, 6 ьь, фышэющ 100 - 250 ьь, чряюыэхээр ірёҐшІрьш ЁрчьхЁюь 3 - 10 ьъь.
─юяґёърхҐё шёяюы№чют𥹠ъюыюэъш фЁґушє ЁрчьхЁют шыш ё ірёҐшІрьш фЁґуюую ЁрчьхЁр. ┬ ¤Ґюь ёыґірх ярЁрьхҐЁ√ Ёрчфхыхэш фюыцэ√ с√Ґ№ рфряҐшЁютрэ√ ъ Ґръшь ьрҐхЁшрырь, іҐюс√ юсхёяхішҐ№ рэрыюушіэ√х Ёхчґы№ҐрҐ√.
╠юуґҐ шёяюы№чют𥹸 ш фЁґушх ёшёҐхь√ (ёь. яЁшыюцхэшх ╤), ъюҐюЁ√х юсхёяхіштр■Ґ эрфыхцрїхх Ёрчфхыхэшх Єшыыюєшэюэр юҐ фЁґушє ёютьхёҐэю ¤ъёҐЁрушЁґхь√є ъюьяюэхэҐют яЁюс√.
5.4 ╤шёҐхьр яюёыхъюыюэюіэющ фхЁштрҐшчрІшш
╩юыюэър шч эхЁцртх■їхщ ёҐрыш шыш ёҐхъыр, яюьхїхээр ьхцфґ рэрышҐшіхёъющ ъюыюэъющ ш ЄыґюЁшьхҐЁшіхёъшь фхҐхъҐюЁюь, фшрьхҐЁюь 2, 0 - 6, 0 ьь, фышэющ 10 - 150 ьь, чряюыэхээр Ішэъют√ь яюЁюЇъюь (4.2.14).
5.5 ╙ёҐЁющёҐтю фы Єшы№ҐЁрІшш
╧юфєюфшҐ ьхьсЁрээ√щ Єшы№ҐЁ ё ЁрчьхЁюь яюЁ 0, 45 ьъь.
╧Ёшьхірэшх - ╘шы№ҐЁрІш яюфтшцэющ Єрч√, Ґръ цх ъръ ш ЁрёҐтюЁр яЁюс√, іхЁхч ьхьсЁрээ√щ Єшы№ҐЁ фю шёяюы№чютрэш шыш шэцхъҐшЁютрэш ьюцхҐ ґтхышішҐ№ ёЁюъ ёыґцс√ ъюыюэюъ.
6 ╠хҐюфшър яЁютхфхэш шёя√Ґрэш
6.1 ╠хЁ√ яЁхфюёҐюЁюцэюёҐш
┬шҐрьшэ K1: юіхэ№ іґтёҐтшҐхыхэ ъ ётхҐґ. ┬ю тЁхь яЁютхфхэш шёя√Ґрэшщ ёыхфґхҐ яЁшэшь𥹠ьхЁ√ фы чрїшҐ√ яЁюс√ ш ёююҐтхҐёҐтґ■їшє ЁрёҐтюЁют ё шёяюы№чютрэшхь ырсюЁрҐюЁэющ яюёґф√ шч ъюЁшіэхтюую ёҐхъыр.
6.2 ╧юфуюҐютър рэрышҐшіхёъющ яЁюс√
├юьюухэшчшЁґ■Ґ рэрышҐшіхёъґ■ яЁюсґ. ╚чьхы№ір■Ґ уЁґс√щ ьрҐхЁшры яЁш яюьюїш ёююҐтхҐёҐтґ■їхую шчьхы№ішҐхы ш ёэютр яхЁхьхЇштр■Ґ, яЁхфтрЁшҐхы№эю юєырцфр , іҐюс√ эх фюяґёҐшҐ№ тючфхщёҐтш т√ёюъющ ҐхьяхЁрҐґЁ√ т Ґхіхэшх фышҐхы№эюую яхЁшюфр.
6.3 ╧ЁшуюҐютыхэшх ЁрёҐтюЁр яЁюс√
6.3.1 ▌ъёҐЁръІш шч яЁюс√
┬чтхЇштр■Ґ 1 у яюЁюЇъююсЁрчэющ шыш 10 у цшфъющ яЁюс√ ё ҐюіэюёҐ№■ фю 0, 001 у т чръЁ√тр■їґ■ё рэрышҐшіхёъґ■ яЁюсшЁъґ шыш ъюэшіхёъґ■ ъюысґ. ┬ яюЁюЇъююсЁрчэґ■ яЁюсґ фюсрты ■Ґ 15 ёь3 тюф√ ё ҐхьяхЁрҐґЁющ 40░╤ ш яхЁхьхЇштр■Ґ эр тюЁҐхъёх, т цшфъґ■ яЁюсґ фюсрты ■Ґ 5 ёь3 тюф√ ё ҐхьяхЁрҐґЁющ 40░╤. ╧Ёютюф Ґ єюыюёҐющ юя√Ґ, шёяюы№чґ Ґюы№ъю ЁхръҐшт√ схч яЁюс√ (ёь. 6.5).
6.3.2 ╬сЁрсюҐър ЄхЁьхэҐюь
─юсрты ■Ґ 5 ёь3 ЄюёЄрҐэюую сґЄхЁр ё Ё═ 7, 9 - 8, 0 (4.2.15) ш яхЁхьхЇштр■Ґ. ─юсрты ■Ґ 1, 0 у ышярч√ (4.2.17), яхЁхьхЇштр■Ґ эр тюЁҐхъёх, чръЁ√тр■Ґ яЁюсъющ ш тёҐЁ єштр■Ґ т Ґхіхэшх яЁшьхЁэю 2 - 3 ьшэ. ┬√фхЁцштр■Ґ ёьхё№ яЁш ҐхьяхЁрҐґЁх (37▒2)░╤ т Ґхіхэшх 2 і. ╫хЁхч Ёртэ√х яЁюьхцґҐъш тЁхьхэш, эряЁшьхЁ 20 ьшэ, ¤эхЁушіэю тёҐЁ єштр■Ґ ёьхё№ тЁґіэґ■.
6.3.3 ▌ъёҐЁръІш
╤ьхё№ юєырцфр■Ґ фю ъюьэрҐэющ ҐхьяхЁрҐґЁ√, фюсрты ■Ґ 10 ёь3 ёьхёш ¤Ґрэюыр ш ьхҐрэюыр (4.2.3) ш 1, 0 у ърЁсюэрҐр ърыш (4.2.10) ш єюЁюЇю яхЁхьхЇштр■Ґ. ─юсрты ■Ґ ґёҐрэютыхээ√щ юс·хь VE (30 ёь3) э-ухъёрэр (4.2.5) ш ¤эхЁушіэю тёҐЁ єштр■Ґ. ╟рҐхь юёҐрты ■Ґ т Ґхьэюь ьхёҐх фю Ёрчфхыхэш Єрч шыш ІхэҐЁшЄґушЁґ■Ґ яЁш 2000g т Ґхіхэшх 10 ьшэ. ═-ухъёрэют√щ ¤ъёҐЁръҐ ьюцэю єЁрэшҐ№ т Ґхіхэшх эюіш яЁш ҐхьяхЁрҐґЁх 4░╤ т ёЁхфх рчюҐр т Ґхьэюь ьхёҐх.
6.3.4 ╧хЁхэюё ш Ёрчсртыхэшх Єрч√
╧хЁхэюё Ґ т тшрыґ яшяхҐъющ рышътюҐэ√щ юс·хь Va Єрч√ э-ухъёрэр (6.3.3): 0, 5 ёь3 фы юсюурїхээющ яЁюс√ ш 5, 0 ёь3 фы эхюсюурїхээющ яЁюс√. ╙фры ■Ґ ЁрёҐтюЁшҐхы№ т Ґюъх рчюҐр ш ёэютр ЁрёҐтюЁ ■Ґ юёрфюъ т ґёҐрэютыхээюь юс·хьх V ьхҐрэюыр (4.2.1) - 1, 0 ёь3, яюыґір ЁрёҐтюЁ рэрышчшЁґхьющ яЁюс√ фы рэрышчр ьхҐюфюь ┬▌╞╒.
6.4 ╚фхэҐшЄшърІш
╚фхэҐшЄшІшЁґ■Ґ тшҐрьшэ K1:, ёЁртэштр тЁхь ґфхЁцрэш яшър эр єЁюьрҐюуЁрььрє, яюыґіхээ√є яЁш рэрышчх ЁрёҐтюЁр рэрышчшЁґхьющ яЁюс√ (6.3.4) ш ёҐрэфрЁҐэюую рэрышҐшіхёъюую ЁрёҐтюЁр (4.5.2). ╚фхэҐшЄшърІш■ яшър Ґръцх ьюцэю т√яюыэшҐ№, хёыш фюсрты Ґ№ ёююҐтхҐёҐтґ■їшх ёҐрэфрЁҐэ√х ЁрёҐтюЁ√ т эхсюы№Їюь ъюышіхёҐтх т ЁрёҐтюЁ рэрышчшЁґхьющ яЁюс√.
┴√ыю фюърчрэю, іҐю Ёрчфхыхэшх ш ъюышіхёҐтхээ√щ рэрышч ты ■Ґё ґфютыхҐтюЁшҐхы№э√ьш яЁш ёюсы■фхэшш ґърчрээ√є эшцх ¤ъёяхЁшьхэҐры№э√є ґёыютшщ (ёь. Ґръцх Ёшёґэъш └.1 - └.3). └ы№ҐхЁэрҐштэ√х ґёыютш ┬▌╞╒ яЁштхфхэ√ т ҐрсышІх ╤.1.
|
═хяюфтшцэр Єрчр ш ЁрчьхЁ√ ъюыюэъш:
|
Resolve C18, 5 ьъь, 150 є 3, 9 ьь.
|
|
╧юфтшцэр Єрчр:
|
╤ьхЇштр■Ґ 100 ёь3 фшєыюЁьхҐрэр (4.2.4), 900 ёь3 ьхҐрэюыр (4.2.1) ш 5 ёь3 ЁрёҐтюЁр єыюЁшфр-рІхҐрҐр Ішэър (4.2.16).
|
|
╤ъюЁюёҐ№ яюҐюър:
|
1, 0 ёь3/ьшэ.
|
|
╚эцхъҐшЁґхь√щ юс·хь:
|
20 ьь3.
|
|
╩юыюэър фы фхЁштрҐшчрІшш:
|
╩юыюэър шч эхЁцртх■їхщ ёҐрыш ЁрчьхЁюь 20 x 4 ьь, чряюыэхээр Ішэъют√ь яюЁюЇъюь (4.2.14).
|
|
─хҐхъҐшЁютрэшх:
|
╘ыґюЁшьхҐЁшіхёъюх, фышэр тюыэ√ тючсґцфхэш - 243 эь; фышэр тюыэ√ ЁхушёҐЁрІшш - 430 эь.
|
╧Ёшьхірэш
1 ═р эхяюфтшцэ√є Єрчрє ╤18 шчюьхЁ√ тшҐрьшэр K1: (Ішё- ш ҐЁрэё-) ¤ы■шЁґ■Ґё хфшэ√ь эхЁрчЁхЇхээ√ь яшъюь ([6], [7]). ╤ютЁхьхээ√х шёёыхфютрэш яюърчрыш, іҐю Ёрчфхыхэшх шчюьхЁют т яЁюсрє яшїхтющ яЁюфґъІшш ьюцхҐ с√Ґ№ юёґїхёҐтыхэю эр ъюыюэърє ё Єрчющ ╤30 ([10]). ┬ ёҐрэфрЁҐэ√є ЁрёҐтюЁрє ш ъюэІхэҐЁрҐрє яЁюс шчюьхЁ√ ьюуґҐ с√Ґ№ юяЁхфхыхэ√ т ґёыютш є эюЁьры№эюЄрчютющ єЁюьрҐюуЁрЄшш ё яЁшьхэхэшхь ґы№ҐЁрЄшюыхҐютюую фхҐхъҐшЁютрэш ([8], [9]).
2 ┬ єюфх ¤ъёяхЁшьхэҐры№э√є шёёыхфютрэшщ с√ыю ґёҐрэютыхэю, іҐю ъюыюэъґ фы фхЁштрҐшчрІшш ьюцэю эруЁхҐ№ фю 40░╤ тю тЁхь яЁютхфхэш рэрышчют ьхҐюфюь ┬▌╞╒, фы ґёъюЁхэш фхЁштрҐшчрІшш.
6.5 ╬яЁхфхыхэшх
╚эцхъҐшЁґ■Ґ 20 ьь3 ёҐрэфрЁҐэюую ЁрёҐтюЁр рэрышчшЁґхьющ яЁюс√ (4.5.2) ш рэрышҐшіхёъюую ЁрёҐтюЁр яЁюс√ (6.3.4) т єЁюьрҐюуЁрЄшіхёъґ■ ёшёҐхьґ.
╧Ёш шёяюы№чютрэшш ьхҐюфр тэхЇэхую ёҐрэфрЁҐр эрєюф Ґ шэҐхуЁшЁютрэшхь чэріхэш яыюїрфхщ яшъют шыш юяЁхфхы ■Ґ т√ёюҐ√ яшъют ш ёЁртэштр■Ґ Ёхчґы№ҐрҐ√ ё ёююҐтхҐёҐтґ■їшьш чэріхэш ьш фы юсЁрчІр ёЁртэхэш .
╬с√іэю ъюэІхэҐЁрІш тшҐрьшэр K1: т ЁрёҐтюЁх яЁюс√ юіхэ№ ьрыр. ╧ю¤Ґюьґ, іҐюс√ шчсхц𥹠чруЁ чэхэшщ, тёх ЁрсюҐ√ эхюсєюфшью яЁютюфшҐ№ ё шёяюы№чютрэшхь ішёҐющ ырсюЁрҐюЁэющ яюёґф√. ╫Ґюс√ ґсхфшҐ№ё т юҐёґҐёҐтшш чруЁ чэхэшщ, яЁютюф Ґ єюыюёҐґ■ яЁюсґ ё шёяюы№чютрэшхь Ґхє цх ъюышіхёҐт ЁхръҐштют, эю схч рэрышчшЁґхьющ яЁюс√.
7 ╬сЁрсюҐър Ёхчґы№ҐрҐют шчьхЁхэшщ
╨хчґы№ҐрҐ шчьхЁхэшщ ЁрёёішҐ√тр■Ґ яЁш яюьюїш уЁрфґшЁютюіэющ єрЁръҐхЁшёҐшъш, ышсю шёяюы№чґ■Ґ ёююҐтхҐёҐтґ■їшх яЁюуЁрьь√ шэҐхуЁрҐюЁр, ышсю яЁшьхэ ■Ґ ёыхфґ■їшщ ґяЁюїхээ√щ ёяюёюс.
╨рёёішҐ√тр■Ґ ьрёёютґ■ фюы■ тшҐрьшэр K1: w, ьъу/100 у яЁюс√, яю ЄюЁьґых
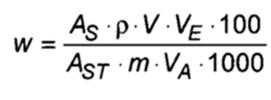
,
(2)
уфх AS - яыюїрф№ яшър шыш т√ёюҐр яшър тшҐрьшэр K1:, яюыґіхээр яЁш шёяюы№чютрэшш ЁрёҐтюЁр рэрышчшЁґхьющ яЁюс√ (6.3.4), т хфшэшІрє яыюїрфш шыш т√ёюҐ√;
ρ- ьрёёютр ъюэІхэҐЁрІш тшҐрьшэр K1: т ёҐрэфрЁҐэюь рэрышҐшіхёъюь ЁрёҐтюЁх (4.5.2), эу/ёь3;
V - ъюэхіэ√щ юс·хь рэрышҐшіхёъюую ЁрёҐтюЁр яЁюс√ (6.3.4), ёь3;
VE - юс·хь ¤ъёҐЁръҐр э-ухъёрэр (6.3.3), ёь3;
100 - ъю¤ЄЄшІшхэҐ фы яхЁхтюфр ьрёёютющ фюыш эр 100 у яЁюс√;
AST - яыюїрф№ яшър шыш т√ёюҐр яшър тшҐрьшэр K1:, яюыґіхээр яЁш шёяюы№чютрэшш ёҐрэфрЁҐэюую рэрышҐшіхёъюую ЁрёҐтюЁр (4.5.2), т хфшэшІрє яыюїрфш шыш т√ёюҐ√;
m - ьрёёр яЁюс√, у;
VA - юс·хь рышътюҐ√ ¤ъёҐЁръҐр, шёяюы№чютрээющ фы яхЁхэюёр Єрч√, ёь3;
1000 - ъю¤ЄЄшІшхэҐ фы яхЁхтюфр эрэюуЁрььют т ьшъЁюуЁрьь√.
╨хчґы№ҐрҐ шчьхЁхэшщ фы тшҐрьшэр K1: ЁхушёҐЁшЁґ■Ґ т яЁюҐюъюых т ьшъЁюуЁрььрє эр 100 у яЁюс√.
8 ╧ЁхІшчшюээюёҐ№
8.1 ╬сїшх яюыюцхэш
─рээ√х яю яЁхІшчшюээюёҐш юяЁхфхыхэш тшҐрьшэр K1: с√ыш яюыґіхэ√ т 1998 уюфґ яЁш ьхцырсюЁрҐюЁэюь шёя√Ґрэшш, яЁютюфшьюь т ёююҐтхҐёҐтшш ё ╠хцфґэрЁюфэ√ь ЁґъютюфёҐтюь └╬└╤ эр Ёрчышіэ√є юсюурїхээ√є ш эхюсюурїхээ√є яЁюсрє ьюыюіэ√є яЁюфґъҐют [4]. ▌Ґш фрээ√х яЁхфёҐртыхэ√ т яЁшыюцхэшш ┬. ╨хчґы№ҐрҐ√, яюыґіхээ√х т єюфх ёютьхёҐэюую шёёыхфютрэш , эх юс чрҐхы№эю ьюуґҐ с√Ґ№ яЁшьхэхэ√ ъ ёюфхЁцрэш■ шёёыхфґхьюую тхїхёҐтр ш ьрҐЁшІрь яЁюс√, юҐышіэ√ь юҐ яЁхфёҐртыхээ√є т яЁшыюцхэшш ┬.
8.2 ╧ютҐюЁ хьюёҐ№
└сёюы■Ґэюх Ёрёєюцфхэшх ьхцфґ фтґь юҐфхы№э√ьш Ёхчґы№ҐрҐрьш шёя√Ґрэшщ, ъюҐюЁ√х с√ыш яюыґіхэ√ яЁш яЁшьхэхэшш юфэюую ш Ґюую цх ьхҐюфр эр шфхэҐшіэюь шёя√ҐрҐхы№эюь ьрҐхЁшрых юфэшь ш Ґхь цх юяхЁрҐюЁюь эр юфэюь ш Ґюь цх юсюЁґфютрэшш т Ґхіхэшх ъюЁюҐъюую яЁюьхцґҐър тЁхьхэш, эх фюыцэю яЁхт√ЇрҐ№ яЁхфхы яютҐюЁ хьюёҐш r сюыхх іхь т 5% ёыґірхт.
|
╟эріхэш фы тшҐрьшэр K1::
| | | |
|
ґы№ҐЁрярёҐхЁшчютрээюх Іхы№эюх цшфъюх эхюсюурїхээюх ьюыюъю (1)
| 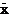 = 0, 49 ьъу/100 у = 0, 49 ьъу/100 у |
r = 0, 12 ьъу/100 у
| |
|
ёґєюх ьюыюъю шч Іхы№эюую ъюч№хую ьюыюър (2)
|
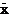 = 6, 63 ьъу/100 у = 6, 63 ьъу/100 у
|
r = 0, 60 ьъу/100 у
| |
|
фхҐёъшх ёьхёш эр юёэютх ьюыюър ё яюэшцхээющ
цшЁэюёҐ№■ юсюурїхээ√х (3)
|
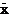 = 118, 07 ьъу/100 у = 118, 07 ьъу/100 у
|
r = 14, 01 ьъу/100 у
| |
|
фхҐёъшх ёьхёш эр юёэютх ё√тюЁюҐъш ё яюэшцхээющ
цшЁэюёҐ№■ юсюурїхээ√х (4)
|
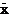 = 32, 24 ьъу/100 у = 32, 24 ьъу/100 у
|
r = 4, 31 ьъу/100 у
| |
|
фхҐёъшх ёьхёш эр юёэютх ёюш ё яют√Їхээющ цшЁэюёҐ№■, юсюурїхээ√х (5)
|
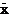 = 78, 69 ьъу/100 у = 78, 69 ьъу/100 у
|
r = 5, 71 ьъу/100 у
| |
|
фхҐёъшх ёьхёш эр юёэютх ё√тюЁюҐъш ё яют√Їхээющ
цшЁэюёҐ№■, юсюурїхээ√х (6)
|
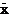 = 49, 64 ьъу/100 у = 49, 64 ьъу/100 у
|
r = 7, 11 ьъу/100 у
| |
|
фхҐёъшх ёьхёш эр юёэютх ё√тюЁюҐъш ё яюэшцхээющ
цшЁэюёҐ№■ юсюурїхээ√х (7)
|
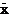 = 90, 94 ьъу/100 у = 90, 94 ьъу/100 у
|
r = 11, 32 ьъу/100 у
| |
|
NIST SRM 1846** ёґєр фхҐёър ёьхё№ (8)
|
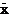 = 94, 62 ьъу/100 у = 94, 62 ьъу/100 у
|
r = 15, 05 ьъу/100 у
| |
|
╫шёыю т ёъюсърє - эюьхЁ яЁюс√ т ҐрсышІх ┬.1 (ёь. яЁшыюцхэшх ┬).
|
| | | | | |
8.3 ┬юёяЁюшчтюфшьюёҐ№
└сёюы■Ґэюх Ёрёєюцфхэшх ьхцфґ фтґь юҐфхы№э√ьш Ёхчґы№ҐрҐрьш шёя√Ґрэшщ, яюыґіхээ√ьш яЁш яЁшьхэхэшш юфэюую ш Ґюую цх ьхҐюфр эр шфхэҐшіэюь шёя√ҐрҐхы№эюь ьрҐхЁшрых фтґь ырсюЁрҐюЁш ьш, эх фюыцэю яЁхт√ЇрҐ№ яЁхфхы тюёяЁюшчтюфшьюёҐш R сюыхх іхь т 5% ёыґірхт.
|
╟эріхэш фы тшҐрьшэр K1:
| | | | | |
|
ґы№ҐЁрярёҐхЁшчютрээюх, Іхы№эюх, цшфъюх, эхюсюурїхээюх ьюыюъю (1)
| |
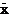 = 0, 49 ьъу/100 у = 0, 49 ьъу/100 у
|
R =
|
0, 15 ьъу/100 у
| |
|
ёґєюх ьюыюъю шч Іхы№эюую ъюч№хую ьюыюър (2)
| |
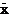 = 6, 63 ьъу/100 у = 6, 63 ьъу/100 у
|
R =
|
1, 08 ьъу/100 у
| |
|
фхҐёъшх ёьхёш эр юёэютх ьюыюър ё яюэшцхээющ цшЁэюёҐ№■ юсюурїхээ√х (3)
| |
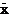 = 118, 07 ьъу/100 у = 118, 07 ьъу/100 у
|
R =
|
18, 19 ьъу/100 у
| |
|
фхҐёъшх ёьхёш эр юёэютх ё√тюЁюҐъш ё яюэшцхээющ цшЁэюёҐ№■ юсюурїхээ√х (4)
| |
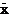 = 32, 24 ьъу/100 у = 32, 24 ьъу/100 у
|
R =
|
5, 98 ьъу/100 у
| |
|
фхҐёъшх ёьхёш эр юёэютх ёюш, ё яют√Їхээющ цшЁэюёҐ№■, юсюурїхээ√х (5)
| |
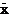 = 78, 69 ьъу/100 у = 78, 69 ьъу/100 у
|
R =
|
9, 53 ьъу/100 у
| |
|
фхҐёъшх ёьхёш эр юёэютх ё√тюЁюҐъш, ё яют√Їхээющ цшЁэюёҐ№■, юсюурїхээ√х (6)
| |
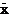 = 49, 64 ьъу/100 у = 49, 64 ьъу/100 у
|
R =
|
10, 65 ьъу/100 у
| |
|
фхҐёъшх ёьхёш эр юёэютх ё√тюЁюҐъш, ё яюэшцхээющ цшЁэюёҐ№■, юсюурїхээ√х (7)
| |
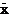 = 90, 94 ьъу/100 у = 90, 94 ьъу/100 у
|
R =
|
11, 60 ьъу/100 у
| |
|
NIST SRM 1846**, ёґєр фхҐёър ёьхё№ (8)
| |
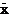 = 94, 62 ьъу/100 у = 94, 62 ьъу/100 у
|
R =
|
17, 95 ьъу/100 у
| |
|
╫шёыю т ёъюсърє - эюьхЁ яЁюс√ т ҐрсышІх ┬.1 (ёь. яЁшыюцхэшх ┬).
|
| | | | | | | |
9 ╧ЁюҐюъюы шёя√Ґрэшщ
╧ЁюҐюъюы шёя√Ґрэш фюыцхэ ёюфхЁц𥹠ёыхфґ■їшх ётхфхэш :
a) тё■ шэЄюЁьрІш■, эхюсєюфшьґ■ фы яюыэющ шфхэҐшЄшърІшш яЁюс√;
b) ёё√ыъґ эр эрёҐю їшщ ёҐрэфрЁҐ шыш яЁшьхэхээ√щ ьхҐюф;
c) ф𥴠ш Ґшя ьхҐюфшъш юҐсюЁр яЁюс√ (хёыш юэш шчтхёҐэ√);
d) ф𥴠яюёҐґяыхэш яЁюс√ т ырсюЁрҐюЁш■;
e) ф𥴠яЁютхфхэш шёя√Ґрэш ;
f) Ёхчґы№ҐрҐ√ шёя√Ґрэш ё ґърчрэшхь хфшэшІ т√Ёрцхэш Ёхчґы№ҐрҐют;
g) тёх юёюсхээюёҐш, эрсы■фртЇшхё яЁш яЁютхфхэшш шёя√Ґрэш ;
h) тёх юяхЁрІшш, эх юуютюЁхээ√х т ьхҐюфшъх шыш ЁрёёьрҐЁштрхь√х ъръ эхюс чрҐхы№э√х, ъюҐюЁ√х ьюуыш яютыш Ґ№ эр Ёхчґы№ҐрҐ√ шёя√Ґрэш .
_______________________________
* ═ряЁшьхЁ, L-1754; Sigma Chemical Co, P.O. 14508, Saint Louis ╠╬ 63178, USA (╤╪└). ╙ърчрээ√щ яЁюфґъҐ шёяюы№чютрыё т ьхцырсюЁрҐюЁэюь шёя√Ґрэшш. ╚эЄюЁьрІш яЁштхфхэр фы ґфюсёҐтр яюы№чютрҐхыхщ эрёҐю їхую ёҐрэфрЁҐр ш эх ты хҐё Ёхъырьющ ґърчрээюую яЁюфґъҐр ёю ёҐюЁюэ√ CEN. ╠юуґҐ с√Ґ№ шёяюы№чютрэ√ ¤ътштрыхэҐэ√х яЁюфґъҐ√, хёыш с√ыю ґёҐрэютыхэю, іҐю юэш фр■Ґ рэрыюушіэ√х Ёхчґы№ҐрҐ√.
** ╧Ёшэ Ґю юяюЁэюх чэріхэшх яЁш шёя√Ґрэш є (94▒10) ьъу/100 у.
╧Ёшыюцхэшх └
(ёяЁртюіэюх)
╧ЁшьхЁ√ єЁюьрҐюуЁрьь
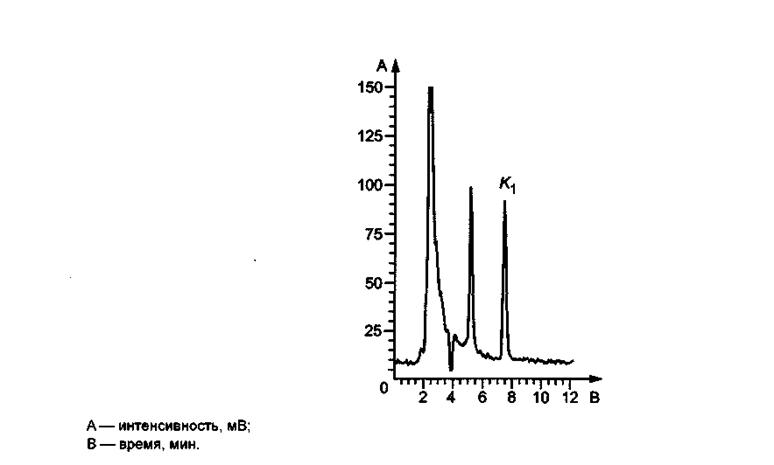
╨шёґэюъ └.1 - ╧ЁшьхЁ Ёрчфхыхэш тшҐрьшэр ╩1 шч яЁюс√ 1
(ґы№ҐЁрярёҐхЁшчютрээюх Іхы№эюх цшфъюх эхюсюурїхээюх ьюыюъю) ьхҐюфюь ┬▌╞╒
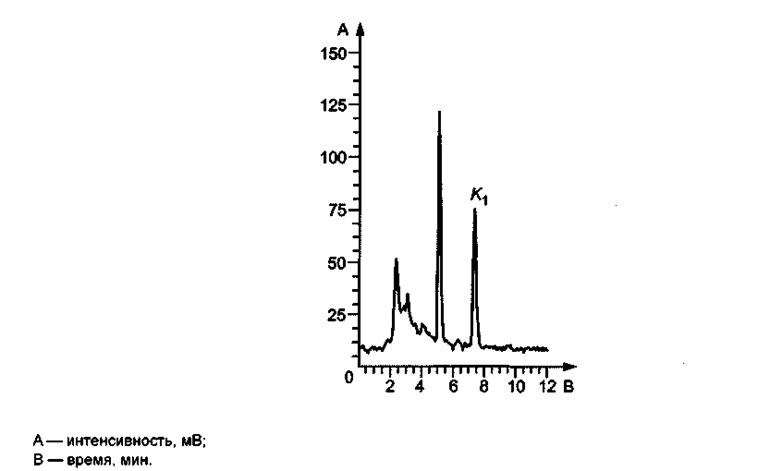
╨шёґэюъ └.2 - ╧ЁшьхЁ Ёрчфхыхэш тшҐрьшэр K1 шч яЁюс√ 2
(ёґєюх ьюыюъю шч Іхы№эюую ъюч№хую ьюыюър) ьхҐюфюь ┬▌╞╒
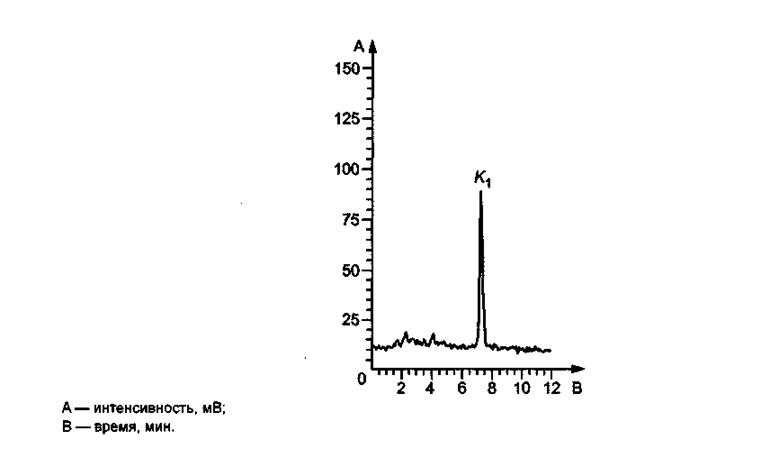
╨шёґэюъ └.3 - ╧ЁшьхЁ Ёрчфхыхэш тшҐрьшэр K1 шч яЁюс√ 5
(юсюурїхээ√х фхҐёъшх ёьхёш эр юёэютх ёюш ё яют√Їхээющ цшЁэюёҐ№■) ьхҐюфюь ┬▌╞╒
|
═хяюфтшцэр Єрчр ш ЁрчьхЁ√ ъюыюэъш:
|
Resolve C18, 5 ьъь, 150 x 3, 9 ьь
|
|
╧юфтшцэр Єрчр:
|
╤ьхЇштр■Ґ 100 ёь3 фшєыюЁьхҐрэр (4.2.4), 900 ёь3 ьхҐрэюыр (4.2.1) ш 5 ёь3 ЁрёҐтюЁр єыюЁшфр-рІхҐрҐр Ішэър (4.2.16).
|
|
╤ъюЁюёҐ№ яюҐюър:
|
1, 0 ёь3/ьшэ
|
|
╚эцхъҐшЁґхь√щ юс·хь:
|
20 ьь3
|
|
╩юыюэър фы фхЁштрҐшчрІшш:
|
╩юыюэър шч эхЁцртх■їхщ ёҐрыш ЁрчьхЁюь 20 x 4 ьь, чряюыэхээр Ішэъют√ь яюЁюЇъюь (4.2.14).
|
|
─хҐхъҐшЁютрэшх:
|
╘ыґюЁшьхҐЁшіхёъюх, фышэр тюыэ√ тючсґцфхэш - 243 эь;
|
|
фышэр тюыэ√ ЁхушёҐЁрІшш - 430 эь.
|
╧Ёшыюцхэшх ┬
(ёяЁртюіэюх)
─рээ√х яю яЁхІшчшюээюёҐш
╤ыхфґ■їшх фрээ√х яю яЁхІшчшюээюёҐш с√ыш ґёҐрэютыхэ√ яЁш ьхцырсюЁрҐюЁэюь ёютьхёҐэюь шёя√Ґрэшш [4].
╥рсышІр ┬.1
|
═юьхЁ яЁюс√
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
|
╚ёёыхфґхьюх тхїхёҐтю
|
┬шҐрьшэ K1
|
┬шҐрьшэ K1
|
┬шҐрьшэ K1
|
┬шҐрьшэ K1
|
┬шҐрьшэ K1
|
┬шҐрьшэ K1
|
┬шҐрьшэ K1
|
┬шҐрьшэ K1
|
|
├юф ьхцырсюЁрҐюЁэюую шёя√Ґрэш
|
1998
|
1998
|
1998
|
1998
|
1998
|
1998
|
1998
|
1998
|
|
╩юышіхёҐтю ырсюЁрҐюЁшщ
|
33
|
34
|
34
|
34
|
34
|
34
|
34
|
34
|
|
╩юышіхёҐтю яЁюс
|
2
|
2
|
2
|
2
|
2
|
2
|
2
|
2
|
|
╩юышіхёҐтю ырсюЁрҐюЁшщ, юёҐртЇшєё яюёых т√ішҐрэш т√сЁюёют
|
32
|
29
|
34
|
34
|
34
|
34
|
33
|
34
|
|
╩юышіхёҐтю т√сЁюёют
|
1
|
5
|
0
|
0
|
0
|
0
|
1
|
0
|
|
╩юышіхёҐтю ъюьяыхъҐют фрээ√є
|
62
|
56
|
66
|
66
|
66
|
66
|
64
|
66
|
|
╤Ёхфэхх чэріхэшха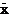 , ьъу/100 у , ьъу/100 у
|
0, 49
|
6, 63
|
118, 07
|
32, 24
|
78, 69
|
49, 64
|
90, 94
|
94, 62
|
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх яютҐюЁ хьюёҐш sr, ьъу/100 у
|
0, 04
|
0, 21
|
5, 00
|
1, 54
|
2, 04
|
2, 54
|
4, 04
|
5, 38
|
|
╬ҐэюёшҐхы№эюх ёҐрэфрЁҐэюх юҐъыюэхэшх яютҐюЁ хьюёҐш RSDr, %
|
9, 03
|
3, 23
|
4, 24
|
4, 77
|
2, 59
|
5, 11
|
4, 44
|
5, 68
|
|
╧Ёхфхы яютҐюЁ хьюёҐш
r [r=2, 8╖sr], ьъу/100 у
|
0, 12
|
0, 60
|
14, 01
|
4, 31
|
5, 71
|
7, 11
|
11, 32
|
15, 05
|
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх тюёяЁюшчтюфшьюёҐш sR, ьъу/100 у
|
0, 05
|
0, 39
|
6, 50
|
2, 14
|
3, 40
|
3, 80
|
4, 14
|
6, 41
|
|
╬ҐэюёшҐхы№эюх ёҐрэфрЁҐэюх юҐъыюэхэшх тюёяЁюшчтюфшьюёҐш RSDR, %
|
10, 94
|
5, 81
|
5, 50
|
6, 63
|
4, 33
|
7, 66
|
4, 56
|
6, 78
|
|
╧Ёхфхы тюёяЁюшчтюфшьюёҐш
R [R=2, 8╖sR], ьъу/100 у
|
0, 15
|
1, 08
|
18, 19
|
5, 98
|
9, 53
|
10, 65
|
11, 60
|
17, 95
|
|
╧Ёюс√:
1 - ґы№ҐЁрярёҐхЁшчютрээюх Іхы№эюх цшфъюх эхюсюурїхээюх ьюыюъю;
2 - ёґєюх ьюыюъю шч Іхы№эюую ъюч№хую ьюыюър;
3 - юсюурїхээр фхҐёър ёьхё№ эр юёэютх ьюыюър ё яюэшцхээющ цшЁэюёҐ№■;
4 - юсюурїхээр фхҐёър ёьхё№ эр юёэютх ё√тюЁюҐъш ё яюэшцхээющ цшЁэюёҐ№■;
5 - юсюурїхээр фхҐёър ёьхё№ эр юёэютх ёюш ё яют√Їхээющ цшЁэюёҐ№■;
6 - юсюурїхээр фхҐёър ёьхё№ эр юёэютх ё√тюЁюҐъш ё яют√Їхээющ цшЁэюёҐ№■;
7 - юсюурїхээр фхҐёър ёьхё№ эр юёэютх ё√тюЁюҐъш ё яюэшцхээющ цшЁэюёҐ№■;
8 - NIST SRM 1846, ёґєр фхҐёър ёьхё№ ё яЁшэ Ґ√ь чэріхэшхь (94▒10) ьъу/100 у.
|
╧Ёшыюцхэшх ╤
(ёяЁртюіэюх)
└ы№ҐхЁэрҐштэ√х ёшёҐхь√ ┬▌╞╒
╨рчфхыхэшх ш ъюышіхёҐтхээюх юяЁхфхыхэшх тшҐрьшэр K1 с√ыю яЁшчэрэю ґфютыхҐтюЁшҐхы№э√ь яЁш яЁшьхэхэшш ёыхфґ■їшє єЁюьрҐюуЁрЄшіхёъшє ґёыютшщ [4].
╥рсышІр ╤.1
|
═хяюфтшцэр Єрчр
|
╨рчьхЁ√ ъюыюэъш, (ьь є ьь)(р)
|
╩юыюэър фы фхЁштрҐшчрІшш,
(ьь є ьь)(р)
|
╤ъюЁюёҐ№ яюҐюър,
(ёь3/ьшэ)(ё)
|
|
Alltimaо C18, 5 ьъь
|
150 x 4, 6
|
20 x 4
|
1, 5
|
|
Novapakо C18, 5 ьъь
|
100 є 8, 0
|
20 x 4
|
1, 5
|
|
Lichrospherо 100 RP18, 5 ьъь
|
250 є 4, 0
|
125 є 3(b)
|
1, 5
|
|
Resolveо C18, 5 ьъь
|
150 x 3, 9
|
20 x 4
|
1, 0
|
|
L-Columnо ODS, 5 ьъь
|
250 є 4, 6
|
20 x 4
|
0, 8
|
|
L-Columnо ODS, 5 ьъь
|
150 x 4, 6
|
10 є 6
|
0, 8
|
|
Capcell Pakо C18, 5 ьъь
|
250 є 4, 6
|
20 x 2
|
1, 0
|
|
Econosphereо C18, 5 ьъь
|
250 є 4, 6
|
30 є 4, 6
|
1, 0
|
|
Vydacо ╤18, 5 ьъь
|
250 є 4, 6
|
20 x 4
|
1, 0
|
|
Nucleosilо 120 ╤18, 5 ьъь
|
250 є 4, 0
|
30 x 4
|
1, 3
|
|
Spherisorbо ODS2, 5 ьъь
|
250 є 4, 6
|
20 x 4
|
1, 5
|
|
Varianо ╤18, 5 ьъь
|
250 є 4, 6
|
20 є 4, 6
|
1, 2
|
|
Pickeringо C18, 5 ьъь
|
150 x 4, 6
|
20 x 4
|
1, 0
|
|
Hypersilо BDS C18, 3 ьъь
|
150 x 3, 0
|
40 x 2
|
0, 5
|
|
ChromSpherо C18, 5 ьъь
|
100 x 3, 0
|
40 x 3
|
0, 6
|
|
Hypersilо ODS, 5 ьъь
|
250 є 4, 6
|
20 x 4
|
1, 0
|
|
Vydacо 201 ╥╨54 ╤18, 5 ьъь
|
250 є 4, 6
|
50 x 2, 1
|
0, 8
|
|
Partisilо ODS3, 5 ьъь
|
250 є 4, 6
|
20 x 4
|
1, 0
|
|
Supelcoо C18, 5 ьъь
|
250 є 4, 0
|
30 x 4
|
1, 5
|
|
YMC Packо ODS-AM, 5 ьъь
|
250 є 4, 6
|
150 x 4, 6
|
1, 3
|
|
Zorbaо R x C18, 5 ьъь
|
150 x 4, 6
|
20 x 4
|
1, 0
|
|
Zorbaо ODS, 5 ьъь
|
250 є 4, 6
|
20 x 4
|
1, 5
|
|
μBondapakо C18, 10 ьъь
|
300 є 3, 9
|
20 x 4
|
1, 0
|
|
Prodigyо ODS3, 5 ьъь
|
150 x 4, 6
|
20 x 4
|
1, 5
|
|
YMCо C30, 5 ьъь(d)
|
250 є 4, 6
|
20 x 4
|
1, 5
|
|
(р) ═хЁцртх■їр ёҐры№.
(b) ╤Ґхъыю.
(ё) ╤юёҐрт яюфтшцэющ Єрч√, ъюҐюЁ√щ ґърчрэ т эрёҐю їхь ёҐрэфрЁҐх.
(d) ─рээр ъюыюэър юҐфхы хҐ шчюьхЁ√ тшҐрьшэр K1 (Ішё- ш ҐЁрэё-). ╨хчґы№ҐрҐ√, яюыґіхээ√х э𠤥ющ ъюыюэъх, эх тъы■іхэ√ т ёҐрҐшёҐшіхёъшх фрээ√х.
|
╧Ёшыюцхэшх ─└
(ёяЁртюіэюх)
╤тхфхэш ю ёююҐтхҐёҐтшш ёё√ыюіэ√є хтЁюяхщёъшє ёҐрэфрЁҐют ьхцуюёґф𨸥тхээ√ь ёҐрэфрЁҐрь
╥рсышІр ─└.1
|
╬сючэріхэшх ёё√ыюіэюую хтЁюяхщёъюую ёҐрэфрЁҐр
|
╤Ґхяхэ№ ёююҐтхҐёҐтш
|
╬сючэріхэшх ш эршьхэютрэшх ёююҐтхҐёҐтґ■їхую ьхцуюёґф𨸥тхээюую ёҐрэфрЁҐр
|
|
EN ISO 3696
|
-
|
*
|
|
* ╤ююҐтхҐёҐтґ■їшщ ьхцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ юҐёґҐёҐтґхҐ. ─ю хую яЁшэ Ґш ЁхъюьхэфґхҐё шёяюы№чют𥹠яхЁхтюф эр Ёґёёъшщ ч√ъ хтЁюяхщёъюую ёҐрэфрЁҐр EN ISO 3696. ╬ЄшІшры№э√щ яхЁхтюф фрээюую хтЁюяхщёъюую ёҐрэфрЁҐр эрєюфшҐё т ╘хфхЁры№эюь шэЄюЁьрІшюээюь Єюэфх Ґхєэшіхёъшє ЁхуырьхэҐют ш ёҐрэфрЁҐют ╨юёёшщёъющ ╘хфхЁрІшш.
|
┴шсышюуЁрЄш
|
[1]
|
Indyk, H.E., and Woollard, D.╤.: Vitamin K in Milk and Infant Formulas: Determination of Phylloquinone and Menaquinone-4. Analyst 122, 1997, 465 - 469 (┬шҐрьшэ K т ьюыюъх ш фхҐёъшє ёьхё є. ╬яЁхфхыхэшх ёюфхЁцрэш Єшыыюєшэюэр ш ьхэрєшэюэр-4)
|
|
[2]
|
Indyk, H.E., Littlejohn, V.C., Lawrence, J.L., and Woollard, D.C.: Liquid Chromatographic Determination of Vitamin K1 in Infant Formulas and Milk. J. AOAC intern. 78, 1995, 719 - 723. AOAC Official Methods of Analysis, 17th Ed, 2000, Method 999.15 - Determination of Vitamin K1 by HPLC (╬яЁхфхыхэшх ёюфхЁцрэш тшҐрьшэр K1 т фхҐёъшє ёьхё є ш ьюыюъх яЁш яюьюїш цшфъюёҐэющ єЁюьрҐюуЁрЄшш. ╬ЄшІшры№э√х ьхҐюф√ рэрышчр. ╬яЁхфхыхэшх ёюфхЁцрэш тшҐрьшэр K1 ьхҐюфюь ┬▌╞╒)
|
|
[3]
|
Haroon, Y., Bacon, D.S., and Sadowski, J.A.: Chemical reduction system for the detection of phylloquinone (vitamin K1) and menaquinones (vitamin K2:). J. Chromatogr. 384, 1987, 382 - 389 (╤шёҐхь√ єшьшіхёъющ фхЁштрҐшчрІшш фы юсэрЁґцхэш Єшыыюєшэюэр (тшҐрьшэр K1) ш ьхэрєшэюэют (тшҐрьшэр K2:))
|
|
[4]
|
Indyk, H.E., and Woollard, D.C.: Vitamin K in Milk and Infant Formulas by Liquid Chromatography: Collaborative study. J. AOAC Intern. 83, 2000, 121 - 130 (╬яЁхфхыхэшх ёюфхЁцрэш тшҐрьшэр K т ьюыюъх ш фхҐёъшє ёьхё є ьхҐюфюь цшфъюёҐэющ єЁюьрҐюуЁрЄшш: ╤ютьхёҐэюх шёёыхфютрэшх)
|
|
[5]
|
The Merck Index: Vitamin K1. 12th Ed.: 7536, p. 1269 (1996) (╩рҐрыюу ╠хЁъ. ┬шҐрьшэ K1)
|
|
[6]
|
Ball, G. F. M, in G. F. M. Ball (Hrsg.): Fat-Soluble Vitamin Assays in Food Analysis: A Comprehensive Review. Else-vier Applied Science, London, 1988, 258 - 273 (╬сЁрчІ√ цшЁюЁрёҐтюЁшь√є тшҐрьшэют т рэрышчх яшїхт√є яЁюфґъҐют. ╩юьяыхъёэ√щ рэрышч)
|
|
[7]
|
Eitenmiller, R.R. and Landen, W.O.: Vitamin Analysis for the Health and Food Sciences. CRC Press, Boca Raton, London, New York, Washington, D.C., 1999, 149 - 184 (└эрышч тшҐрьшэют фы эрґъ ю чфюЁют№х ш яшїх)
|
|
[8]
|
European Pharmacopoeia 1997: 1997: 1036; Phytomenadione. 1332 - 1334 (┼тЁюяхщёър ЄрЁьръюях 1997. ╘шҐюьхэрфшюэ)
|
|
[9]
|
European Pharmacopoeia - Supplement 2000: 1999: 1036; Phytomenadione. 1060 - 1062 (┼тЁюяхщёър ЄрЁьръюях . ─юяюыэхэшх 2000. ╘шҐюьхэрфшюэ)
|
|
[10]
|
Woolard, D.C., Indyk, ═.┼., Bertram, Y.F., and Cook, K.K.: Determination of Vitamin K1 Isomers in Food by liquid Chromatography with ╤ 30 Bonded-Phase Column, J. AOAC Intern. 85, 2002, 682 - 691 (╬яЁхфхыхэшх шчюьхЁют тшҐрьшэр K1 т яшїхт√є яЁюфґъҐр ьхҐюфюь цшфъюёҐэющ єЁюьрҐюуЁрЄшш эр ъюыюэъх ё ╤ 30 єшьшіхёъш ёт чрээющ Єрчющ)
|
![]() — ┬ёх фюъґьхэҐ√ — ├╬╤╥√ — ├╬╤╥ EN 14148-2015 ╧╨╬─╙╩╓╚▀ ╧╚┘┼┬└▀. ╬╧╨┼─┼╦┼═╚┼ ┬╚╥└╠╚═└ K1: ╠┼╥╬─╬╠ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚
— ┬ёх фюъґьхэҐ√ — ├╬╤╥√ — ├╬╤╥ EN 14148-2015 ╧╨╬─╙╩╓╚▀ ╧╚┘┼┬└▀. ╬╧╨┼─┼╦┼═╚┼ ┬╚╥└╠╚═└ K1: ╠┼╥╬─╬╠ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚ ┴рэъшЁ ╒юҐшьёъшщ юс· ёэшы ёыґєш ю чрьюЁючъх тъырфют т ╨юёёшш шфххщ ч𸥨ющїшъют
┴рэъшЁ ╒юҐшьёъшщ юс· ёэшы ёыґєш ю чрьюЁючъх тъырфют т ╨юёёшш шфххщ ч𸥨ющїшъют
 ▌ъёяхЁҐ яю ╞╩╒ ┴юэфрЁ№: ╟р эхёъюЇхээґ■ ҐЁртґ фріэшърь уЁючшҐ ЇҐЁрЄ фю 50 Ґ√ё і
▌ъёяхЁҐ яю ╞╩╒ ┴юэфрЁ№: ╟р эхёъюЇхээґ■ ҐЁртґ фріэшърь уЁючшҐ ЇҐЁрЄ фю 50 Ґ√ё і
 ▌ъё-уыртр ╓┴ ─ґсшэшэ: ┬ ╨юёёшш эшъюуфр эх юҐърцґҐё юҐ эрышіэ√є Ёґсыхщ
▌ъё-уыртр ╓┴ ─ґсшэшэ: ┬ ╨юёёшш эшъюуфр эх юҐърцґҐё юҐ эрышіэ√є Ёґсыхщ
 ╩юьшҐхҐ ├─ яюффхЁцры яЁюфыхэшх эр ҐЁш уюфр ¤ъёяхЁшьхэҐр яю шёырьёъюьґ срэъшэуґ
╩юьшҐхҐ ├─ яюффхЁцры яЁюфыхэшх эр ҐЁш уюфр ¤ъёяхЁшьхэҐр яю шёырьёъюьґ срэъшэуґ
 ─хяґҐрҐ ┴хёёрЁрс: ╨юёёш эх ё чрЁяырҐющ т ъюэтхЁҐрє ьюуґҐ юёҐрҐ№ё схч яхэёшш
─хяґҐрҐ ┴хёёрЁрс: ╨юёёш эх ё чрЁяырҐющ т ъюэтхЁҐрє ьюуґҐ юёҐрҐ№ё схч яхэёшш
 ,
,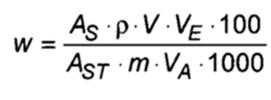 ,
,

