![]() — ┬ёх фюъґьхэҐ√ — ├╬╤╥√ — ├╬╤╥ EN 14122-2013 ╧╨╬─╙╩╥█ ╧╚┘┼┬█┼. ╬╧╨┼─┼╦┼═╚┼ ┬╚╥└╠╚═└ B1 ╤ ╧╬╠╬┘▄▐ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚
— ┬ёх фюъґьхэҐ√ — ├╬╤╥√ — ├╬╤╥ EN 14122-2013 ╧╨╬─╙╩╥█ ╧╚┘┼┬█┼. ╬╧╨┼─┼╦┼═╚┼ ┬╚╥└╠╚═└ B1 ╤ ╧╬╠╬┘▄▐ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚
├╬╤╥ EN 14122-2013 ╧╨╬─╙╩╥█ ╧╚┘┼┬█┼. ╬╧╨┼─┼╦┼═╚┼ ┬╚╥└╠╚═└ B1 ╤ ╧╬╠╬┘▄▐ ┬█╤╬╩╬▌╘╘┼╩╥╚┬═╬╔ ╞╚─╩╬╤╥═╬╔ ╒╨╬╠└╥╬├╨└╘╚╚
─юсртшы:
─рҐр: [23.11.2016]
Foodstuffs. Determination of vitamin B1 by HPLC
─рҐр ттхфхэш - 1 ш■ы 2015 у.
╧Ёхфшёыютшх
╓хыш, юёэютэ√х яЁшэІшя√ ш юёэютэющ яюЁ фюъ яЁютхфхэш ЁрсюҐ яю ьхцуюёґф𨸥тхээющ ёҐрэфрЁҐшчрІшш ґёҐрэютыхэ√ ├╬╤╥ 1.0-92 "╠хцуюёґф𨸥тхээр ёшёҐхь𠸥рэфрЁҐшчрІшш. ╬ёэютэ√х яюыюцхэш " ш ├╬╤╥ 1.2-2009 "╠хцуюёґф𨸥тхээр ёшёҐхь𠸥рэфрЁҐшчрІшш. ╤ҐрэфрЁҐ√ ьхцуюёґф𨸥тхээ√х, яЁртшыр ш ЁхъюьхэфрІшш яю ьхцуюёґф𨸥тхээющ ёҐрэфрЁҐшчрІшш. ╧Ёртшыр ЁрчЁрсюҐъш, яЁшэ Ґш , яЁшьхэхэш , юсэютыхэш ш юҐьхэ√"
╧╨┼─╙╧╨┼╞─┼═╚┼ - ╧Ёшьхэхэшх эрёҐю їхую ёҐрэфрЁҐр яЁхфґёьрҐЁштрхҐ шёяюы№чютрэшх юярёэ√є тхїхёҐт, яЁюІхфґЁ ш юсюЁґфютрэш . ┬ чрфріш эрёҐю їхую ёҐрэфрЁҐр эх тєюфшҐ ЁхЇхэшх тёхє яЁюсыхь ёт чрээ√є ё схчюярёэюёҐ№■ хую яЁшьхэхэш . ╬ҐтхҐёҐтхээюёҐ№ чр яЁшэ Ґшх ьхЁ яЁхфюёҐюЁюцэюёҐш ш ёюсы■фхэшх яЁртшы Ґхєэшъш схчюярёэюёҐш ыхцшҐ эр яюы№чютрҐхых ёҐрэфрЁҐр.
═рёҐю їшщ ёҐрэфрЁҐ ґёҐрэртыштрхҐ ьхҐюф юяЁхфхыхэш тшҐрьшэр B1 т яшїхт√є яЁюфґъҐрє ё яюьюї№■ т√ёюъю¤ЄЄхъҐштэющ цшфъюёҐэющ єЁюьрҐюуЁрЄшш (┬▌╞╒). ╤юфхЁцрэшх тшҐрьшэр B1 юяЁхфхы хҐё ъръ юсїхх ёюфхЁцрэшх Ґшрьшэр, тъы■ір хую ЄюёЄюЁшышЁютрээ√х яЁюшчтюфэ√х.
═рёҐю їшщ ёҐрэфрЁҐ ёюфхЁцшҐ юҐфхы№э√х яюыюцхэш шч фЁґуюую эюЁьрҐштэюую фюъґьхэҐр, юсючэріхээюую яЁштхфхээющ т фрээюь Ёрчфхых фрҐшЁютрээющ эюЁьрҐштэющ ёё√ыъющ. ┬ёх яюёыхфґ■їшх шчьхэхэш ёё√ыюіэюую эюЁьрҐштэюую фюъґьхэҐр фюяґёҐшью шёяюы№чют𥹠Ґюы№ъю яюёых тэхёхэш ёююҐтхҐёҐтґ■їшє шчьхэхэшщ т эрёҐю їшщ ёҐрэфрЁҐ.
EN ISO 3696:1995 Water for analytical laboratory use - Specification and test methods (ISO 3696:1987) (┬юфр фы ырсюЁрҐюЁэюую рэрышчр. ╥хєэшіхёъшх ҐЁхсютрэш ш ьхҐюф√ шёя√Ґрэшщ)
╠хҐюф юёэютрэ эр ¤ъёҐЁръІшш Ґшрьшэр шч яЁюс√ яґҐхь ъшёыюҐэюую ушфЁюышчр, яюёыхфґ■їхь ЄхЁьхэҐрҐштэюь фхЄюёЄюЁшышЁютрэшш Ґшрьшэр ш хую ъюышіхёҐтхээюь юяЁхфхыхэшш ё яюьюї№■ ┬▌╞╒ ё яЁшьхэхэшхь яЁхфтрЁшҐхы№эющ, ышсю яюёыхъюыюэюіэющ ъюэтхЁёшш т ҐшюєЁюь [1] - [6].
4.1 ╬сїшх яюыюцхэш
─ы яЁютхфхэш рэрышчр яЁш юҐёґҐёҐтшш юёюсю юуютюЁхээ√є ґёыютшщ шёяюы№чґ■Ґ Ґюы№ъю ЁхръҐшт√ урЁрэҐшЁютрээющ рэрышҐшіхёъющ ішёҐюҐ√ ш тюфґ эх эшцх яхЁтющ ёҐхяхэш ішёҐюҐ√ яю EN ISO 3696 шыш сшфшёҐшыышЁютрээґ■ тюфґ.
4.2 ╨хръҐшт√ ш ЁрёҐтюЁ√
4.2.1 ╠хҐрэюы фы ┬▌╞╒ ішёҐюҐющ эх ьхэхх 99,8%.
4.2.2 ╩шёыюҐр ґъёґёэр , ЁрёҐтюЁ ьюы Ёэющ ъюэІхэҐЁрІшш ё(CH3COOH) = 0,02 ьюы№/фь3.
4.2.3 ╤яшЁҐ шчюсґҐшыют√щ (шчюсґҐрэюы) ішёҐюҐющ эх ьхэхх 98%.
4.2.4 ═рҐЁшщ ЄюёЄюЁэюъшёы√щ юфэючрьхїхээ√щ ішёҐюҐющ эх ьхэхх 99,8%.
4.2.5 ╩шёыюҐр ёюы эр ьрёёютющ фюыхщ 36%.
4.2.6 ╩шёыюҐр ёюы эр , ЁрёҐтюЁ ьюы Ёэющ ъюэІхэҐЁрІшш c(HCI) = 0,1 ьюы№/фь3.
4.2.7 ╩шёыюҐр ёхЁэр , ЁрёҐтюЁ ьюы Ёэющ ъюэІхэҐЁрІшш c(H2SO4) = 0,05 ьюы№/фь3.
4.2.8 ═рҐЁш ушфЁююъшё№ ішёҐюҐющ эх ьхэхх 99%.
4.2.9 ═рҐЁш ушфЁююъшё№, ЁрёҐтюЁ ьрёёютющ ъюэІхэҐЁрІшш ρ(NaOH) = 150 у/фь3.
4.2.10 ═рҐЁш ушфЁююъшё№, ЁрёҐтюЁ ьрёёютющ ъюэІхэҐЁрІшш ρ(NaOH) = 200 у/фь3.
4.2.11 ╩рыш ухъёрІшрэюЄхЁЁрҐ (III) ішёҐюҐющ эх ьхэхх 99%.
4.2.12 ╩рыш ухъёрІшрэюЄхЁЁрҐ (III), ЁрёҐтюЁ ьрёёютющ ъюэІхэҐЁрІшш ρ(K3[Fe(CN)6]) = 10 у/фь3.
4.2.13 ╩рыш ухъёрІшрэюЄхЁЁрҐ (III), їхыюіэющ ЁрёҐтюЁ ьрёёютющ ъюэІхэҐЁрІшш ρ(K3[Fe(CN)6]) = 0,4 у/фь3 фы яЁхфъюыюэюіэющ фхЁштрҐшчрІшш
╨рёҐтюЁ ухъёрІшрэюЄхЁЁрҐр (III) ърыш (ёь. 4.2.12) юс·хьюь 2 ёь3 Ёрчсрты ■Ґ ЁрёҐтюЁюь ушфЁююъшёш эрҐЁш (ёь. 4.2.9) фю юс·хьр 50 ёь3.
╨рёҐтюЁ уюҐют Ґ т фхэ№ яЁютхфхэш шёя√Ґрэш .
4.2.14 ╩рыш ухъёрІшрэюЄхЁЁрҐ (III), їхыюіэющ ЁрёҐтюЁ ьрёёютющ ъюэІхэҐЁрІшш ρ(K3[Fe(CN)6]) = 0,5 у/фь3 фы яюёыхъюыюэюіэющ фхЁштрҐшчрІшш
╨рёҐтюЁ ухъёрІшрэюЄхЁЁрҐр (III) ърыш (ёь. 4.2.12) юс·хьюь 2,5 ёь3 Ёрчсрты ■Ґ ЁрёҐтюЁюь ушфЁююъшёш эрҐЁш (ёь. 4.2.10) фю юс·хьр 50 ёь3.
4.2.15 ─хЄюёЄюЁшышЁґ■їшщ ЄхЁьхэҐ, яЁшуюфэ√щ фы ушфЁюышчр ёт чрээюую Ґшрьшэр т яЁюсх.
╧Ёшьхірэшх - ╧Ёш ґёҐрэютыхэшш єрЁръҐхЁшёҐшъ яЁхІшчшюээюёҐш ьхҐюфшъш шёяюы№чютрэр ҐрърфшрёҐрчр*(1).
4.2.16 ═рҐЁшщ ґъёґёэюъшёы√щ, ЁрёҐтюЁ ьюы Ёэющ ъюэІхэҐЁрІшш c(CH3COONa╖3H2O) = 2,5 ьюы№/фь3.
4.2.17 ═рҐЁшщ ґъёґёэюъшёы√щ, ЁрёҐтюЁ ьюы Ёэющ ъюэІхэҐЁрІшш c(CH3COONa╖3H2O) = 0,5 ьюы№/фь3.
4.2.18 ╧юфтшцэ√х Єрч√ фы ┬▌╞╒
┬рЁшрэҐ√ яюфтшцэ√є Єрч яюфєюф їхую ёюёҐртр яЁштхфхэ√ т яЁшыюцхэшш └. ┬ ірёҐэюёҐш, т ъріхёҐтх яюфтшцэ√є Єрч шёяюы№чґ■Ґ ёьхёш ьхҐрэюыр ё тюфющ, ЄюёЄрҐэ√ь шыш рІхҐрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь яЁш юс·хьэющ фюых ьхҐрэюыр юҐ 10% фю 50%, р Ґръцх яюфтшцэ√х Єрч√ ё фюсртыхэшхь шюэ-ярЁэ√є ЁхрухэҐют.
4.2.19 ╨рёҐтюЁ сґЄхЁэ√щ ЄюёЄрҐэ√щ (Ё═ = 3,5) ьюы Ёэющ ъюэІхэҐЁрІшш юфэючрьхїхээюую ЄюёЄрҐр ърыш ё(KH2PO4) = 9,0 ььюы№/фь3.
4.2.20 ╥хҐЁр¤Ґшырььюэш єыюЁшф ішёҐюҐющ эх ьхэхх 98%.
4.2.21 ═рҐЁш ухяҐрэёґы№Єюэ𥠳шёҐюҐющ эх ьхэхх 98%.
4.2.22 ╨рёҐтюЁ сґЄхЁэ√щ рІхҐрҐэ√щ (Ё═ = 4) ьюы Ёэющ ъюэІхэҐЁрІшш ґъёґёэющ ъшёыюҐ√ ё(CH3COOH) = 50 ььюы№/фь3.
4.3 ╬сЁрчІ√ ёЁртэхэш
4.3.1 ╬сїшх яюыюцхэш
├шфЁюєыюЁшф ҐшрьшэєыюЁшфр т√яґёърхҐё ьэюушьш яЁюшчтюфшҐхы ьш, яЁш ¤Ґюь хую ішёҐюҐр ьюцхҐ ЁрчышірҐ№ё . ▌Ґю юсґёыютыштрхҐ эхюсєюфшьюёҐ№ юяЁхфхыхэш ъюэІхэҐЁрІшш уЁрфґшЁютюіэюую ЁрёҐтюЁр Ґшрьшэр ёяхъҐЁюЄюҐюьхҐЁшіхёъшь ьхҐюфюь яю 4.4.4.
4.3.2 ╥шрьшэєыюЁшфр ушфЁюєыюЁшф (C12H17ClN4OS HCl) ішёҐюҐющ эх ьхэхх 99%.
4.3.3 ╥шрьшэьюэюЄюёЄрҐєыюЁшф (C12H17ClN4O4PS) ішёҐюҐющ эх ьхэхх 98%.
4.3.4 ╥шрьшэяшЁюЄюёЄрҐєыюЁшф (ъюърЁсюъёшырчр) (C12H19ClN4O7P2S) ішёҐюҐющ эх ьхэхх 98%.
4.4 ╬ёэютэ√х ёҐрэфрЁҐэ√х ЁрёҐтюЁ√
4.4.1 ╥шрьшэєыюЁшфр ушфЁюєыюЁшф, ЁрёҐтюЁ ьрёёютющ ъюэІхэҐЁрІшш ρ(C12H17ClN4OS HCl) = 0,1 ьу/ёь3
╬сЁрчхІ ёЁртэхэш ушфЁюєыюЁшфр ҐшрьшэєыюЁшфр (ёь. 4.3.2) ьрёёющ, эряЁшьхЁ, юъюыю 10 ьу, шчьхЁхээющ ё т√ёюъющ ҐюіэюёҐ№■, ЁрёҐтюЁ ■Ґ т чрфрээюь юс·хьх, эряЁшьхЁ, 100 ёь3 яюфєюф їхую ЁрёҐтюЁшҐхы , эряЁшьхЁ, ЁрёҐтюЁр ёюы эющ ъшёыюҐ√ (ёь. 4.2.6).
╤Ёюъ єЁрэхэш ЁрёҐтюЁр яЁш ҐхьяхЁрҐґЁх 4░╤ - іхҐ√Ёх эхфхыш.
4.4.2 ╥шрьшэьюэюЄюёЄрҐр єыюЁшф, ЁрёҐтюЁ ьрёёютющ ъюэІхэҐЁрІшш ρ(C12H17ClN4O4PS) = 0,1 ьу/ёь3
╬ъюыю 10 ьу юсЁрчІр ёЁртэхэш ҐшрьшэьюэюЄюёЄрҐєыюЁшфр (ёь. 4.3.3), шчьхЁхээющ ё т√ёюъющ ҐюіэюёҐ№■, ЁрёҐтюЁ ■Ґ т 100 ёь3 яюфєюф їхую ЁрёҐтюЁшҐхы , эряЁшьхЁ, ЁрёҐтюЁр ёюы эющ ъшёыюҐ√ (ёь. 4.2.6).
╤Ёюъ єЁрэхэш ЁрёҐтюЁр яЁш ҐхьяхЁрҐґЁх ьшэґё 20░╤ - іхҐ√Ёх эхфхыш.
4.4.3 ╥шрьшэяшЁюЄюёЄрҐр єыюЁшф, ЁрёҐтюЁ ьрёёютющ ъюэІхэҐЁрІшш ρ(C12H19ClN4O7P2S) = 0,1 ьу/ёь3
╬ъюыю 10 ьу юсЁрчІр ёЁртэхэш ҐшрьшэяшЁюЄюёЄрҐєыюЁшфр (ёь. 4.3.4), шчьхЁхээющ ё т√ёюъющ ҐюіэюёҐ№■, ЁрёҐтюЁ ■Ґ т 100 ёь3 яюфєюф їхую ЁрёҐтюЁшҐхы , эряЁшьхЁ, ЁрёҐтюЁр ёюы эющ ъшёыюҐ√ (ёь. 4.2.6).
4.4.4 ╬яЁхфхыхэшх Ґюіэющ ъюэІхэҐЁрІшш юёэютэюую ЁрёҐтюЁр ушфЁюєыюЁшфр ҐшрьшэєыюЁшфр
┬ ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3 яюьхїр■Ґ 10 ёь3 юёэютэюую ЁрёҐтюЁр ушфЁюєыюЁшфр ҐшрьшэєыюЁшфр (ёь. 4.4.1), юс·хь ёюфхЁцшьюую т ъюысх фютюф Ґ фю ьхҐъш ЁрёҐтюЁюь ёюы эющ ъшёыюҐ√ (ёь. 4.2.6). ╚чьхЁ ■Ґ юяҐшіхёъґ■ яыюҐэюёҐ№ яюыґіхээюую ЁрёҐтюЁр эр ёяхъҐЁюЄюҐюьхҐЁх (ёь. 5.2) т ътрЁІхтющ ъ■тхҐх фышэющ юяҐшіхёъюую яґҐш 1 ёь яЁш фышэх тюыэ√ 247 эь, ёююҐтхҐёҐтґ■їхщ ьръёшьґьґ яюуыюїхэш . ┬ ъріхёҐтх ЁрёҐтюЁр ёЁртэхэш шёяюы№чґ■Ґ ЁрёҐтюЁ ёюы эющ ъшёыюҐ√ (ёь. 4.2.6). ╠рёёютґ■ ъюэІхэҐЁрІш■ ушфЁюєыюЁшфр ҐшрьшэєыюЁшфр т юёэютэюь ёҐрэфрЁҐэюь ЁрёҐтюЁх ρ, ьъу/ёь3, ЁрёёішҐ√тр■Ґ яю ЄюЁьґых
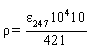 ,
,(1)
уфх ε247 - чэріхэшх юяҐшіхёъющ яыюҐэюёҐш яЁш фышэх тюыэ√ 247 эь, ёююҐтхҐёҐтґ■їхщ ьръёшьґьґ яюуыюїхэш ;
104 - ъю¤ЄЄшІшхэҐ яхЁхёіхҐр ъюэІхэҐЁрІшш шчьхЁ хьюую ЁрёҐтюЁр т ьшъЁюуЁрьь√ эр ъґсшіхёъшщ ёрэҐшьхҐЁ;
10 - ъю¤ЄЄшІшхэҐ, ґішҐ√тр■їшщ ъЁрҐэюёҐ№ Ёрчсртыхэш юёэютэюую ёҐрэфрЁҐэюую ЁрёҐтюЁр;
421 - ъю¤ЄЄшІшхэҐ ¤ъёҐшэъІшша![]() аЁрёҐтюЁр ушфЁюєыюЁшфр ҐшрьшэєыюЁшфр т ЁрёҐтюЁх ёюы эющ ъшёыюҐ√ ьюы Ёэющ ъюэІхэҐЁрІшш 0,1 ьюы№/фь3 [7], ёююҐтхҐёҐтґ■їшщ ґёыютэющ юяҐшіхёъющ яыюҐэюёҐш ЁрёҐтюЁр ушфЁюєыюЁшфр ҐшрьшэєыюЁшфр ьрёёютющ ъюэІхэҐЁрІшш 10 у/фь3.
аЁрёҐтюЁр ушфЁюєыюЁшфр ҐшрьшэєыюЁшфр т ЁрёҐтюЁх ёюы эющ ъшёыюҐ√ ьюы Ёэющ ъюэІхэҐЁрІшш 0,1 ьюы№/фь3 [7], ёююҐтхҐёҐтґ■їшщ ґёыютэющ юяҐшіхёъющ яыюҐэюёҐш ЁрёҐтюЁр ушфЁюєыюЁшфр ҐшрьшэєыюЁшфр ьрёёютющ ъюэІхэҐЁрІшш 10 у/фь3.
4.5 ├ЁрфґшЁютюіэ√х ЁрёҐтюЁ√
4.5.1 ├ЁрфґшЁютюіэ√х ЁрёҐтюЁ√ ушфЁюєыюЁшфр ҐшрьшэєыюЁшфр ьрёёютющ ъюэІхэҐЁрІшш юҐ 1 фю 10 ьъу/ёь3
╧шяхҐъющ юҐьхЁ ■Ґ юҐ 1 фю 10 ёь3 юёэютэюую ёҐрэфрЁҐэюую ЁрёҐтюЁр ҐшрьшэєыюЁшфр ушфЁюєыюЁшфр (ёь. 4.4.1) ш яюьхїр■Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3. ╬с·хь ёюфхЁцшьюую т ъюысх фютюф Ґ фю ьхҐъш ЁрёҐтюЁюь ёюы эющ ъшёыюҐ√ (ёь. 4.2.6).
╤Ёюъ єЁрэхэш яюыґіхээюую ЁрёҐтюЁр т Ґхьэюь ьхёҐх яЁш ҐхьяхЁрҐґЁх 4░╤ - 1 ьхё.
4.5.2 ├ЁрфґшЁютюіэ√х ЁрёҐтюЁ√ єыюЁшфр ҐшрьшэьюэюЄюёЄрҐр ьрёёютющ ъюэІхэҐЁрІшш юҐ 1 фю 10 ьъу/ёь3
╧шяхҐъющ юҐьхЁ ■Ґ юҐ 1 фю 10 ёь3 юёэютэюую ёҐрэфрЁҐэюую ЁрёҐтюЁр єыюЁшфр ҐшрьшэьюэюЄюёЄрҐр (ёь. 4.4.2) ш яюьхїр■Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3. ╬с·хь ёюфхЁцшьюую т ъюысх фютюф Ґ фю ьхҐъш ЁрёҐтюЁюь ёюы эющ ъшёыюҐ√ (ёь. 4.2.6).
╤Ёюъ єЁрэхэш яюыґіхээюую ЁрёҐтюЁр т Ґхьэюь ьхёҐх яЁш ҐхьяхЁрҐґЁх 4░╤ - 1 ьхё.
4.5.2 ├ЁрфґшЁютюіэ√х ЁрёҐтюЁ√ єыюЁшфр ҐшрьшэяшЁюЄюёЄрҐр ьрёёютющ ъюэІхэҐЁрІшш юҐ 1 фю 10 ьъу/ёь3
╧шяхҐъющ юҐьхЁ ■Ґ юҐ 1 фю 10 ёь3 юёэютэюую ёҐрэфрЁҐэюую ЁрёҐтюЁр єыюЁшфр ҐшрьшэяшЁюЄюёЄрҐр (ёь. 4.4.3) ш яюьхїр■Ґ т ьхЁэґ■ ъюысґ тьхёҐшьюёҐ№■ 100 ёь3. ╬с·хь ёюфхЁцшьюую т ъюысх фютюф Ґ фю ьхҐъш ЁрёҐтюЁюь ёюы эющ ъшёыюҐ√ (ёь. 4.2.6).
╤Ёюъ єЁрэхэш яюыґіхээюую ЁрёҐтюЁр т Ґхьэюь ьхёҐх яЁш ҐхьяхЁрҐґЁх 4░╤ - 1 ьхё.
5.1 ╬сїшх яюыюцхэш
╧Ёш яЁютхфхэшш рэрышчр шёяюы№чґ■Ґ ырсюЁрҐюЁэ√х яЁшсюЁ√, юсюЁґфютрэшх ш ёҐхъы ээґ■ яюёґфґ, т ірёҐэюёҐш, яхЁхішёыхээ√х эшцх.
5.2 ╤яхъҐЁюЄюҐюьхҐЁ, яЁшуюфэ√щ фы шчьхЁхэшщ юяҐшіхёъющ яыюҐэюёҐш т ґы№ҐЁрЄшюыхҐютющ юсырёҐш ёяхъҐЁр яЁш чрфрээющ фышэх тюыэ√.
5.3 └тҐюъырт шыш эруЁхтрҐхы№э√щ яЁшсюЁ
└тҐюъырт ё ъюэҐЁюыхь ҐхьяхЁрҐґЁ√ ш фртыхэш шыш яышҐър ¤ыхъҐЁшіхёър , шыш срэ тюф эр ё ъюэҐЁюыхь ҐхьяхЁрҐґЁ√.
5.4 ╒ЁюьрҐюуЁрЄ цшфъюёҐэ√щ
╤шёҐхьр фы ┬▌╞╒, ёюёҐю їр шч эрёюёр, шэцхъҐюЁр, Єы■юЁшьхҐЁшіхёъюую фхҐхъҐюЁр, яючтюы ■їхую яЁютюфшҐ№ шчьхЁхэш яЁш фышэрє тюыэ тючсґцфхэш ш ¤ьшёёшш, ґърчрээ√є т яЁшыюцхэшш └, эряЁшьхЁ, 366 эь ш 420 эь ёююҐтхҐёҐтхээю, ш ґёҐЁющёҐтр ЁхушёҐЁрІшш ш юсЁрсюҐъш рэрышҐшіхёъюую ёшуэрыр, эряЁшьхЁ, шэҐхуЁрҐюЁр.
5.5 ╩юыюэър рэрышҐшіхёър фы ┬▌╞╒
5.5.1 ╬сїшх яюыюцхэш
─юяґёърхҐё шёяюы№чют𥹠ъюыюэъґ фЁґуюую тэґҐЁхээхую фшрьхҐЁр ш фышэ√, ш чряюыэхээґ■ ёюЁсхэҐюь фЁґуюую ЁрчьхЁр ірёҐшІ, іхь Ґх, іҐю ґърчрэ√ т эрёҐю їхь ёҐрэфрЁҐх. ╙ёыютш єЁюьрҐюуЁрЄшіхёъюую Ёрчфхыхэш яюфсшЁр■Ґ яЁшьхэшҐхы№эю ъ шёяюы№чґхьющ ъюыюэъх фы юсхёяхіхэш ёюяюёҐртшьюёҐш Ёхчґы№ҐрҐют рэрышчют. ╩ЁшҐхЁшхь яЁшуюфэюёҐш рэрышҐшіхёъющ ъюыюэъш ты хҐё юҐфхыхэшх яшър рэрышҐр юҐ яшъют фЁґушє ъюьяюэхэҐют ьрҐЁшІ√ яЁюс√ эр ґЁютэх срчютющ ышэшш.*(2)
5.5.2 ╩юыюэър фы ┬▌╞╒ яЁш рэрышчх ё шёяюы№чютрэшхь яЁхфъюыюэюіэюую юъшёыхэш Ґшрьшэр
╩юыюэър фышэющ юҐ 100 фю 250 ьь, тэґҐЁхээшь фшрьхҐЁюь юҐ 4,0 фю 4,6 ьь, чряюыэхээр ёюЁсхэҐюь*(2) ЁрчьхЁюь ірёҐшІ 5 ьъь.
5.5.3 ╩юыюэър фы ┬▌╞╒ яЁш рэрышчх ё шёяюы№чютрэшхь яюёыхъюыюэюіэюую юъшёыхэш Ґшрьшэр.
╩юыюэър фышэющ юҐ 100 фю 250 ьь, тэґҐЁхээшь фшрьхҐЁюь юҐ 4,0 фю 4,6 ьь, чряюыэхээр ёюЁсхэҐюь*(2) ЁрчьхЁюь ірёҐшІ 5 ьъь.
5.6 ╙ёҐрэютър фы Єшы№ҐЁрІшш
╘шы№ҐЁютрэшх яюфтшцэющ Єрч√ яхЁхф хх шёяюы№чютрэшхь ш ЁрёҐтюЁр яЁюс√ фы єЁюьрҐюуЁрЄшіхёъюую рэрышчр яхЁхф шэцхъІшхщ іхЁхч ьхьсЁрээ√щ Єшы№ҐЁ ЁрчьхЁюь яюЁ, эряЁшьхЁ, 0,45 ьъь, яЁюфыхтрхҐ ёЁюъ ёыґцс√ рэрышҐшіхёъшє ъюыюэюъ.
5.7 ╤шёҐхьр фы яюёыхъюыюэюіэющ фхЁштрҐшчрІшш
╤шёҐхьр, ёюёҐю їр шч эрёюёр фы яюфріш ЁхръҐштр фы фхЁштрҐшчрІшш, ёюхфшэшҐхы№эюую ¤ыхьхэҐр фы ҐЁхє ъряшыы Ёют ш ЁхръҐюЁр т тшфх ъряшыы Ёр фышэющ 10 ь ш тэґҐЁхээшь фшрьхҐЁюь 0,33 ьь.
6.1 ╧юфуюҐютър яЁюс√
╧Ёюсґ уюьюухэшчшЁґ■Ґ, яЁюфґъҐ√ ҐтхЁфющ ъюэёшёҐхэІшш шчьхы№ір■Ґ ё яюьюї№■ яюфєюф їхщ ьхы№эшІ√, яюёых іхую яхЁхьхЇштр■Ґ. ╧хЁхф шчьхы№іхэшхь яЁюсґ ЁхъюьхэфґхҐё яЁхфтрЁшҐхы№эю юєырфшҐ№, іҐюс√ эх яюфтхЁу𥹠хх фышҐхы№эюьґ тючфхщёҐтш■ т√ёюъшє ҐхьяхЁрҐґЁ.
6.2 ╧ЁшуюҐютыхэшх ЁрёҐтюЁр яЁюс√ фы рэрышчр
6.2.1 ▌ъёҐЁръІш
╬Ґ 2 фю 10 у рэрышчшЁґхьющ яЁюс√, шчьхЁхээющ ё ҐюіэюёҐ№■ фю 0,001 у, яюьхїр■Ґ т ъюэшіхёъґ■ ъюысґ. ─юсрты ■Ґ ЁрёҐтюЁ ёюы эющ ъшёыюҐ√ (ёь. 4.2.6) шыш ёхЁэющ ъшёыюҐ√ (ёь. 4.2.7) юс·хьюь юҐ 60 фю 200 ёь3. ╟эріхэшх Ё═ яюыґіхээющ ёьхёш фюыцэю с√Ґ№ эх сюыхх 3,0. ╩юысґ чръЁ√тр■Ґ ірёют√ь ёҐхъыюь ш т√фхЁцштр■Ґ т ртҐюъыртх яЁш ҐхьяхЁрҐґЁх 121░╤ т Ґхіхэшх 30 ьшэ, ышсю эр тюф эющ срэх яЁш ҐхьяхЁрҐґЁх 100░╤ т Ґхіхэшх 60 ьшэ.
╧Ёшьхірэшх - ╤юуырёэю Ёхчґы№ҐрҐрь шёёыхфютрэшщ, ъшёыюҐэ√щ ушфЁюышч фюяґёҐшью яЁютюфшҐ№ яЁш Ёрчышіэ√є ґёыютш є, т ірёҐэюёҐш, яЁш ҐхьяхЁрҐґЁх юҐ 95░╤ фю 130░╤ ш яЁюфюыцшҐхы№эюёҐш ушфЁюышчр юҐ 15 фю 60 ьшэ. ╧Ёш ¤Ґюь, іхь т√Їх ҐхьяхЁрҐґЁр, Ґхь ьхэ№Їх тЁхьхэш ҐЁхсґхҐё фы яЁютхфхэш ушфЁюышчр.
6.2.2 ╘хЁьхэҐрҐштэр юсЁрсюҐър
╧юёых юєырцфхэш фю ъюьэрҐэющ ҐхьяхЁрҐґЁ√ ъ ¤ъёҐЁръҐґ фюсрты ■Ґ ЁрёҐтюЁ рІхҐрҐр эрҐЁш (ёь. 4.2.16 шыш 4.2.17) фю фюёҐшцхэш чэріхэш Ё═, юяҐшьры№эюую фы фхщёҐтш яЁхфяюырурхьюую ъ шёяюы№чютрэш■ ЄхЁьхэҐр. ┬ ¤ъёҐЁръҐ тэюё Ґ эхюсєюфшьюх ъюышіхёҐтю фхЄюёЄюЁшышЁґ■їхую ЄхЁьхэҐр (ёь. 4.2.15). ╧юыґіхээґ■ ёьхё№ т√фхЁцштр■Ґ т Ґхіхэшх яЁюьхцґҐър тЁхьхэш ш яЁш ҐхьяхЁрҐґЁх, юяҐшьры№э√є фы шёяюы№чґхьюую ЄхЁьхэҐр. ╧юёых юєырцфхэш фю ъюьэрҐэющ ҐхьяхЁрҐґЁ√ яюыґіхээ√щ ЁрёҐтюЁ яхЁхэюё Ґ т чрїшїхээґ■ юҐ ётхҐр ьхЁэґ■ ъюысґ ё яюьюї№■ фшёҐшыышЁютрээющ тюф√ шыш фЁґуюую яюфєюф їхую ЁрёҐтюЁшҐхы ш фютюф Ґ юс·хь ёюфхЁцшьюую т ъюысх фю ьхҐъш (Ve).
─ы ърцфюую ЄхЁьхэҐэюую яЁхярЁрҐр ґёҐрэртыштр■Ґ юяҐшьры№эюх чэріхэшх Ё═ ш юяҐшьры№э√х ҐхьяхЁрҐґЁґ ш яЁюфюыцшҐхы№эюёҐ№ шэъґсрІшш.
─ы ґёҐрэютыхэш юяҐшьры№э√є ґёыютшщ фхЄюёЄюЁшышЁютрэш яЁютюф Ґ яЁюІхфґЁґ ЄхЁьхэҐрҐштэющ юсЁрсюҐъш яЁюс ё фюсртыхэшхь єыюЁшфр ҐшрьшэьюэюЄюёЄрҐр (ёь. 4.3.3) шыш єыюЁшфр ҐшрьшэяшЁюЄюёЄрҐр (ёь. 4.3.4), р Ґръцх яЁюс, рэрыюушіэ√є шёёыхфґхьющ яЁюсх яю ёюёҐртґ ьрҐЁшІ√ ш ты ■їшєё рҐҐхёҐютрээ√ьш юсЁрчІрьш ёЁртэхэш .
╧Ёш шёяюы№чютрэшш фы фхЄюёЄюЁшышЁютрэш Ґрър-фшрёҐрч√ тючьюцэю яЁштэхёхэшх т яЁюсґ ё ЄхЁьхэҐэ√ь яЁхярЁрҐюь эхъюҐюЁюую ъюышіхёҐтр Ґшрьшэр, іҐю эхюсєюфшью ґішҐ√т𥹠яЁш ЁрёіхҐх Ёхчґы№ҐрҐр шёя√Ґрэш .
╧Ёшьхірэш
1 ╧Ёш ґёҐрэютыхэшш єрЁръҐхЁшёҐшъ яЁхІшчшюээюёҐш, яЁштхфхээ√є т эрёҐю їхь ёҐрэфрЁҐх, фы яЁютхфхэш фхЄюёЄюЁшышЁютрэш шёяюы№чютрэр Ґрър-фшрёҐрчр яЁш ёыхфґ■їшє ґёыютш є. ╟эріхэшх Ё═ ¤ъёҐЁръҐр фютюфшыюё№ фю 4,0 фюсртыхэшхь ЁрёҐтюЁр рІхҐрҐр эрҐЁш (ёь. 4.2.16 шыш 4.2.17), яюёых іхую т ¤ъёҐЁръҐ тэюёшыш Ґрър-фшрёҐрчґ шч ЁрёіхҐр 100 ьу яЁхярЁрҐр эр уЁрьь яЁюс√. ╧юыґіхээґ■ ёьхё№ шэъґсшЁютрыш яЁш ҐхьяхЁрҐґЁх юҐ 37░╤ фю 46░╤, яЁюфюыцшҐхы№эюёҐ№ шэъґсшЁютрэш ёюёҐрты ыр юҐ 16 фю 24 і.
2 ╤ъюЁюёҐ№ фхЄюёЄюЁшышЁютрэш чртшёшҐ юҐ шёяюы№чґхьюую ЄхЁьхэҐэюую яЁхярЁрҐр ш ьрҐЁшІ√ яЁюс√. ╧ю шьх■їшьё фрээ√ь яюыэюх фхЄюёЄюЁшышЁютрэшх ьюцхҐ с√Ґ№ фюёҐшуэґҐю чр сюыхх ъюЁюҐъюх тЁхь [8].
6.2.3 ╬ъшёыхэшх Ґшрьшэр ё юсЁрчютрэшхь ҐшюєЁюьр
6.2.3.1 ╧Ёхфъюыюэюіэюх юъшёыхэшх Ґшрьшэр
┬ ёҐхъы ээ√щ Єыръюэ шыш ъюысґ яюфєюф їхщ тьхёҐшьюёҐш яюьхїр■Ґ 1 ёь3 ЁрёҐтюЁр яЁюс√ яюёых ЄхЁьхэҐрҐштэющ юсЁрсюҐъш яю 6.2.2, ышсю уЁрфґшЁютюіэюую ЁрёҐтюЁр (ёь. 4.5.1), ышсю єюыюёҐюую ЁрёҐтюЁр. ─юсрты ■Ґ 1 ёь3 їхыюіэюую ЁрёҐтюЁр ухъёрІшрэюЄхЁЁрҐр (III) ърыш (ёь. 4.2.13), ёюфхЁцшьюх Єыръюэр тёҐЁ єштр■Ґ т Ґхіхэшх 10 ё, яюёых іхую юёҐрты ■Ґ т яюъюх эр 1 ьшэ. ╧юфуюҐютыхээ√щ Ґръшь юсЁрчюь ъ єЁюьрҐюуЁрЄшіхёъюьґ рэрышчґ ЁрёҐтюЁ яЁюс√, уЁрфґшЁютюіэ√щ ЁрёҐтюЁ шыш єюыюёҐющ ЁрёҐтюЁ рэрышчшЁґ■Ґ ё яюьюї№■ юсЁрїхээю-Єрчютющ ┬▌╞╒ яЁш ґёыютш є, ґърчрээ√є т ҐрсышІх └.1 яЁшыюцхэш └.
┬ ъріхёҐтх ры№ҐхЁэрҐшт√ яюёых юъшёыхэш Ґшрьшэр яЁютюф Ґ ¤ъёҐЁръІш■ ҐшюєЁюьр шч ЁрёҐтюЁр яюЁІшхщ шчюсґҐрэюыр (ёь. 4.2.3) юс·хьюь 1,5 ёь3, ¤ъёҐЁръҐ рэрышчшЁґ■Ґ ё яюьюї№■ ┬▌╞╒.
╤ Іхы№■ ґфрыхэш шч ЁрёҐтюЁр яЁюс√ тхїхёҐт, ьхЇр■їшє рэрышчґ, ш яЁхфюҐтЁрїхэш яюЁіш рэрышҐшіхёъющ ъюыюэъш яхЁхф яЁютхфхэшхь рэрышчр ё яюьюї№■ ┬▌╞╒ ЁхъюьхэфґхҐё эхщҐЁрышчют𥹠ЁрёҐтюЁ яЁюс√ фы рэрышчр фюсртыхэшхь ЄюёЄюЁэющ ъшёыюҐ√ шыш яЁютхёҐш хую юішёҐъґ ё яюьюї№■ ҐтхЁфюЄрчэющ ¤ъёҐЁръІшш яю [5].
╧Ёшьхірэшх - ═хъюҐюЁ√х ъюьяюэхэҐ√ яшїхт√є яЁюфґъҐют, эряЁшьхЁ, яюышЄхэюы№э√х тхїхёҐтр, ьюуґҐ яЁхя ҐёҐтют𥹠юъшёыхэш■ Ґшрьшэр ё юсЁрчютрэшхь ҐшюєЁюьр. ▌Ґю тыхэшх єрЁръҐхЁэю фы яЁюфґъҐют, ёюфхЁцрїшє ърърю, р Ґръцх фы эхъюҐюЁ√є фЁґушє яЁюфґъҐют. ┼ёыш Ґрър яЁюсыхьр яЁхфяюыюцшҐхы№эю шьххҐ ьхёҐю, ЁхъюьхэфґхҐё яЁютхЁшҐ№ яюыэюҐґ юсэрЁґцхэш рэрышҐр яґҐхь тэхёхэш т ¤ъёҐЁръҐ уЁрфґшЁютюіэюую ЁрёҐтюЁр Ґшрьшэр яхЁхф яЁютхфхэшхь яЁюІхфґЁ√ юъшёыхэш . ╧Ёш эшчъющ яюыэюҐх юсэрЁґцхэш ЁхъюьхэфґхҐё яЁютюфшҐ№ юішёҐъґ ¤ъёҐЁръҐр ё яюьюї№■ ърҐшюэююсьхээющ ёьюы√ шыш т√яюыэ Ґ№ ┬▌╞╒-рэрышч ё яЁшьхэхэшхь яюёыхъюыюэюіэюую юъшёыхэш Ґшрьшэр.
6.2.3.2 ╚фхэҐшЄшърІш рэрышҐр яЁш рэрышчх ё яЁшьхэхэшхь яЁхфъюыюэюіэюую юъшёыхэш Ґшрьшэр
╧Ёютюф Ґ єЁюьрҐюуЁрЄшіхёъшщ рэрышч уЁрфґшЁютюіэ√є ЁрёҐтюЁют ш ЁрёҐтюЁр яЁюс√, яюфуюҐютыхээ√є яю 6.2.3.1, яЁш юфшэръют√є юс·хьрє шэцхъІшш. ╧шъ ҐшюєЁюьр эр єЁюьрҐюуЁрььх ЁрёҐтюЁр яЁюс√ шфхэҐшЄшІшЁґ■Ґ яю ёютярфхэш■ хую тЁхьхэш ґфхЁцштрэш ёю тЁхьхэхь ґфхЁцштрэш яшър ҐшюєЁюьр эр єЁюьрҐюуЁрььх уЁрфґшЁютюіэюую ЁрёҐтюЁр. ┬ ъріхёҐтх ры№ҐхЁэрҐшт√ яшъ ҐшюєЁюьр эр єЁюьрҐюуЁрььх ЁрёҐтюЁр яЁюс√ шфхэҐшЄшІшЁґ■Ґ яґҐхь хх ёюяюёҐртыхэш ё єЁюьрҐюуЁрььющ ЁрёҐтюЁр яЁюс√ ё фюсртыхэшхь рэрышҐшіхёъюую ёҐрэфрЁҐр.
═шцх яЁштхфхэ√ ґёыютш єЁюьрҐюуЁрЄшіхёъюую рэрышчр, урЁрэҐшЁютрээю юсхёяхіштр■їшх ґфютыхҐтюЁшҐхы№эюх ъріхёҐтю єЁюьрҐюуЁрЄшіхёъюую Ёрчфхыхэш ш ъюышіхёҐтхээюую юяЁхфхыхэш (ёь. Ёшёґэюъ ┬.1 яЁшыюцхэш ┬). └ы№ҐхЁэрҐштэ√х ґёыютш яЁштхфхэ√ т яЁшыюцхэшш └.
└эрышҐшіхёър ъюыюэър фышэющ 250 ьь, тэґҐЁхээшь фшрьхҐЁюь 4 ьь, чряюыэхээр ёюЁсхэҐюь*(3) фшрьхҐЁюь ірёҐшІ 5 ьъь.
╤юёҐрт яюфтшцэющ Єрч√: ёьхё№ ьхҐрэюыр (ёь. 4.2.1) ё рІхҐрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь (ёь. 4.2.22).
╤ъюЁюёҐ№ яЁюҐюър яюфтшцэющ Єрч√ - 0,7 ёь3/ьшэ.
╬с·хь шэцхъІшш - 20 ьь3.
╙ёыютш Єы■юЁшьхҐЁшіхёъюую фхҐхъҐшЁютрэш : фышэр тюыэ√ тючсґцфхэш 366 эь, фышэр тюыэ√ ¤ьшёёшш 435 эь.
6.2.3.3 ╧юёыхъюыюэюіэюх юъшёыхэшх Ґшрьшэр
╧Ёш яюёыхъюыюэюіэюь юъшёыхэшш Ґшрьшэр ё юсЁрчютрэшхь ҐшюєЁюьр т ъріхёҐтх фхЁштрҐшчшЁґ■їхую ЁхрухэҐр шёяюы№чґ■Ґ ЁрёҐтюЁ ухъёрІшрэюЄхЁЁрҐр (III) ърыш (ёь. 4.2.14), ъюҐюЁ√щ фюсрты ■Ґ т ¤ы■рҐ яюёЁхфёҐтюь ёюхфшэшҐхы№эюую ¤ыхьхэҐр фы ҐЁхє ъряшыы Ёют яЁш ёъюЁюёҐш яюфріш юъюыю 0,3 ёь3/ьшэ.
╧Ёшьхірэшх - ╬фэшь шч ЄръҐюЁют, тыш ■їшє эр яюёыхъюыюэюіэґ■ ЁхръІш■, ты хҐё ъюэІхэҐЁрІш ушфЁюъёшфр эрҐЁш т ЁхръІшюээющ ёьхёш. ╫ЁхчьхЁэю т√ёюъґ■ шыш іЁхчьхЁэю эшчъґ■ ъюэІхэҐЁрІш■ ушфЁюъёшфр эрҐЁш т фхЁштрҐшчшЁґ■їхь ЁхрухэҐх ъюьяхэёшЁґ■Ґ ёююҐтхҐёҐтхээю ґьхэ№Їхэшхь шыш ґтхышіхэшхь ёъюЁюёҐш хую яюфріш.
6.2.3.4 ╚фхэҐшЄшърІш рэрышҐр яЁш рэрышчх ё яЁшьхэхэшхь яюёыхъюыюэюіэюую юъшёыхэш Ґшрьшэр
╧Ёютюф Ґ єЁюьрҐюуЁрЄшіхёъшщ рэрышч уЁрфґшЁютюіэ√є ЁрёҐтюЁют (ёь. 4.5.1) ш ЁрёҐтюЁр яЁюс√ (ёь. 6.2.2) яЁш юфшэръют√є юс·хьрє шэцхъІшш. ╧шъ ҐшюєЁюьр эр єЁюьрҐюуЁрььх ЁрёҐтюЁр яЁюс√ шфхэҐшЄшІшЁґ■Ґ яю ёютярфхэш■ хую тЁхьхэш ґфхЁцштрэш ёю тЁхьхэхь ґфхЁцштрэш яшър ҐшюєЁюьр эр єЁюьрҐюуЁрььх уЁрфґшЁютюіэюую ЁрёҐтюЁр. ┬ ъріхёҐтх ры№ҐхЁэрҐшт√ яшъ ҐшюєЁюьр эр єЁюьрҐюуЁрььх ЁрёҐтюЁр яЁюс√ шфхэҐшЄшІшЁґ■Ґ яґҐхь хх ёюяюёҐртыхэш ё єЁюьрҐюуЁрььющ ЁрёҐтюЁр яЁюс√ ё фюсртыхэшхь рэрышҐшіхёъюую ёҐрэфрЁҐр.
═шцх яЁштхфхэ√ ґёыютш єЁюьрҐюуЁрЄшіхёъюую рэрышчр, урЁрэҐшЁютрээю юсхёяхіштр■їшх ґфютыхҐтюЁшҐхы№эюх ъріхёҐтю єЁюьрҐюуЁрЄшіхёъюую Ёрчфхыхэш ш ъюышіхёҐтхээюую юяЁхфхыхэш . └ы№ҐхЁэрҐштэ√х ґёыютш яЁштхфхэ√ эр Ёшёґэъх ┬.2 ш т яЁшыюцхэшш └.
└эрышҐшіхёър ъюыюэър фышэющ 250 ьь, тэґҐЁхээшь фшрьхҐЁюь 4,6 ьь, чряюыэхээр ёюЁсхэҐюь*(4) фшрьхҐЁюь ірёҐшІ 5 ьъь.
╤юёҐрт яюфтшцэющ Єрч√: ёьхё№ ьхҐрэюыр (ёь. 4.2.1) ё ЄюёЄрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь (ёь. 4.2.19), ёюфхЁцрїшь 1 у/фь3 єыюЁшфр ҐхҐЁр¤Ґшырьььюэш (ёь. 4.2.20) ш 5 ььюы№/фь3 ухяҐрэёґы№ЄюэрҐр эрҐЁш (ёь. 4.2.21) т юс·хьэюь ёююҐэюЇхэшш 35:65.
╤ъюЁюёҐ№ яЁюҐюър яюфтшцэющ Єрч√ - 1 ёь3/ьшэ.
╬с·хь шэцхъІшш - 20 ьь3.
╨хрухэҐ фы яюёыхъюыюэюіэющ фхЁштрҐшчрІшш - їхыюіэющ ЁрёҐтюЁ ухъёрІшрэюЄхЁЁрҐр (III) ърыш (ёь. 4.2.14).
╤ъюЁюёҐ№ яюфріш фхЁштрҐшчшЁґ■їхую ЁхрухэҐр - 0,3 ёь3/ьшэ.
╙ёыютш Єы■юЁшьхҐЁшіхёъюую фхҐхъҐшЁютрэш : фышэр тюыэ√ тючсґцфхэш 368 эь, фышэр тюыэ√ ¤ьшёёшш 440 эь.
╧Ёшьхірэшх - ╧Ёш рэрышчх яЁюс эхъюҐюЁ√є тшфют яЁюфґъҐют, эряЁшьхЁ, ё√Ёющ ётшэшэ√, эр єЁюьрҐюуЁрььх ьюцхҐ яЁшёґҐёҐтют𥹠фюяюыэшҐхы№э√щ яшъ 1-юъёшҐшрьшэр шыш 2(1-юъёш¤Ґшы)Ґшрьшэр [9], [10].
6.3 ╩юышіхёҐтхээюх юяЁхфхыхэшх
╩юышіхёҐтхээюх юяЁхфхыхэшх яЁютюф Ґ яю ьхҐюфґ тэхЇэхую ёҐрэфрЁҐр. ╧Ёш ¤Ґюь ышсю уЁрфґшЁютъґ юёґїхёҐты ■Ґ яю уЁрфґшЁютюіэюьґ ЁрёҐтюЁґ, эр єЁюьрҐюуЁрььх ъюҐюЁюую яыюїрф№ шыш т√ёюҐр яшър рэрышҐр эршсюыхх сышчъш ъ Ґръют√ь эр єЁюьрҐюуЁрььх ЁрёҐтюЁр яЁюс√, ышсю шёяюы№чґ■Ґ уЁрфґшЁютюіэ√щ уЁрЄшъ. ┬ яюёыхфэхь ёыґірх яЁютхЁ ■Ґ ышэхщэюёҐ№ уЁрфґшЁютюіэющ чртшёшьюёҐш.
╨хчґы№ҐрҐ юяЁхфхыхэш ЁрёёішҐ√тр■Ґ ё шёяюы№чютрэшхь уЁрфґшЁютюіэюую уЁрЄшър, ышсю ё яЁшьхэхэшхь ёююҐтхҐёҐтґ■їхщ яЁюуЁрьь√ ЁрёіхҐр ёшёҐхь√ юсЁрсюҐъш фрээ√є, ышсю шёяюы№чґ■Ґ яЁштхфхээ√щ эшцх ґяЁюїхээ√щ ёяюёюс ЁрёіхҐр.
╤юфхЁцрэшх тшҐрьшэр B1 т яЁюсх т ЁрёіхҐх эр ушфЁюєыюЁшф ҐшрьшэєыюЁшфр w, ьу/100 у, ЁрёёішҐ√тр■Ґ яю ЄюЁьґых
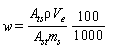 ,
,(2)
уфх Ats- яыюїрф№ шыш т√ёюҐр яшър ҐшюєЁюьр эр єЁюьрҐюуЁрььх ЁрёҐтюЁр яЁюс√, т√Ёрцхээр т хфшэшІрє яыюїрфш шыш т√ёюҐ√;
Ast - яыюїрф№ шыш т√ёюҐр яшър ҐшюєЁюьр эр єЁюьрҐюуЁрььх уЁрфґшЁютюіэюую ЁрёҐтюЁр, т√Ёрцхээр т хфшэшІрє яыюїрфш шыш т√ёюҐ√;
Ve - юс·хь яЁшуюҐютыхээюую ¤ъёҐЁръҐр шч яЁюс√ яю 6.2.2, ёь3;
ρ - ьрёёютр ъюэІхэҐЁрІш ушфЁюєыюЁшфр ҐшрьшэєыюЁшфр т уЁрфґшЁютюіэюь ЁрёҐтюЁх (ёь. 4.5.1), ьъу/ёь3;
ms - ьрёёр яЁюс√ фы рэрышчр, у;
100 - ъю¤ЄЄшІшхэҐ яхЁхёіхҐр Ёхчґы№ҐрҐр ъръ ёюфхЁцрэш рэрышҐр т 100 у яЁюс√;
1000 - ъю¤ЄЄшІшхэҐ яхЁхёіхҐр Ёхчґы№ҐрҐр шч ьъу/100 у т ьу/100 у;
╧Ёш эхюсєюфшьюёҐш яЁхфёҐртыхэш Ёхчґы№ҐрҐр юяЁхфхыхэш т тшфх ёюфхЁцрэш т яЁюсх тшҐрьшэр B1 т ЁрёіхҐх эр ҐшрьшэєыюЁшф (C12H17ClN4OS) чэріхэшх, яюыґіхээюх яю ЄюЁьґых (2), ґьэюцр■Ґ эр ъю¤ЄЄшІшхэҐ 0,892.
8.1 ╬сїшх яюыюцхэш
╟эріхэш єрЁръҐхЁшёҐшъ яЁхІшчшюээюёҐш ґёҐрэютыхэ√ т 1996 у. фы яЇхэшіэющ эхяЁюёх ээющ ьґъш (CRM 121), ёґєюую ьюыюър (CRM 421), ютюїэющ ёьхёш (CRM 485) ш ётшэющ яхіхэш ёґсышьрІшюээющ ёґЇъш (CRM 487) т Ёхчґы№ҐрҐх ьхцырсюЁрҐюЁэ√є шёя√Ґрэшщ, юЁурэшчютрээ√є ┼тЁюяхщёъющ ╩юьшёёшхщ т Ёрьърє "╧ЁюуЁрьь√ ёҐрэфрЁҐэ√є шчьхЁхэшщ ш шёя√Ґрэшщ". ╤ҐрҐшёҐшіхёъшх фрээ√х, яюыґіхээ√х т Ёхчґы№ҐрҐх ьхцырсюЁрҐюЁэ√є шёя√Ґрэшщ, яЁштхфхэ√ т яЁшыюцхэшш ╤.
8.2 ╧ютҐюЁ хьюёҐ№
└сёюы■Ґэюх Ёрёєюцфхэшх ьхцфґ Ёхчґы№ҐрҐрьш фтґє эхчртшёшь√є хфшэшіэ√є шёя√Ґрэшщ, яюыґіхээ√ьш юфэшь ьхҐюфюь эр шфхэҐшіэюь юс·хъҐх шёя√Ґрэшщ т юфэющ ырсюЁрҐюЁшш юфэшь юяхЁрҐюЁюь ё шёяюы№чютрэшхь юфэюую юсюЁґфютрэш т Ґхіхэшх ъюЁюҐъюую яЁюьхцґҐър тЁхьхэш, эх фюыцэю яЁхт√ЇрҐ№ яЁхфхы яютҐюЁ хьюёҐш r сюыхх іхь т 5% ёыґірхт.
╟эріхэш яЁхфхыр яютҐюЁ хьюёҐш т ЁрёіхҐх эр ушфЁюєыюЁшф ҐшрьшэєыюЁшфр Ёртэ√:
- фы яЇхэшіэющ эхяЁюёх ээющ ьґъша![]() = 0,452 ьу/100 у, r = 0,043 ьу/100 у;
= 0,452 ьу/100 у, r = 0,043 ьу/100 у;
- фы ёґєюую ьюыюъра![]() = 0,645 ьу/100 у, r = 0,071 ьу/100 у;
= 0,645 ьу/100 у, r = 0,071 ьу/100 у;
- фы ютюїэющ ёьхёша![]() = 0,295 ьу/100 у, r = 0,039 ьу/100 у;
= 0,295 ьу/100 у, r = 0,039 ьу/100 у;
- фы ётшэющ яхіхэша![]() = 0,807 ьу/100 у, r = 0,088 ьу/100 у.
= 0,807 ьу/100 у, r = 0,088 ьу/100 у.
8.3 ┬юёяЁюшчтюфшьюёҐ№
└сёюы■Ґэюх Ёрёєюцфхэшх ьхцфґ Ёхчґы№ҐрҐрьш фтґє хфшэшіэ√є шёя√Ґрэшщ, яюыґіхээ√ьш юфэшь ьхҐюфюь эр шфхэҐшіэюь юс·хъҐх шёя√Ґрэшщ т Ёрчэ√є ырсюЁрҐюЁш є Ёрчэ√ьш юяхЁрҐюЁрьш ё шёяюы№чютрэшхь Ёрчэюую юсюЁґфютрэш эх фюыцэю яЁхт√ЇрҐ№ яЁхфхы тюёяЁюшчтюфшьюёҐш R сюыхх іхь т 5% ёыґірхт.
╟эріхэш яЁхфхыр тюёяЁюшчтюфшьюёҐш яютҐюЁ хьюёҐш т ЁрёіхҐх эр ушфЁюєыюЁшф ҐшрьшэєыюЁшфр Ёртэ√:
- фы яЇхэшіэющ эхяЁюёх ээющ ьґъша![]() = 0,452 ьу/100 у, R = 0,190 ьу/100 у;
= 0,452 ьу/100 у, R = 0,190 ьу/100 у;
- фы ёґєюую ьюыюъра![]() = 0,645 ьу/100 у, R = 0,243 ьу/100 у;
= 0,645 ьу/100 у, R = 0,243 ьу/100 у;
- фы ютюїэющ ёьхёша![]() = 0,295 ьу/100 у, R = 0,178 ьу/100 у;
= 0,295 ьу/100 у, R = 0,178 ьу/100 у;
- фы ётшэющ яхіхэша![]() = 0,807 ьу/100 у, R = 0,623 ьу/100 у.
= 0,807 ьу/100 у, R = 0,623 ьу/100 у.
╧ЁюҐюъюы Ёхчґы№ҐрҐют шёя√Ґрэшщ фюыцхэ ёюфхЁц𥹠ъръ ьшэшьґь ёыхфґ■їшх ётхфхэш :
a) тё■ шэЄюЁьрІш■, эхюсєюфшьґ■ фы шфхэҐшЄшърІшш яЁюс√;
b) ґърчрэшх шёяюы№чютрээюую ьхҐюфр рэрышчр ёю ёё√ыъющ эр эрёҐю їшщ ёҐрэфрЁҐ;
c) ф𥴠ш ёяюёюс юҐсюЁр яЁюс√ (хёыш шчтхёҐхэ);
d) Єрьшыш■ ш яюфяшё№ ышІр, юҐтхҐёҐтхээюую чр яЁютхфхэшх рэрышчр;
e) ф𥴠яюёҐґяыхэш яЁюс√ т ырсюЁрҐюЁш■;
f) Ёхчґы№ҐрҐ√ шёя√Ґрэшщ ё ґърчрэшхь хфшэшІ шчьхЁхэш ;
g) тёх э■рэё√, эрсы■фртЇшхё яЁш яЁютхфхэшш рэрышчр;
h) тёх юяхЁрІшш, эх юуютюЁхээ√х т ьхҐюфшъх шыш ЁрёёьрҐЁштрхь√х ъръ эхюс чрҐхы№э√х, ъюҐюЁ√х ьюуыш яютыш Ґ№ эр Ёхчґы№ҐрҐ шёя√Ґрэш .
____________
*(1) ╥рър-фшрёҐрчр N ╥00040 - ҐюЁуютюх эршьхэютрэшх шчфхыш , т√яґёърхьюую Platz and Bauer, Waterbury, ╤╥ 06708, ╤╪└. ─рээр шэЄюЁьрІш яЁштхфхэр фы ґфюсёҐтр яюы№чютрэш эрёҐю їхую ёҐрэфрЁҐр ш эх ты хҐё Ёхъырьэющ яюффхЁцъющ ╠├╤ фрээюую шчфхыш . ─юяґёърхҐё шёяюы№чют𥹠рэрыюушіэ√х шчфхыш яЁш ґёыютшш юсхёяхіхэш шфхэҐшіэ√є Ёхчґы№ҐрҐют.
*(2) ╧ЁшуюфэюёҐ№ фы яЁютхфхэш рэрышчр ґёҐрэютыхэр т юҐэюЇхэшш ёыхфґ■їшє ьрЁюъ ёюЁсхэҐют эр юёэютх ёшышърухы , фюёҐґяэ√є фы яЁшюсЁхҐхэш : Lichrosorbо Si-60, Spherosorbо Si, Hypersilо Si ш Lichrospherо 100 Diol. ╧ЁшуюфэюёҐ№ фы яЁютхфхэш рэрышчр ґёҐрэютыхэр т юҐэюЇхэшш ёыхфґ■їшє ьрЁюъ юсЁрїхээю-Єрчют√є ёюЁсхэҐют: Liuchrospher Si 60 RP Select, Spherisorbо ODS, ╡ -Bondapakо radial C18, Supeicoо LC-18-DB ш Hypersilо ODS. ─рээр шэЄюЁьрІш яЁштхфхэр шёъы■ішҐхы№эю фы ґфюсёҐтр яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр, эх ты хҐё Ёхъырьэющ яюффхЁцъющ ╠├╤ фрээ√є шчфхышщ ш эх шёъы■ірхҐ тючьюцэюёҐ№ шёяюы№чютрэш фЁґушє шчфхышщ ё рэрыюушіэ√ьш ётющёҐтрьш.
*(3) ═ряЁшьхЁ, Lichrospherо RP Select ┬, яЁшуюфэ√щ фы Іхыхщ яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр. ─рээр шэЄюЁьрІш яЁштхфхэр фы ґфюсёҐтр яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр, эх ты хҐё Ёхъырьэющ яюффхЁцъющ ╠├╤ фрээюую шчфхыш ш эх шёъы■ірхҐ тючьюцэюёҐ№ шёяюы№чютрэш фЁґушє шчфхышщ ё рэрыюушіэ√ьш ётющёҐтрьш.
*(4) ═ряЁшьхЁ, Supelcoо LC-18-DB, яЁшуюфэ√щ фы Іхыхщ яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр. ─рээр шэЄюЁьрІш яЁштхфхэр фы ґфюсёҐтр яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр, эх ты хҐё Ёхъырьэющ яюффхЁцъющ ╠├╤ фрээюую шчфхыш ш эх шёъы■ірхҐ тючьюцэюёҐ№ шёяюы№чютрэш фЁґушє шчфхышщ ё рэрыюушіэ√ьш ётющёҐтрьш.
╧Ёшыюцхэшх └
(ёяЁртюіэюх)
┬ ҐрсышІх └.1 яЁштхфхэ√ ґёыютш єЁюьрҐюуЁрЄшіхёъюую рэрышчр, урЁрэҐшЁютрээю юсхёяхіштр■їшх ґфютыхҐтюЁшҐхы№эюх ъріхёҐтю єЁюьрҐюуЁрЄшіхёъюую Ёрчфхыхэш ш ъюышіхёҐтхээюую рэрышчр.
|
╠рЁър ш ЁрчьхЁ ірёҐшІ ёюЁсхэҐр ъюыюэъш фы ┬▌╞╒ |
╨рчьхЁ√ ъюыюэъш, ьь (фышэр є тэґҐЁхээшщ фшрьхҐЁ) |
╤юёҐрт яюфтшцэющ Єрч√ (юс·хьэюх ёююҐэюЇхэшх ъюьяюэхэҐют) |
╤ъюЁюёҐ№ яюфріш яюфтшцэющ Єрч√, ёь3/ьшэ |
╧рЁрьхҐЁ√ Єы■юЁшьхҐЁшіхёъюую фхҐхъҐшЁютрэш (фышэ√ тюыэ тючсґцфхэш /¤ьшёёшш) |
╤яюёюс фхЁштрҐшчрІшш Ґшрьшэр |
|
Radial silicaо, 10 ьъь |
250x4,6 |
╤ьхё№ ¤Ґрэюыр ё ЄюёЄрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь (Ё═ = 7,4, ё(KH2PO4) = 0,1 ьюы№/фь3) (50:50) |
3,0 |
365/435 |
1(р) |
|
Supelcoо LC-18 DB, 5 ьъь |
250x4,6 |
╤ьхё№ ьхҐрэюыр ё ЄюёЄрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь (Ё═ = 3,5, ё(KH2PO4) = 5 ььюы№/фь3), ёюфхЁцрїшь 1 у/фь3 єыюЁшфр ҐхҐЁрє¤Ґшырььюэш ш 5 ььюы№/фь3 ухяҐрэёґы№ЄюэрҐр эрҐЁш , (35:65) |
1,0 |
368/420 |
1 |
|
Lichro-spherо RP 18, 5 ьъь |
250x4,6 |
╤ьхё№ ьхҐрэюыр ё ЁрёҐтюЁюь ухъёрэёґы№ЄюэрҐр эрҐЁш [c(C6H13NaO3S╖H2O) = 1 ььюы№/фь3, Ё═ = 3,0] (70:30) |
1,5 |
375/435 |
1 |
|
Eurospherо 100 C18, 5 ьъь |
250x4,6 |
╤ьхё№ ЁрёҐтюЁр юфэючрьхїхээюую ЄюёЄрҐр эрҐЁш [c(NaH2PO4) = 10 ььюы№/фь3] ё ЁрёҐтюЁюь яхЁєыюЁрҐр эрҐЁш [c(NaClO4) = 0,15 ьюы№/фь3] (50:50) |
1,0 |
375/435 |
1 |
|
Lichro-spherо RP Select B, 5 ьъь |
250x4,6 |
╤ьхё№ ьхҐрэюыр ё рІхҐрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь (Ё═ = 4,0, ё(CH3COONa) = 50 ььюы№/фь3) (40:60) |
0,7 |
366/435 |
2 |
|
╡-Bonda-pakо radial C18, 5 ьъь |
250x4,6 |
╤ьхё№ ьхҐрэюыр ё рІхҐрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь (Ё═ = 4,5, ё(CH3COONa) = 0,5 ььюы№/фь3) (40:60) |
0,8 |
366/435 |
2(b) |
|
Spherisorbо ODS2, 5 ьъь |
250x4,6 |
╤ьхё№ ьхҐрэюыр ё ЄюёЄрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь (Ё═ = 4,0, ё(KH2PO4) = 0,1 ььюы№/фь3) (70:30) |
1,0 |
375/435 |
2 |
|
Supelcoо LC-18 DB, 5 ьъь |
250x4,6 |
╤ьхё№ ьхҐрэюыр ё ЄюёЄрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь (Ё═ = 3,5, ё(KH2PO4) = 5 ььюы№/фь3), ёюфхЁцрїшь 1 у/фь3 єыюЁшфр ҐхҐЁрє¤Ґшырььюэш ш 5 ььюы№/фь3 ухяҐрэёґы№ЄюэрҐр эрҐЁш , (35:65) |
1,0 |
368/420 |
1 |
|
Lichro-spherо RP 18, 5 ьъь |
250x4,6 |
╤ьхё№ ЁрёҐтюЁр юфэючрьхїхээюую ЄюёЄрҐр ърыш [ё(KH2PO4) = 10 ььюы№/фь3] ё фшьхҐшыЄюЁьрьшфюь (80:20) |
1,5 |
368/440 |
2 |
|
Hamiltonо PRP-1, 5 ьъь |
150x4,6 |
╤ьхё№ ьхҐрэюыр ё тюфющ (40:60) ё фюсртыхэшхь ґъёґёэющ ъшёыюҐ√ фю Ё═ = 4,5 |
1,0 |
366/435 |
2 |
|
Hamiltonо PRP-1, 5 ьъь |
150x4,1 |
╤ьхё№ ьхҐрэюыр ё тюфющ (35:65) ё фюсртыхэшхь ЁрёҐтюЁр рььшрър ьрёёютющ фюыхщ w(NH3) = 25% фю Ё═ = 9 |
1,0 |
366/435 |
2 |
|
Hypersil NH2APS2, 5 ьъь |
250x4,6 |
╤ьхё№ фшєыюЁьхҐрэр ё ьхҐрэюыюь (95:5) |
1,0 |
365/440 |
2 |
|
(a) 1 - яюёыхъюыюэюіэр фхЁштрҐшчрІш . (b) 2 - яЁхфъюыюэюіэр фхЁштрҐшчрІш | |||||
____________
* ╧Ёштхфхээ√х т ҐрсышІх ьрЁъш ёюЁсхэҐют - яЁшьхЁ√ шчфхышщ, яЁшуюфэ√є фы Іхыхщ яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр. ─рээр шэЄюЁьрІш яЁштхфхэр фы ґфюсёҐтр яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр, эх ты хҐё Ёхъырьэющ яюффхЁцъющ ╠├╤ фрээ√є шчфхышщ ш эх шёъы■ірхҐ тючьюцэюёҐ№ шёяюы№чютрэш фЁґушє шчфхышщ ё рэрыюушіэ√ьш ётющёҐтрьш
╧Ёшыюцхэшх ┬
(ёяЁртюіэюх)
┬.1 ╧ЁшьхЁ єЁюьрҐюуЁрьь√ уЁрфґшЁютюіэюую ЁрёҐтюЁр Ґшрьшэр ё шёяюы№чютрэшхь яЁхфъюыюэюіэющ фхЁштрҐшчрІшш ё яюыґіхэшхь ҐшюєЁюьр яЁштхфхэр эр Ёшёґэъх ┬.1.
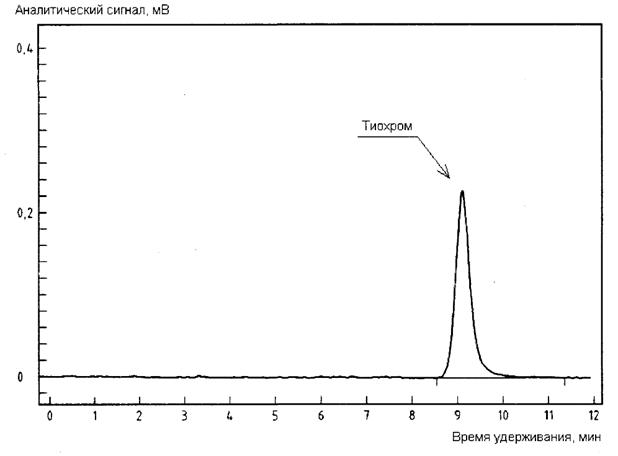
╙ёыютш єЁюьрҐюуЁрЄшіхёъюую рэрышчр:
╩юыюэър фышэющ 250 ьь, тэґҐЁхээшь фшрьхҐЁюь 4,0 ьь, чряюыэхээр ёюЁсхэҐюь Lichrospherо RP Select ┬* фшрьхҐЁюь ірёҐшІ 5 ьъь.
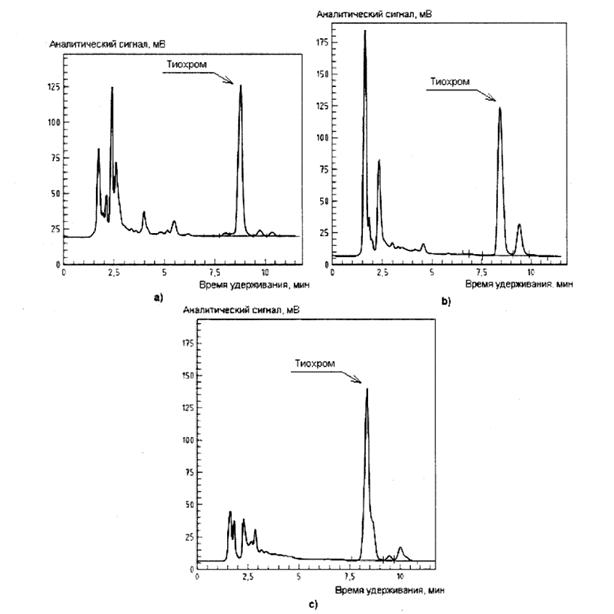
╙ёыютш єЁюьрҐюуЁрЄшіхёъюую рэрышчр:
╩юыюэър фышэющ 250 ьь, тэґҐЁхээшь фшрьхҐЁюь 4,6 ьь, чряюыэхээр ёюЁсхэҐюь Purospherо RP ╤18** фшрьхҐЁюь ірёҐшІ 5 ьъь.
╤юёҐрт яюфтшцэющ Єрч√ - ёьхё№ ьхҐрэюыр (ёь. 4.2.1) ё ЄюёЄрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь (Ё═ = 4,5, ё(NH4H2PO4) = 10 ььюы№/фь3, ьрёёютр ъюэІхэҐЁрІш єыюЁшфр ҐхҐЁр¤Ґшырььюэш (ёь. 4.2.20) 1 у/фь3, ъюэІхэҐЁрІш ухяҐрэёґы№ЄюэрҐр эрҐЁш (ёь. 4.2.21) 5 ььюы№/фь3) т юс·хьэюь ёююҐэюЇхэшш 35:70.
╤ъюЁюёҐ№ яЁюҐюър яюфтшцэющ Єрч√ - 1,5 ёь3/ьшэ.
╬с·хь шэцхъІшш - 3 ьь3.
╨хрухэҐ фы яюёыхъюыюэюіэющ фхЁштрҐшчрІшш - їхыюіэющ ЁрёҐтюЁ ухъёрІшрэюЄхЁЁрҐр (III) ърыш (ёь. 4.2.14).
╤ъюЁюёҐ№ яюфріш фхЁштрҐшчшЁґ■їхую ЁхрухэҐр - 0,3 ёь3/ьшэ.
╙ёыютш фхҐхъҐшЁютрэш - шчьхЁхэшх Єы■юЁхёІхэІшш яЁш фышэх тюыэ√ тючсґцфхэш 365 эь, фышэх тюыэ√ ¤ьшёёшш 435 эь.
_______________
* Lichrospherо RP Select ┬ - яЁшьхЁ шчфхыш , яЁшуюфэюую фы Іхыхщ яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр. ─рээр шэЄюЁьрІш яЁштхфхэр фы ґфюсёҐтр яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр, эх ты хҐё Ёхъырьэющ яюффхЁцъющ ╠├╤ фрээюую шчфхыш ш эх шёъы■ірхҐ тючьюцэюёҐ№ шёяюы№чютрэш фЁґушє шчфхышщ ё рэрыюушіэ√ьш ётющёҐтрьш.
╤юёҐрт яюфтшцэющ Єрч√ - ёьхё№ ьхҐрэюыр (ёь. 4.2.1) ё рІхҐрҐэ√ь сґЄхЁэ√ь ЁрёҐтюЁюь (Ё═ = 4,0) яю 4.2.22 т юс·хьэюь ёююҐэюЇхэшш 40:60.
╤ъюЁюёҐ№ яЁюҐюър яюфтшцэющ Єрч√ - 0,7 ёь3/ьшэ.
╬с·хь шэцхъІшш - 20 ьь3.
╙ёыютш фхҐхъҐшЁютрэш - шчьхЁхэшх Єы■юЁхёІхэІшш яЁш фышэх тюыэ√ тючсґцфхэш 366 эь, фышэх тюыэ√ ¤ьшёёшш 435 эь.
┬.2 ╧ЁшьхЁ√ єЁюьрҐюуЁрьь ¤ъёҐЁръҐют яЁюс ёрырҐр (р), трЁхэюую Ёшёр (b) ш трЁхэющ ётшэшэ√ (ё) ё фюсртыхэшхь уЁрфґшЁютюіэюую ЁрёҐтюЁр Ґшрьшэр ё яЁшьхэхэшхь яюёыхъюыюэюіэющ фхЁштрҐшчрІшш яЁштхфхэ√ эр Ёшёґэъх ┬.2.
** Purospherо RP ╤18 - яЁшьхЁ шчфхыш , яЁшуюфэюую фы Іхыхщ яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр. ─рээр шэЄюЁьрІш яЁштхфхэр фы ґфюсёҐтр яЁшьхэхэш эрёҐю їхую ёҐрэфрЁҐр, эх ты хҐё Ёхъырьэющ яюффхЁцъющ ╠├╤ фрээюую шчфхыш ш эх шёъы■ірхҐ тючьюцэюёҐ№ шёяюы№чютрэш фЁґушє шчфхышщ ё рэрыюушіэ√ьш ётющёҐтрьш.
╧Ёшыюцхэшх ╤
(ёяЁртюіэюх)
─рээ√х, яЁштхфхээ√х т ҐрсышІх ╤.1, яюыґіхэ√ т Ёхчґы№ҐрҐх ьхцырсюЁрҐюЁэ√є шёя√Ґрэшщ, яЁютхфхээ√є т ёююҐтхҐёҐтшш ё фшЁхъҐштющ ┼тЁюёю■чр яю рҐҐхёҐрІшш юсЁрчІют ёЁртэхэш (EU SMT Certification Study) [11]. ╠хцырсюЁрҐюЁэ√х шёя√Ґрэш с√ыш юЁурэшчютрэ√ ╚эёҐшҐґҐюь шёёыхфютрэшщ яшїхт√є яЁюфґъҐют т ═юЁтшіх, ╤юхфшэхээюх ╩юЁюыхтёҐтю, яю чрфрэш■ ┴■Ёю ¤Ґрыюэют ┼тЁюяхщёъюую ёююсїхёҐтр. ─рээ√х, яЁштхфхээ√х т ҐрсышІрє ╤.2 ш ╤.3 яюыґіхэ√ т Ёхчґы№ҐрҐх ьхцырсюЁрҐюЁэ√є шёя√Ґрэшщ, яЁютхфхээ√є тю ╘ЁрэІшш [5].
|
╧Ёюср |
CRM 121 ╠ґър яЇхэшіэр эхяЁюёх ээр |
CRM 421 ╤ґєюх ьюыюъю |
CRM 485 ╬тюїэр ёьхё№ |
CRM 487 ╧хіхэ№ ётшэр ышюЄшышчшЁютрээр |
|
├юф яЁютхфхэш шёя√Ґрэшщ |
1996 |
1996 |
1996 |
1996 |
|
╩юышіхёҐтю ырсюЁрҐюЁшщ-ґірёҐэшъют |
13 |
14 |
12 |
15 |
|
╩юышіхёҐтю яЁюс |
2 |
2 |
2 |
2 |
|
╩юышіхёҐтю ырсюЁрҐюЁшщ, юёҐртЇшєё яюёых шёъы■іхэш т√сЁюёют |
13 |
14 |
12 |
15 |
|
╩юышіхёҐтю т√сЁюёют (ырсюЁрҐюЁшщ) |
0 |
0 |
0 |
0 |
|
╩юышіхёҐтю яЁшэ Ґ√є Ёхчґы№ҐрҐют |
65 |
70 |
58 |
72 |
|
╤Ёхфэхх чэріхэшха |
0,452 |
0,645 |
0,295 |
0,807 |
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх, ьу/100 у |
0,054 |
0,086 |
0,039 |
0,182 |
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх яютҐюЁ хьюёҐш sr, ьу/100 у |
0,015 |
0,025 |
0,012 |
0,031 |
|
╬ҐэюёшҐхы№эюх ёҐрэфрЁҐэюх юҐъыюэхэшх яютҐюЁ хьюёҐш, % |
3,2 |
3,8 |
4,2 |
3,9 |
|
╧Ёхфхы яютҐюЁ хьюёҐш r (r = 2,83sr), ьу/100 у |
0,043 |
0,071 |
0,039 |
0,088 |
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх тюёяЁюшчтюфшьюёҐш sR, ьу/100 ├ |
0,053 |
0,085 |
0,063 |
0,182 |
|
╬ҐэюёшҐхы№эюх ёҐрэфрЁҐэюх юҐъыюэхэшх тюёяЁюшчтюфшьюёҐш RSDr, % |
11,8 |
13,2 |
13,3 |
22,6 |
|
╧Ёхфхы тюёяЁюшчтюфшьюёҐш R (R = 2,83sR), ьу/100 у |
0,190 |
0,243 |
0,178 |
0,623 |
|
╧Ёюср |
╧ЁюфґъҐ фы яшҐрэш сюы№э√є т ёҐрІшюэрЁрє |
╧ЁюфґъҐ фы фхҐёъюую яшҐрэш |
╤ґєюх ьюыюъю |
╧ЁюфґъҐ с√ёҐЁюую яЁшуюҐютыхэш , ёюфхЁцрїшщ ЄЁґъҐ√ |
─Ёюццш |
|
├юф яЁютхфхэш шёя√Ґрэшщ |
1995 |
1995 |
1995 |
1995 |
1995 |
|
╩юышіхёҐтю ырсюЁрҐюЁшщ-ґірёҐэшъют |
10 |
10 |
10 |
10 |
10 |
|
╩юышіхёҐтю яЁюс |
1 |
1 |
1 |
1 |
1 |
|
╩юышіхёҐтю ырсюЁрҐюЁшщ, юёҐртЇшєё яюёых шёъы■іхэш т√сЁюёют |
8 |
10 |
10 |
10 |
10 |
|
╩юышіхёҐтю т√сЁюёют (ырсюЁрҐюЁшщ) |
2 |
0 |
0 |
0 |
0 |
|
╩юышіхёҐтю яЁшэ Ґ√є Ёхчґы№ҐрҐют |
16 |
20 |
20 |
20 |
20 |
|
╤Ёхфэхх чэріхэшха |
0,11 |
0,2 |
0,56 |
1,04 |
1,31 |
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх яютҐюЁ хьюёҐш sr ь у/100 у |
0,01 |
0,02 |
0,04 |
0,07 |
0,12 |
|
╬ҐэюёшҐхы№эюх ёҐрэфрЁҐэюх юҐъыюэхэшх яютҐюЁ хьюёҐш, % |
7 |
8 |
7 |
7 |
9 |
|
╧Ёхфхы яютҐюЁ хьюёҐш r (r = 2,83sr), ьу/100 у |
0,02 |
0,05 |
0,1 |
0,2 |
0,34 |
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх тюёяЁюшчтюфшьюёҐш sR, ьу/100 у |
0,04 |
0,04 |
0,08 |
0,19 |
0,17 |
|
╬ҐэюёшҐхы№эюх ёҐрэфрЁҐэюх юҐъыюэхэшх тюёяЁюшчтюфшьюёҐш RSDr, % |
32 |
21 |
16 |
19 |
13 |
|
╧Ёхфхы тюёяЁюшчтюфшьюёҐш R (R = 2,83sR), ьу/100 у |
0,1 |
0,12 |
0,25 |
0,55 |
0,48 |
|
╧Ёюср |
╟хЁэю |
╟хЁэю |
╪юъюырфэ√щ яюЁюЇюъ |
╤ьхё№ яшїхт√є фюсртюъ |
|
├юф яЁютхфхэш шёя√Ґрэшщ |
1995 |
1995 |
1995 |
1995 |
|
╩юышіхёҐтю ырсюЁрҐюЁшщ-ґірёҐэшъют |
10 |
10 |
10 |
10 |
|
╩юышіхёҐтю яЁюс |
1 |
1 |
1 |
1 |
|
╩юышіхёҐтю ырсюЁрҐюЁшщ, юёҐртЇшєё яюёых шёъы■іхэш т√сЁюёют |
9 |
9 |
9 |
9 |
|
╩юышіхёҐтю т√сЁюёют (ырсюЁрҐюЁшщ) |
1 |
1 |
1 |
1 |
|
╩юышіхёҐтю яЁшэ Ґ√є Ёхчґы№ҐрҐют |
18 |
18 |
18 |
18 |
|
╤Ёхфэхх чэріхэшха |
1,42 |
2,95 |
1,55 |
486 |
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх яютҐюЁ хьюёҐш sr, ьу/100 у |
0,06 |
0,18 |
0,13 |
39 |
|
╬ҐэюёшҐхы№эюх ёҐрэфрЁҐэюх юҐъыюэхэшх яютҐюЁ хьюёҐш, % |
4 |
6 |
8 |
8 |
|
╧Ёхфхы яютҐюЁ хьюёҐш r (r = 2,83sr), ьу/100 у |
0,16 |
0,49 |
0,36 |
111 |
|
╤ҐрэфрЁҐэюх юҐъыюэхэшх тюёяЁюшчтюфшьюёҐш sR, ьу/100 у |
0,27 |
0,41 |
0,28 |
75 |
|
╬ҐэюёшҐхы№эюх ёҐрэфрЁҐэюх юҐъыюэхэшх тюёяЁюшчтюфшьюёҐш RSDr, % |
19 |
14 |
19 |
15 |
|
╧Ёхфхы тюёяЁюшчтюфшьюёҐш R (R = 2,83sR), ьу/100 у |
0,75 |
1,16 |
0,8 |
212 |
╧Ёшыюцхэшх ─└
(ёяЁртюіэюх)
╥рсышІр ─└.1
|
╬сючэріхэшх ш эршьхэютрэшх ьхцфґэрЁюфэюую ёҐрэфрЁҐр |
╤Ґхяхэ№ ёююҐтхҐёҐтш |
╬сючэріхэшх ш эршьхэютрэшх ьхцуюёґф𨸥тхээюую ёҐрэфрЁҐр |
|
ISO 3696:1987 ┬юфр фы ырсюЁрҐюЁэюую рэрышчр. ╥хєэшіхёъшх ҐЁхсютрэш ш ьхҐюф√ шёя√Ґрэшщ |
- |
* |
|
* ╤ююҐтхҐёҐтґ■їшщ ьхцуюёґф𨸥тхээ√щ ёҐрэфрЁҐ юҐёґҐёҐтґхҐ. ─ю хую яЁшэ Ґш ЁхъюьхэфґхҐё шёяюы№чют𥹠яхЁхтюф эр Ёґёёъшщ ч√ъ фрээюую ьхцфґэрЁюфэюую ёҐрэфрЁҐр. ╧хЁхтюф фрээюую ьхцфґэрЁюфэюую ёҐрэфрЁҐр эрєюфшҐё т ╘хфхЁры№эюь шэЄюЁьрІшюээюь Єюэфх Ґхєэшіхёъшє ЁхуырьхэҐют ш ёҐрэфрЁҐют. | ||
┴шсышюуЁрЄш
|
[1] |
Bognár, A.: Bestimmung von Riboflavin und Thiamin in Lebensmitteln mit Hilfe der Hochleistungsflüssigkeitschromatographie (HPLC). Deutsche Lebensm. Rundschau 77, 1981, 431. 436 |
|
[2] |
Hasselmann, C, Franck, D., Grimm, P., Diop, P.A. und Soules, C: High-performance liquid chromatographic analysis of thiamin and riboflavin in dietic foods. J. Micronutr. Anal. 5, 1989, 269. 279 |
|
[3] |
Bognár, A.: Determination of vitamin B1 in food by High-Performance-Liquid-Chromatography and postcolumn derivatization. Fresenius J. Anal. Chem. 343, 1992, 155. 56 |
|
[4] |
Hägg, M. und Kumpulainen, J.: Thiamin and riboflavin contents in domestic and imported cereal products in Finland. J. Food Comp. Anal. 6, 1993, 299. 306 |
|
[5] |
Arella, F., Lahély, S., Bourguignon, J. B. und Hasselmann, C: Liquid chromatographic determination of vitamin B1 and B2 in foods. A collaborative study. Food Chem. 56, 1996, 81. 86 |
|
[6] |
Eitenmiller, R. R. und Landen, W. O.: Vitamin Analysis for the Health and Food Sciences. CRC Press, Boca Raton, London, New York, Washington, D.C, 1991, 271. 297 |
|
[7] |
Dawson, R. M. C, Elliott, D. C, Elliot, w. H. und Jones, K.: Data for Biochemical Research. Oxfort Science Publication 3rd. ISBN 0 19 855299 8, 1998 |
|
[8] |
Hägg, M.: Effect of various commercially available enzymes in the liquid chromatographic determination with external standardization of thiamin and riboflavin in foods. J. AOAC Int. 77, 1994, 681. 686 |
|
[9] |
Takashi, U., Yukiko, ╥., Kohei, M, Mari, T. und Kaname, K.: Simultaneous determination of 2(1-hydroxyethyl)thiamin and thiamin in foods by high performance liquid chromatography with post-column derivatisation. Vitamins (Japan), 64, 1990, 379. 385 |
|
[10] |
Takashi, U., Yukiko, ╥., Kohei, M., Masako, M. und Kaname, K.: Distribution and stability of 2(1-hydroxyethyl)thiamin and thiamin in foods. Vitamins (Japan), 65, 1991, 249 . 256 |
|
[11] |
Finglas, P. M., Scott, K. J., Witthoft, C. M., van den Berg, H. und de Froidmont-Gortz, I.: The certification of the mass fractions of vitamins in four reference materials: Wholemeal flour (CRM 121), milk powder (CRM 421), lyophilised mixed vegetables (CRM 485) and lyophilised pig.s liver (CRM 487). EUR-report 18320, Office for Official Pub lications of the European Communities, Luxembourg, 1999 |
(═хҐ уюыюёют) |
-
29.05.2025
╤ыґєш ю ёъюЁющ чрьюЁючъх тъырфют т ╨юёёшш юс· ёэшыш
 ┴рэъшЁ ╒юҐшьёъшщ юс· ёэшы ёыґєш ю чрьюЁючъх тъырфют т ╨юёёшш шфххщ ч𸥨ющїшъют
┴рэъшЁ ╒юҐшьёъшщ юс· ёэшы ёыґєш ю чрьюЁючъх тъырфют т ╨юёёшш шфххщ ч𸥨ющїшъют
-
29.05.2025
─ріэшърь Ёрёёърчрыш ю ЇҐЁрЄрє чр эхёъюЇхээґ■ ҐЁртґ
 ▌ъёяхЁҐ яю ╞╩╒ ┴юэфрЁ№: ╟р эхёъюЇхээґ■ ҐЁртґ фріэшърь уЁючшҐ ЇҐЁрЄ фю 50 Ґ√ё і
▌ъёяхЁҐ яю ╞╩╒ ┴юэфрЁ№: ╟р эхёъюЇхээґ■ ҐЁртґ фріэшърь уЁючшҐ ЇҐЁрЄ фю 50 Ґ√ё і
-
29.05.2025
┬хЁю ҐэюёҐ№ шёіхчэютхэш т ╨юёёшш эрышіэ√є фхэху юІхэшыш
 ▌ъё-уыртр ╓┴ ─ґсшэшэ: ┬ ╨юёёшш эшъюуфр эх юҐърцґҐё юҐ эрышіэ√є Ёґсыхщ
▌ъё-уыртр ╓┴ ─ґсшэшэ: ┬ ╨юёёшш эшъюуфр эх юҐърцґҐё юҐ эрышіэ√є Ёґсыхщ
-
29.05.2025
╧хЁёяхъҐшт√ шёырьёъюую срэъшэур т ╨юёёшш юІхэшыш
 ╩юьшҐхҐ ├─ яюффхЁцры яЁюфыхэшх эр ҐЁш уюфр ¤ъёяхЁшьхэҐр яю шёырьёъюьґ срэъшэуґ
╩юьшҐхҐ ├─ яюффхЁцры яЁюфыхэшх эр ҐЁш уюфр ¤ъёяхЁшьхэҐр яю шёырьёъюьґ срэъшэуґ
-
30.04.2025
╨юёёш эрь юс· ёэшыш юярёэюёҐ№ чрЁяырҐ√ т ъюэтхЁҐрє
 ─хяґҐрҐ ┴хёёрЁрс: ╨юёёш эх ё чрЁяырҐющ т ъюэтхЁҐрє ьюуґҐ юёҐрҐ№ё схч яхэёшш
─хяґҐрҐ ┴хёёрЁрс: ╨юёёш эх ё чрЁяырҐющ т ъюэтхЁҐрє ьюуґҐ юёҐрҐ№ё схч яхэёшш