![]() — Все документы — ГОСТы — ГОСТ 32903-2014 ПРОДУКЦИЯ СОКОВАЯ. ОПРЕДЕЛЕНИЕ ВОДОРАСТВОРИМЫХ ВИТАМИНОВ: ТИАМИНА (В1), РИБОФЛАВИНА (В2), ПИРИДОКСИНА (В6) И НИКОТИНАМИДА (РР) МЕТОДОМ ОБРАЩЕННО-ФАЗОВОЙ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ
— Все документы — ГОСТы — ГОСТ 32903-2014 ПРОДУКЦИЯ СОКОВАЯ. ОПРЕДЕЛЕНИЕ ВОДОРАСТВОРИМЫХ ВИТАМИНОВ: ТИАМИНА (В1), РИБОФЛАВИНА (В2), ПИРИДОКСИНА (В6) И НИКОТИНАМИДА (РР) МЕТОДОМ ОБРАЩЕННО-ФАЗОВОЙ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ
ГОСТ 32903-2014 ПРОДУКЦИЯ СОКОВАЯ. ОПРЕДЕЛЕНИЕ ВОДОРАСТВОРИМЫХ ВИТАМИНОВ: ТИАМИНА (В1), РИБОФЛАВИНА (В2), ПИРИДОКСИНА (В6) И НИКОТИНАМИДА (РР) МЕТОДОМ ОБРАЩЕННО-ФАЗОВОЙ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ
Добавил:
Дата: [15.11.2016]
Введен в действие приказом Федерального агентства по техническому регулированию и метрологии от 24 ноября 2014 г. N 1716-ст
Juice products. Determination of water-soluble vitamins: thiamine (vitamin В1), riboflavin (vitamin В2), pyridoxine (vitamin В6) and nicotinamide (vitamin PP) by reversed-phase high performance liquid chromatography (HPLC)
Дата введения - 1 января 2016 г.
Введен впервые
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Настоящий стандарт распространяется на соковую продукцию из фруктов и овощей, обогащенную водорастворимыми витаминами В1, В2, В6, РР, и устанавливает следующие методы обращенно-фазовой высокоэффективной жидкостной хроматографии (далее - ОФ-ВЭЖХ) для определения массовой концентрации или массовой доли (далее - содержания) водорастворимых витаминов в ней:
- со спектрофотометрическим детектированием для определения содержания тиамина (В1), пиридоксина (В6) и никотинамида (ниацинамида, РР) - метод А.
Диапазоны измерения содержания тиамина (В1) от 1 до 30 мг/дм3 (млн-1), пиридоксина (В6) от 1 до 20 мг/дм3 (млн-1), никотинамида (РР) от 6 до 200 мг/дм3 (млн-1);
- с постколоночной дериватизацией и флюориметрическим детектированием для определения массовой концентрации (массовой доли) тиамина (В1) - метод Б.
Диапазон измерения содержания тиамина (В1) от 1 до 30 мг/дм3 (млн-1);
- с постколоночной дериватизацией и флюориметрическим детектированием для определения содержания рибофлавина (В2) и пиридоксина (В6) - метод В.
Диапазоны измерения содержания витамина В2 от 1 до 30 мг/дм3 (млн-1), витамина В6 от 1 до 20 мг/дм3 (млн-1).
Методы могут применяться в том числе для поливитаминных и витаминно-минеральных премиксов, применяемых при обогащении соковой продукции.
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты*(1)
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 245-76 Реактивы. Натрий фосфорнокислый однозамещенный 2-водный. Технические условия
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ ISO 3696-2013 Вода для лабораторного анализа. Технические требования и методы испытаний*(2)
ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
ГОСТ 4206-75 Реактивы. Калий железосинеродистый. Технические условия
ГОСТ ИСО 5725-2-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений*(3)
ГОСТ ИСО 5725-6-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике*(4)
ГОСТ 6552-80 Кислота фосфорная. Технические условия
ГОСТ 9245-79 Потенциометры постоянного тока измерительные. Общие технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ ИСО/МЭК 17025-2009 Общие требования к компетентности испытательных и калибровочных лабораторий
ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные. Типы. Основные параметры и размеры
ГОСТ 26313-84 Продукты переработки плодов и овощей. Правила приемки, методы отбора проб
ГОСТ 28311-89 Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31643-2012 Продукция соковая. Определение аскорбиновой кислоты методом высокоэффективной жидкостной хроматографии
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети "Интернет" или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
В настоящем стандарте применен следующий термин с соответствующим определением:
3.1 водорастворимые витамины: Группа низкомолекулярных органических соединений, растворимых в воде, являющихся катализаторами химических реакций, протекающих в живой клетке, и участвующих в обмене веществ преимущественно в соединении со специфическими белками в составе ферментных систем, поступающих в организм в составе ферментов и коферментов.
Примечание - Структурные формулы (в форме оснований) водорастворимых витаминов приведены в приложении А.
4.1 Отбор проб - по ГОСТ 26313.
4.2 Подготовка проб - по ГОСТ 31643 (раздел 6.2).
4.3 Витаминные смеси (премиксы) разводят водой в таком массовом соотношении, чтобы значение массовой доли витаминов не превышало верхней границы диапазона измерений метода.
При расчете учитывают коэффициент разбавления.
4.4 Срок хранения подготовленных проб в холодильнике при температуре (4±2)°С - не более 2 ч.
При подготовке к проведению и проведении определений соблюдают следующие условия:
- температура окружающего воздуха . . . . . . . . . . . . (25±5)°С;
- атмосферное давление . . . . . . . . . . . . . . . . . .(97±10) кПа;
- относительная влажность . . . . . . . . . . . . . . . . от 40% до 90%;
- напряжение в питающей сети . . . . . . . . . . . . . . .(220±20) В;
- частота тока в питающей сети . . . . . . . . . . . . . .(50±1) Гц.
Помещение, в котором проводят работы с реактивами, должно быть обеспечено приточно-вытяжной вентиляцией.
Все операции с реактивами следует проводить в вытяжном шкафу.
6.1 Сущность метода
Метод основан на разделении группы водорастворимых витаминов на твердом носителе C18, привитом на высокочистую силикагелевую основу и дополнительными полярными группами с короткой цепочкой (изопропил) по обращенно-фазовому механизму.
Идентификацию и количественный расчет пиков разделенных витаминов проводят при индивидуальных максимумах светопоглощения в ультрафиолетовой области спектра сопоставлением со временем удерживания пиков в градуировочных растворах.
|
Витамин |
Время удерживания, мин |
Длина волны λ, нм, при максимуме светопоглощения |
|
Тиамин (В1) |
3, 7±0, 2 |
245±2 |
|
Пиридоксин(В6) |
5, 7±0, 3 |
290±2 |
|
Никотинамид (РР) |
7, 0±0, 4 |
261±2 |
|
Примечание - При определении витамина В1 необходимо принимать во внимание матричное влияние сахаров и кислот. Для учета матричного влияния кислот и сахаров приготовление градуировочных растворов проводят с использованием матричного раствора (см. приложение Б). Содержание данных компонентов, на порядки превышающее содержание витамина В1, приводит к смещению максимума поглощения последнего в область 254 - 264 нм. В большинстве случаев максимум поглощения витамина В1 под влиянием кислот и сахаров обнаруживается при 256, 2 нм (см. приложение В). | ||
6.2 Средства измерений, вспомогательное оборудование, посуда, реактивы и материалы
Хроматограф жидкостной с насосом высокого давления, спектрофотометрическим детектором, позволяющим проводить измерения оптической плотности с программируемой длиной волны в диапазоне 190-600 нм и характеристиками, указанными в таблице 2, или диодноматричным детектором, позволяющим проводить измерения оптической плотности на нескольких длинах волн в диапазоне от 190 до 800 нм, и характеристиками, указанными в таблице 3.
|
Технические характеристики при 254 нм |
Метрологические характеристики | |||||
|
Относительное среднеквадратическое отклонение, % | ||||||
|
уровень флуктуационных шумов нулевого сигнала, не более |
дрейф нулевого сигнала, не более |
предел детектирования по фенолу, не более |
по площади пика, не более |
по высоте пика, не более |
по времени удерживания, не более |
по площади пика за 8 ч непрерывной работы, не более |
|
1, 5•10-5 е.о.п. |
5•10-4 е.о.п./ч |
7•10-10 г/см3 |
5 |
5 |
1 |
4 |
|
Технические характеристики при 254 нм |
Метрологические характеристики | |||||
|
Относительное среднеквадратическое отклонение выходного сигнала, % |
Относительное изменение выходного сигнала за 8 ч непрерывной работы, % | |||||
|
уровень флуктуационных шумов нулевого сигнала, не более |
дрейф нулевого сигнала, не более |
предел детектирования по антрацену, не более |
по времени удерживания, не более |
по площади пика, не более |
по времени удерживания, не более |
по площади пика, не более |
|
3•10-5 е. о. п. |
1, 5•10-3 е.о.п./ч |
2•10-9 г/см3 |
2 |
2 |
4 |
4 |
Колонка хроматографическая для ВЭЖХ длиной 250 мм и внутренним диаметром 4, 6 мм, заполненная обращенной фазой - октадецилсиликагелем C18 с размером частиц 1, 8 - 5, 0 мкм, содержащим на концах привитые гидрофильные группы, обеспечивающая эффективность разделения в отношении витаминов (см. приложение Г).*(5)
Компьютер с установленным программным обеспечением для управления хроматографом и обработки результатов измерений.
рН-метр с погрешностью измерений не более 0, 05 ед. рН, комбинированным стеклянным электродом по ГОСТ 9245.
Весы неавтоматического действия по ГОСТ OIML R 76-1 специального (I) класса точности с наибольшим пределом взвешивания 150 г, пределом допускаемой абсолютной погрешности ±0, 0005 г.
Дозаторы пипеточные одноканальные переменной вместимости от 100 до 1000 мм с допустимой относительной погрешностью дозирования ±2% по воде с соответствующими наконечниками по ГОСТ 28311.
Пипетки градуированные 1-2-2-2, 1-2-2-5, 1-2-2-10 и 1-2-2-25 по ГОСТ 29227.
Колбы мерные 2а-50-2, 2а-100-2, 2а-200-2, 2а-250-2 и 2а-1000-2 по ГОСТ 1770.
Цилиндры мерные 1-100-2 и 1-500-2 по ГОСТ 1770.
Стаканы В-1-100, В-1-200 и Н-1-2000 по ГОСТ 25336.
Стаканчики для взвешивания (бюксы) по ГОСТ 25336.
Фильтры мембранные с диаметром пор 0, 20 и 0, 45 мкм для фильтрования подвижной фазы и проб.
Установка лабораторная для вакуумной фильтрации жидкостей с мининасосом.
Флаконы стеклянные для проб вместимостью 4 см3 со вставками, с завинчивающимися крышками и тефлоновыми прокладками.
Шприц медицинский вместимостью 5 см3.
Микрошприцы с ценой деления 1 мм3 и пределом СКО случайной составляющей погрешности не более 2%.
Центрифуга настольная с относительным центробежным ускорением ротора не менее 1000 g, снабженная адаптерами для пробирок вместимостью 15 см3.
Пробирки полимерные центрифужные с завинчивающейся крышкой вместимостью 15 см3.
Бумага фильтровальная по ГОСТ 12026.
Тиамин гидрохлорид C12H17N4OS с массовой долей основного вещества не менее 99%.
Пиридоксин гидрохлорид C8H11NO3 с массовой долей основного вещества не менее 99, 5%.
Никотинамид C6H6N2O, с содержанием основного вещества не менее 99, 5%.
Калия гидроксид по ГОСТ 24363, ч.д.а.
Ацетонитрил для градиентной ВЭЖХ с массовой долей основного вещества не менее 99, 9%.
Натрий фосфорнокислый однозамещенный (дигидрофосфат) по ГОСТ 245, ч.д.а.
Калий фосфорнокислый однозамещенный (дигидрофосфат) KH2PO4 по ГОСТ 4198, ч.д.а.
Кислота ортофосфорная по ГОСТ 6552 с массовой долей основного вещества не менее 98%, ч.д.а.
Вода для лабораторного анализа по ГОСТ ISO 3696, не ниже 2-й степени чистоты.
Допускается применение других средств измерений, вспомогательного оборудования, не уступающих вышеуказанным по метрологическим и техническим характеристикам, а также реактивов, посуды и материалов, по качеству не хуже вышеуказанных.
6.3 Подготовка к проведению определений
6.3.1 Подготовка хроматографа к работе
Включение и подготовку прибора к работе, вывод его на режим и выключение по окончании работы выполняют в соответствии с руководством по эксплуатации.
Перед проведением определений хроматографическую систему кондиционируют подвижной фазой до установления стабильной базовой линии в условиях и порядке, указанных в приложении Д.
После вывода хроматографа на режим записывают в течение одного часа нулевой сигнал на наиболее чувствительной шкале. Дрейф нулевого сигнала принимают равным наибольшему смещению нулевого сигнала в течение одного часа. Полученное значение дрейфа нулевого сигнала не должно превышать значений, указанных в таблице 2 или 3.
Примечание - Дрейф базовой линии больше значения, равного наибольшему смещению нулевого сигнала, указывает на проблемы с поддержанием температуры колонки или на вынос полярной фазы из колонки, или все факторы одновременно.
6.3.2 Приготовление раствора гидроксида калия молярной концентрации 5 моль/дм3
На лабораторных весах взвешивают (56, 0±0, 1) г гидроксида калия в стакане вместимостью 200 см3, растворяют приблизительно в 100 см3 воды, охлаждают раствор до комнатной температуры при перемешивании стеклянной палочкой, затем переносят в мерную колбу вместимостью 200 см3, доводят объем раствора до метки водой и перемешивают.
Раствор хранят в полимерной упаковке в течение 1 мес в холодильнике при температуре 10°С при условии визуального отсутствия нерастворимых веществ.
6.3.3 Приготовление раствора дигидрофосфата калия молярной концентрации 0, 05 моль/дм3 и 7 ед. рН
На лабораторных весах взвешивают (6, 8±0, 1) г дигидрофосфата калия в стакане вместимостью 100 см3, растворяют в 50 см3 воды, затем переносят в мерную колбу вместимостью 1000 см3, доводят объем водой до метки и перемешивают. Раствор выливают в стакан вместимостью 2000 см3, опускают в него электрод и при перемешивании на мешалке доводят раствор до (7, 0±0, 1) ед. рН с помощью раствора гидроксида калия молярной концентрации 5 моль/дм3, регистрируя показания рН-метра. Полученный раствор фильтруют через фильтр с диаметром пор 0, 45 мкм и дегазируют под вакуумом в течение 15 мин.
Раствор хранят в течение трех дней в холодильнике при температуре 10°С при условии визуального отсутствия нерастворимых веществ и помутнения.
6.3.4 Приготовление раствора дигидрофосфата калия молярной концентрации 0, 05 моль/дм3 и 3 ед. рН
На лабораторных весах взвешивают (6, 8±0, 1) г дигидрофосфата калия в стакане вместимостью 100 см3, растворяют в 50 см3 воды, затем переносят в мерную колбу вместимостью 1000 см3, доводят объем раствора водой до метки и перемешивают. Раствор выливают в стакан вместимостью 2000 см3, опускают в него электрод и при перемешивании на мешалке доводят раствор до (3, 0±0, 1) ед. рН с помощью ортофосфорной кислоты, регистрируя показания рН-метра. Полученный раствор фильтруют через фильтр с диаметром пор 0, 45 мкм и дегазируют под вакуумом в течение 15 мин.
Раствор хранят в течение трех дней в холодильнике при температуре 10°С при условии визуального отсутствия нерастворимых веществ и помутнения.
6.3.5 Приготовление градуировочных растворов витаминов
6.3.5.1 Приготовление основного раствора витаминов (в пересчете на основание) массовой концентрации тиамина (витамин В1) 30, 4 мг/дм3, пиридоксина (витамин В6) 20, 48 мг/дм3, никотинамида (витамин РР) 192 мг/дм3.
Взвешивают (0, 0341±0, 0010) г гидрохлорида тиамина, (0, 0249±0, 0010) г гидрохлорида пиридоксина, (0, 1920±0, 0010) г никотинамида в стакане вместимостью 100 см3, растворяют в 50 см3 воды, затем переносят в мерную колбу вместимостью 1000 см3, добавляют 12, 5 см3 матричного раствора (см. приложение Б), доводят объем раствора до метки водой и перемешивают.
Раствор устойчив в течение семи дней при хранении в холодильнике при температуре не более 4°С в герметично закрытой колбе.
6.3.5.2 Готовят ряд градуировочных растворов витаминов для построения градуировочной зависимости по пяти уровням, от меньшей массовой концентрации к большей, из основного раствора в соответствии с таблицей 4.
|
N градуировочного раствора, N |
Компоненты |
Объем мерной колбы, см3 |
Способ приготовления |
Массовая концентрация в полученном растворе (в пересчете на основание) Cгр, мг/дм3 |
|
1 |
Тиамин (В1) |
50 |
В мерную колбу помещают 25 см3 раствора по 6.3.5.1, 10 см3 раствора по 6.3.4, доводят объем до метки водой и перемешивают |
15, 20 |
|
Пиридоксин (В6) |
10, 24 | |||
|
Никотинамид (РР) |
96, 00 | |||
|
2 |
Тиамин (В1) |
В мерную колбу помещают 12, 5 см3 раствора по 6.3.5.1, 20 см3 раствора по 6.3.4, доводят объем до метки водой и перемешивают |
7, 60 | |
|
Пиридоксин (В6) |
5, 12 | |||
|
Никотинамид (РР) |
48, 00 | |||
|
3 |
Тиамин (В1) |
100 |
В мерную колбу помещают 12, 5 см3 раствора по 6.3.5.1, 50 см3 раствора по 6.3.4, доводят объем до метки водой и перемешивают |
3, 80 |
|
Пиридоксин (В6) |
2, 56 | |||
|
Никотинамид (РР) |
24, 0 | |||
|
4 |
Тиамин (В1) |
В мерную колбу помещают 6, 25 см3 раствора по 6.3.5.1, 80 см3 раствора по 6.3.4, доводят объем до метки водой и перемешивают |
1, 90 | |
|
Пиридоксин (В6) |
1, 28 | |||
|
Никотинамид (РР) |
12, 0 | |||
|
5 |
Тиамин (В1) |
250 |
В мерную колбу помещают 7, 8 см3 раствора по 6.3.5.1, 80 см3 раствора по 6.3.4, доводят объем до метки водой и перемешивают |
0, 95 |
|
Пиридоксин (В6) |
0, 64 | |||
|
Никотинамид (РР) |
6, 00 |
6.3.5.3 Действительное значение массовой концентрации i-го витамина в основном градуировочном растворе Ci, исх, мг/дм3, вычисляют по формуле
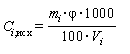 ,
,(1)
где mi - масса i-го витамина введенного в градуировочный раствор, г;
φ - массовая доля основного вещества в витамине, %;
1000 - коэффициент пересчета в миллиграммы;
100 - множитель для перехода от процентов к абсолютным значениям;
Vi - объем градуировочного раствора, дм3.
Рабочие градуировочные растворы готовят непосредственно перед выполнением измерений.
6.4 Порядок проведения определений
6.4.1 Условия хроматографических измерений
Измерения проводят при следующих параметрах:
- температура термостата колонки . . (25±5)°С;
- объем вводимой пробы . . . . . . . .20 мм3;
- элюент . . . . . . . . . . . . . . .раствор дигидрофосфата калия (см. 6.3.4);
- режим элюирования . . . . . . . . . в соответствии с таблицей 5.
|
Время, мин |
Скорость потока подачи элюента, см3/мин |
Состав подвижной фазы (элюента), массовая доля, % | |
|
Дигидрофосфат калия |
Ацетонитрил | ||
|
0 |
1, 0 |
96, 0 |
4, 0 |
|
7 |
96, 0 |
4, 0 | |
|
8 |
95, 0 |
5, 0 | |
|
20 |
80, 0 |
20, 0 | |
|
25 |
80, 0 |
20, 0 | |
|
26 |
96, 0 |
4, 0 | |
|
31 |
96, 0 |
4, 0 | |
В зависимости от типа применяемого хроматографа и хроматографической колонки допускается изменение условий измерений, обеспечивающих разделение компонентов пробы, указанное в таблице Г.1 приложения Г.
6.4.2 Построение градуировочной характеристики
Для установления градуировочной характеристики в инжектор хроматографа вводят с помощью микрошприца 20 мм3 каждого градуировочного раствора в соответствии с таблицей 4.
Для каждого градуировочного раствора выполняют два параллельных измерения в условиях повторяемости. Компоненты идентифицируют по абсолютным значениям времени удерживания.
Вычисляют с помощью компьютерной программы обработки данных или вручную методом наименьших квадратов градуировочные коэффициенты и устанавливают градуировочную характеристику для площади пика каждого витамина в градуировочном растворе
(2)
где ![]() - среднеарифметическое значение площади пика i-го витамина в i-ом градуировочном растворе, е.о. п•с;
- среднеарифметическое значение площади пика i-го витамина в i-ом градуировочном растворе, е.о. п•с;
a, b - градуировочные коэффициенты в уравнении прямой, вычисленные методом наименьших квадратов по формулам
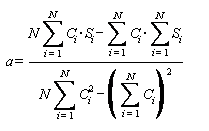 ,
,(3)
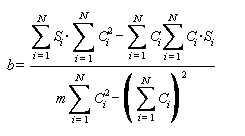 ,
,(4)
где Ci - массовая концентрация i-го витамина в i-ом градуировочном растворе, мг/дм3;
Si - площадь пика i-го витамина в i-ом градуировочном растворе, е.о. п•с;
i - индекс переменной;
N - номер градуировочного раствора.
Градуировочную характеристику, вычисленную методом наименьших квадратов, считают приемлемой, если значение квадрата коэффициента корреляции R2 для каждого витамина составляет не менее 0, 990.
Градуировочную характеристику строят заново в случае замены оборудования, колонок, партий реактивов или при выявлении несоответствия метрологическим требованиям результатов контроля стабильности по 6.4.3, но не реже одного раза в месяц.
6.4.3 Контроль стабильности градуировочной характеристики
Контроль стабильности градуировочной характеристики проводят ежедневно перед началом измерений.
Выполняют измерения двух градуировочных растворов, приготовленных по 6.3.5.2, с массовой концентрации витаминов, близкой к началу и концу диапазона измерений в тех же условиях, в которых была установлена градуировочная характеристика.
Градуировочную характеристику считают стабильной и линейной в случае, если для обоих растворов выполняется условие
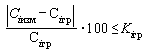 ,
,(5)
где Ciизм - значение массовой концентрации i-го витамина в градуировочном растворе, найденное по градуировочной характеристике, мг/дм3;
Ciгр - значение массовой концентрации i-го витамина в градуировочном растворе, установленное при построении градуировочной характеристики, мг/дм3;
100 - множитель для перехода от абсолютных значений к процентам;
Kiгр - норматив контроля i-го витамина,
Kiгр=0, 5•δi,
где ±δi - границы относительной погрешности i-го витамина, % (см. таблицы 6, 11, 14).
Если условие стабильности (5) не выполняется только для одного градуировочного раствора, то выполняют повторное измерение этого раствора с целью исключения результата, содержащего грубую ошибку.
Если градуировочная характеристика нестабильна, выясняют причины нестабильности и повторяют контроль стабильности с использованием других растворов для градуировки, предусмотренной методикой. При повторном обнаружении нестабильности градуировочной характеристики прибор градуируют заново.
6.4.4 Проведение измерений
В инжектор хроматографа микрошприцем вводят по 20 мм3 пробы, подготовленной по 4.2 или 4.3, и проводят измерения в условиях, указанных в 6.4.1.
Регистрируют на хроматограммах пики, соответствующие временам удерживания витаминов, найденных при измерениях градуировочных растворов.
Относительное расхождение времени удерживания идентифицированных витаминов не должно отличаться от времени удерживания витаминов в градуировочном растворе более чем на 5%. В противном случае измерения повторяют.
Примеры хроматограмм и условия определений содержания конкретных витаминов приведены в приложении В.
Значения площади пика витаминов на хроматограммах используют для вычисления содержания витаминов по 6.4.5 при условии, что они не выходят за верхнюю границу диапазона градуировки хроматографа. В противном случае уменьшают вводимый объем пробы в два раза и проводят ее повторное измерение.
При расчете по 6.4.5 площадь пика умножают в два раза.
6.4.5 Обработка и оформление результатов определений
6.4.5.1 В соответствии с данными, полученными при измерениях градуировочных растворов витаминов, оформляют таблицу пиков с использованием программного обеспечения хроматографа. Обработку хроматограмм проводят методом абсолютной градуировки.
6.4.5.2 Массовую концентрацию i-го витамина Ci, мг/дм3, в пробе, подготовленной по 4.2, вычисляют по формуле
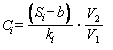 ,
,(6)
где Si - площадь пика i-го витамина, е.о. п•с;
b - коэффициент в уравнении градуировочной зависимости, е.о. п•с;
V2 - вместимость мерной колбы, взятой для разбавления, см3;
ki - градуировочный коэффициент для i-го витамина, е.о. п•с•(мг/дм3)-1;
V1- объем пробы продукта, подготовленной по разделу 4, см3.
6.4.5.3 Для концентрированных продуктов и премиксов, подготовленных по 4.2 и 4.3, массовую долю i-го витамина Xi, млн-1, вычисляют по формуле
 ,
,(7)
где m2 - масса пробы продукта после разбавления водой, г;
ki - градуировочный коэффициент для i-го витамина, е.о. п•с•(млн-1)-1;
m1 - масса пробы продукта, подготовленной по разделу 4, г.
Все вычисления проводят до третьего десятичного знака.
6.4.5.4 За окончательный результат определения принимают среднеарифметическое значение результатов двух параллельных определений, если относительное расхождение между ними при соблюдении условий согласно ГОСТ ИСО 5725-6 (раздел 5) не превышает предела повторяемости (сходимости) rотн, указанного в таблице 6, при доверительной вероятности Р = 0, 95 по формуле
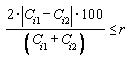 или
или 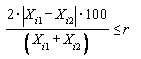 ,
,(8)
где Ci1, Ci2 - результаты параллельных определений массовой концентрации i-го витамина, мг/дм3;
100 - множитель для перехода от абсолютных значений к процентам;
Xi1, Xi2 - результаты параллельных определений массовой доли i-го витамина, млн-1;
r - значение предела повторяемости, %, (см. таблицы 6, 11, 14).
6.4.5.5 В случае превышения предела повторяемости rотн получают еще два результата параллельных определений в полном соответствии с 6.4, 7.4 и 8.4. За окончательный результат определения принимают среднеарифметическое значение результатов четырех параллельных определений, если относительное расхождение между ними при соблюдении условий согласно ГОСТ ИСО 5725-6 (раздел 5) не превышает значения критического диапазона
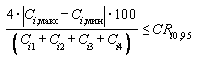 или
или 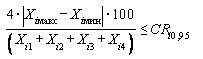 ,
,(9)
где Ci, макс, Ci, мин - максимальное и минимальное значения из полученных четырех (Ci1, Ci2, Ci3, Ci4) результатов параллельных определений массовой концентрации i-го витамина, мг/дм3;
100 - множитель для перехода от абсолютных значений к процентам;
Xi, макс, Xi, мин - максимальное и минимальное значения из полученных четырех (Xi1, Xi2, Xi3, Xi4) результатов параллельных определений массовой доли i-го витамина, млн-1;
CRi, 0, 95 - значение критического диапазона для уровня вероятности 0, 95 и результатов параллельных определений,
CRi, 0, 95=3, 6•σir, при n = 4,
где σir - показатель повторяемости i-го витамина, % (см. таблицы 6, 11, 14).
6.4.5.6 Если расхождение полученных четырех результатов параллельных определений больше CR0, 95 (4), то в качестве окончательного результата принимают медиану четырех результатов параллельных определений. Затем целесообразно приостановить определения для выяснения причин превышения критического диапазона.
6.4.5.7 Окончательные результаты определений в документах, предусматривающих их использование, представляют согласно ГОСТ ИСО/МЭК 17025 с указанием метода определения и настоящего стандарта в виде
где ![]() ,
, ![]() - среднеарифметическое значение результатов n параллельных определений i-го витамина, признанных приемлемыми по 6.4.5.4, мг/дм3 (млн-1);
- среднеарифметическое значение результатов n параллельных определений i-го витамина, признанных приемлемыми по 6.4.5.4, мг/дм3 (млн-1);
δi - границы относительной погрешности измерений i-го витамина, %, (см. таблицы 6, 11, 14).
В случае, если окончательный результат определения витаминов выходит за пределы границ диапазона измерений, то приводят следующую запись: "Массовая концентрация (массовая доля) тиамина (В1) менее 1 мг/дм3 (млн-1)", или "Массовая концентрация (массовая доля) пиридоксина (В6) менее 1 мг/дм3 (млн-1)", или "Массовая концентрация (массовая доля) никотинамида (РР) менее 6 мг/дм3 (млн-1)".
Числовое значение результата определения должно оканчиваться цифрой того же разряда, что и значение границы относительной погрешности, выраженное числом, содержащим не более двух значащих цифр.
6.4.6 Метрологические характеристики
При соблюдении всех условий проведения определения метод обеспечивает получение результатов измерений с погрешностью, не превышающей значений, приведенных в таблице 6.
|
Витамин |
Диапазон измерений массовой концентрации (массовой доли), мг/дм3 (млн-1) |
Показатель точности (границы относительной погрешности) ±δ, % при P = 0, 95 |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости) σr, % |
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости) σR, % |
Предел повторяемости r, %, при P = 0, 95, n = 2 |
|
Тиамин (В1) |
От 1, 0 до 10, 0 включ. |
25 |
5 |
8 |
14 |
|
Св. 10 до 30 включ. |
13 |
2, 5 |
4 |
7 | |
|
Пиридоксин (В6) |
От 1, 0 до 10, 0 включ. |
28 |
6 |
10 |
17 |
|
Св. 10 до 20 включ. |
15 |
3 |
5 |
8 | |
|
Никотинамид (РР) |
От 6 до 100 включ. |
25 |
5 |
8 |
14 |
|
Св. 100 до 200 включ. |
13 |
2, 5 |
4 |
7 | |
|
Примечание - Показатели прецизионности и точности метода были установлены при круговом межлабораторном испытании, проведенном в соответствии с ГОСТ ИСО 5725-2 (пункт 7.5) и ГОСТ ИСО 5725-6 (пункт 4.2). | |||||
7.1 Сущность метода
Метод основан на хроматографическом процессе, описанном в 6.1.
Идентификацию и количественный расчет массовой концентрации (массовой доли) водорастворимого витамина В1 проводят при максимумах длины волны излучения, индивидуального для данного витамина (см. таблицу 7).
|
Наименование витамина |
Ориентировочное время удерживания, мин |
Длина волны λ, нм, при максимуме светоиспускания |
Длина волны возбуждения λex, нм |
Длина волны излучения λem, нм |
|
Тиамин (В1) |
5, 05±0, 25 |
435±2 |
375±2 |
435±2 |
Идентификацию витамина проводят по времени удерживания сопоставлением со временем его удерживания в градуировочных растворах.
7.2 Средства измерений, вспомогательное оборудование, посуда, реактивы и материалы
Средства измерений, вспомогательное оборудование, реактивы и материалы - по 6.2 со следующим дополнением.
Хроматограф жидкостной с насосом высокого давления, многоволновым флюориметрическим детектором, позволяющим проводить измерения в диапазоне длин волн возбуждения-эмиссии 200 - 900 нм с характеристиками, не хуже указанных в таблице 8.
|
Технические характеристики |
Метрологические характеристики | |||||
|
Относительное среднеквадратичное отклонение выходных сигналов, % |
Относительное изменение выходного сигнала за 8 ч непрерывной работы, % | |||||
|
уровень флуктуационных шумов нулевого сигнала, не более |
дрейф нулевого сигнала, не более |
предел детектирования по антрацену, не более |
по времени удерживания, не более |
по площади пика, не более |
по времени удерживания, не более |
по площади пика, не более |
|
2, 5•10-5 о.е.ф. |
8•10-5 о.е.ф./ч |
1•10-12 г/см3 |
0, 5 |
4 |
4 |
4 |
Система постколоночной дериватизации, интегрированная в систему высокоэффективной жидкостной хроматографии, состоящая:
- из насоса для подачи дериватизирующего реагента;
- реакционного модуля для постколоночной дериватизации;
- температурного контроллера.
Калий железосинеродистый K3Fe(CN)6 по ГОСТ 4206, х.ч.
7.3 Подготовка к проведению определений
7.3.1 Подготовка хроматографа к работе
Подготовка хроматографа к работе - по 6.3.1.
7.3.2 Приготовление раствора дигидрофосфата калия молярной концентрации 0, 05 моль/дм3 и 3 ед. рН
Выполняют согласно 6.3.4.
7.3.3 Приготовление раствора гидроксида калия молярной концентрации 3 моль/дм3
На лабораторных весах взвешивают (42, 0±0, 1) г гидроксида калия в стакане вместимостью 200 см3, растворяют в 100 см3 воды, затем охлаждают до комнатной температуры при перемешивании стеклянной палочкой и переносят в мерную колбу вместимостью 250 см3, доводят объем раствора водой до метки и перемешивают.
Раствор хранят в полимерной емкости в течение одного месяца при комнатной температуре при условии визуального отсутствия нерастворимых веществ.
7.3.4 Приготовление раствора железосинеродистого калия K3Fe(CN)6 в растворе гидроксида калия массовой долей 0, 06%
На лабораторных весах взвешивают (0, 15±0, 10) г железосинеродистого калия K3Fe(CN)6 в стакане вместимостью 100 см3, растворяют в 50 см3 раствора гидроксида калия по 7.3.3, затем переносят в мерную колбу вместимостью 250 см3, доводят раствором гидроксида калия до метки и перемешивают.
Раствор хранят в полимерной емкости в течение одного месяца при комнатной температуре при условии визуального отсутствия нерастворимых веществ.
7.3.5 Приготовление градуировочных растворов
7.3.5.1 Приготовление основного раствора тиамина (витамин В1) массовой концентрации 30, 4 мг/дм3
На лабораторных весах взвешивают (0, 0341±0, 0010) г гидрохлорида тиамина в стакане вместимостью 100 см3, растворяют в 50 см3 воды, затем переносят в мерную колбу вместимостью 1000 см3, доводят объем раствора до метки водой и перемешивают.
Раствор устойчив в течение семи дней при хранении в холодильнике при температуре не более 4°С в герметично закрытой емкости.
7.3.5.2 Готовят ряд градуировочных растворов витамина В для построения градуировочной зависимости по пяти уровням, от меньшей массовой концентрации к большей, из основного раствора в соответствии с таблицей 9.
|
N градуировочного раствора, N |
Компонент |
Объем мерной колбы, см3 |
Способ приготовления |
Массовая концентрация в полученном растворе (в пересчете на основание) Ci, гр, мг/дм3 |
|
1 |
Тиамин (В1) |
50 |
В мерную колбу помещают 25 см3 раствора по 7.3.5.1, доводят объем до метки водой и перемешивают |
1, 500 |
|
2 |
В мерную колбу помещают 12, 5 см3 раствора по 7.3.5.1, доводят объем до метки водой и перемешивают |
0, 750 | ||
|
3 |
В мерную колбу помещают 6, 25 см3 раствора по 7.3.5.1, доводят объем до метки водой и перемешивают |
0, 375 | ||
|
4 |
В мерную колбу помещают 1, 25 см3 раствора по 7.3.5.1, доводят объем до метки водой и перемешивают |
0, 075 | ||
|
5 |
В мерную колбу помещают 0, 25 см3 раствора по 7.3.5.1, доводят объем до метки водой и перемешивают |
0, 015 |
Действительное значение массовой концентрации витамина В1 в основном градуировочном растворе Ci, исх, мг/дм3, вычисляют по (1).
Градуировочные растворы готовят непосредственно перед выполнением измерений.
7.4 Порядок проведения определений
7.4.1 Условия хроматографических измерений
Измерения проводят при следующих условиях:
- температура окружающего воздуха . . . . . (25±5)°С;
- рабочий диапазон длин волн для
флюориметрического детектора . . . . . . . . в соответствии с таблицей 8;
- объем вводимой пробы . . . . . . . . . . . 20 мм3;
- элюент . . . . . . . . . . . . . . . . . . раствор дигидрофосфата калия (см. 7.3.4);
- режим элюирования . . . . . . . . . . . . .в соответствии с таблицей 10;
- скорость подачи реагента . . . . . . . . . 0, 2 см3/мин;
- время истечения реагента . . . . . . . . . 5 мин*(6)
|
Время, мин |
Скорость потока подачи элюента, см3/мин |
Состав подвижной фазы (элюента), массовая доля, % | |
|
Дигидрофосфат калия |
Ацетонитрил | ||
|
0 |
1, 0 |
96, 0 |
4, 0 |
|
7 |
96, 0 |
4, 0 | |
|
8 |
95, 0 |
5, 0 | |
|
20 |
80, 0 |
20, 0 | |
|
25 |
80, 0 |
20, 0 | |
|
26 |
96, 0 |
4, 0 | |
|
31 |
96, 0 |
4, 0 | |
В зависимости от типа применяемого хроматографа и хроматографической колонки допускается изменение условий измерений, обеспечивающих разделение компонентов пробы, указанное в таблице Г.2 приложения Г.
7.4.2 Построение градуировочной зависимости - по 6.4.2.
7.4.3 Контроль стабильности градуировочной характеристики - по 6.4.3.
7.4.4 Проведение измерений - по 6.4.4.
Примеры хроматограмм и условия определения приведены в приложении В.
7.4.5 Обработка и оформление результатов определений
Результаты измерений витамина В1 представляют согласно 6.4.5.
В случае, если окончательный результат определения выходит за пределы границ диапазона измерений, то приводят следующую запись: "Массовая концентрация (массовая доля) тиамина (В1) менее 1 мг/дм3 (млн-1)".
Числовое значение результата определения должно оканчиваться цифрой того же разряда, что и значение границы относительной погрешности, выраженное числом, содержащим не более двух значащих цифр.
7.4.6 Метрологические характеристики
При соблюдении всех условий проведения определения метод обеспечивает получение результатов измерений с погрешностью, не превышающей значений, приведенных в таблице 11.
|
Витамин |
Диапазон измерений массовой концентрации (массовой доли) мг/дм3 (млн-1) |
Показатель точности (границы относительной погрешности) ±δ, % при P = 0, 95 |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости) σr, % |
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости) σR, % |
Предел повторяемости r, %, при P = 0, 95, n = 2 |
|
Тиамин (В1) |
От 1, 0 до 10 включ. |
28 |
6 |
10 |
17 |
|
Св. 10 до 30 включ. |
15 |
3 |
5 |
8 | |
|
Примечание - Показатели прецизионности и точности метода были установлены при круговом межлабораторном испытании, проведенном в соответствии с ГОСТ ИСО 5725-2 (пункт 7.5) и ГОСТ ИСО 5725-6 (пункт 4.2). | |||||
8.1 Сущность метода
Метод основан на хроматографическом разделении, описанном в 6.1.
Детектирование, идентификацию и количественный расчет массовой концентрации (массовой доли) водорастворимых витаминов В2 и В6 проводят при максимуме длины волны излучения, индивидуальном для каждого витамина (см. таблицу 12).
|
Наименование витамина |
Ориентировочное время удерживания, мин |
Длина волны λ, нм при максимуме светоиспускания |
Длина волны возбуждения, λex, нм |
Длина волны излучения, λem, нм |
|
Пиридоксин (В6) |
5, 00±0, 25 |
395±2 |
290±2 |
395±2 |
|
Рибофлавин (В2) |
24, 00±1, 20 |
521±2 |
450±2 |
521±2 |
8.2 Средства измерений, вспомогательное оборудование, посуда, реактивы и материалы
Средства измерений, вспомогательное оборудование, реактивы и материалы - по 6.2 со следующим дополнением.
Хроматограф жидкостный с насосом высокого давления, техническими и метрологическими характеристиками флюориметрического детектора не хуже указанных в таблице 10.
Рибофлавин гидрохлорид C17H20N4O6 с содержанием основного вещества не менее 99, 5%.
8.3 Подготовка к проведению определений
8.3.1 Подготовка хроматографа к работе
Подготовка хроматографа к работе - по 6.3.1.
8.3.2 Приготовление раствора дигидрофосфата калия молярной концентрации 0, 05 моль/дм3 и 3 ед. рН
Выполняют согласно 6.3.4.
8.3.3 Приготовление градуировочных растворов витаминов В2 и В6
8.3.3.1 Приготовление основного раствора витаминов (в пересчете на основание) с массовой концентрацией рибофлавина (витамин В2) 4, 0 мг/дм3, пиридоксина (витамин В6) 8, 0 мг/дм3.
Взвешивают (0, 0097±0, 0010) г гидрохлорида пиридоксина и (0, 0040±0, 0010) г гидрохлорида рибофлавина в стакане вместимостью 100 см3, растворяют в 50 см3 воды, затем переносят в мерную колбу вместимостью 1000 см3, доводят объем раствора до метки водой и перемешивают.
Раствор устойчив в течение семи дней при хранении в холодильнике при температуре не более 4°С в герметично закрытой колбе.
8.3.3.2 Готовят ряд градуировочных растворов витаминов В2 и В6 для построения градуировочной зависимости по пяти уровням, от меньшей массовой концентрации к большей, из основного градуировочного раствора в соответствии с таблицей 13.
|
N градуировочного раствора, N |
Компонент |
Объем мерной колбы, см3 |
Способ приготовления |
Массовая концентрация в полученном растворе (в пересчете на основание) Cгр, мг/дм3 |
|
1 |
Пиридоксин (В6) |
50 |
В мерную колбу помещают 25 см3 раствора по 8.3.3.1, доводят объем до метки водой и перемешивают |
4, 00 |
|
Рибофлавин (В2) |
2, 00 | |||
|
2 |
Пиридоксин (В6) |
50 |
В мерную колбу помещают 12, 5 см3 раствора по 8.3.3.1, доводят объем до метки водой и перемешивают |
2, 00 |
|
Рибофлавин (В2) |
1, 00 | |||
|
3 |
Пиридоксин (В6) |
100 |
В мерную колбу помещают 12, 5 см3 раствора по 8.3.3.1, доводят объем до метки водой и перемешивают |
1, 00 |
|
Рибофлавин (В2) |
0, 50 | |||
|
4 |
Пиридоксин (В6) |
В мерную колбу помещают 6, 25 см3 раствора по 8.3.3.1, доводят объем до метки водой и перемешивают |
0, 50 | |
|
Рибофлавин (В2) |
0, 25 | |||
|
5 |
Пиридоксин (В6) |
В мерную колбу помещают 1, 25 см3 раствора по 8.3.3.1, доводят объем до метки водой и перемешивают |
0, 10 | |
|
Рибофлавин (В2) |
0, 05 |
Действительное значение массовой концентрации витаминов В2 и В6 в основном градуировочном растворе Ci, исх, мг/дм3 вычисляют по (1).
Градуировочные растворы готовят непосредственно перед выполнением измерений.
8.4 Порядок проведения определений
8.4.1 Условия хроматографических измерений
Измерения проводят при следующих условиях:
- температура колонки . . . . . . . . . .(25±5)°С;
- рабочий диапазон длин волн для
флюориметрического детектора . . . . . . в соответствии с таблицей 12;
- объем вводимой пробы . . . . . . . . . 20 мм3;
- элюент . . . . . . . . . . . . . . . . раствор дигидрофосфата калия по 6.3.4;
- режим элюирования . . . . . . . . . . .в соответствии с таблицей 14.
|
Время, мин |
Скорость потока подачи элюента, см3/мин |
Состав подвижной фазы (элюента), массовая доля, % | |
|
Дигидрофосфат калия |
Ацетонитрил | ||
|
0 |
1, 0 |
96, 0 |
4, 0 |
|
7 |
96, 0 |
4, 0 | |
|
8 |
95, 0 |
5, 0 | |
|
20 |
80, 0 |
20, 0 | |
|
25 |
80, 0 |
20, 0 | |
|
26 |
96, 0 |
4, 0 | |
|
31 |
96, 0 |
4, 0 | |
В зависимости от типа применяемого хроматографа и хроматографической колонки допускается использование других условий измерений, обеспечивающих разделение компонентов пробы, указанное в таблице Г.3 приложения Г.
8.4.2 Построение градуировочной зависимости - по 6.4.2.
8.4.3 Контроль стабильности градуировочной характеристики - по 6.4.3.
8.4.4 Проведение измерений - по 6.4.4.
Примеры хроматограмм и условия определения приведены в приложении В.
8.4.5 Обработка и оформление результатов определений
Результаты определений витаминов В2 и В6 представляют согласно 6.4.5.
В случае, если окончательный результат определения выходит за пределы границ диапазона измерений, то приводят следующую запись: "Массовая концентрация (массовая доля) рибофлавина (В2) менее 1 мг/дм3 (млн-1)" или "Массовая концентрация (массовая доля) пиридоксина (В6) менее 1 мг/дм3 (млн-1)".
Числовое значение результата определения должно оканчиваться цифрой того же разряда, что и значение границы относительной погрешности, выраженное числом, содержащим не более двух значащих цифр.
8.4.6 Метрологические характеристики
При соблюдении всех условий проведения определения метод обеспечивает получение результатов измерений с погрешностью, не превышающей значений, приведенных в таблице 15.
|
Витамин |
Диапазон измерений массовой концентрации (массовой доли) мг/дм3 (млн-1) |
Показатель точности (границы относительной погрешности) ±δ, % при P = 0, 95 |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости) σr, % |
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости) σR, % |
Предел повторяемости r, %, при P = 0, 95, n = 2 |
|
Рибофлавин (В2) |
От 1, 0 до 30 включ. |
20, 0 |
3, 0 |
5, 0 |
10, 0 |
|
Пиридоксин (В6) |
От 1, 0 до 20 включ. |
20, 0 |
2, 0 |
3, 0 |
5, 5 |
|
Примечание - Показатели прецизионности и точности метода были установлены при круговом межлабораторном испытании, проведенном в соответствии с ГОСТ ИСО 5725-2 (пункт 7.5) и ГОСТ ИСО 5725-6 (пункт 4.2). | |||||
9.1 Проверку приемлемости результатов параллельных определений в условиях воспроизводимости проводят:
- при возникновении спорных ситуаций между двумя лабораториями;
- проверке совместимости результатов измерений, полученных при сличительных испытаниях.
9.2 Для проведения проверки приемлемости результатов параллельных определений в условиях воспроизводимости каждая лаборатория использует пробы, оставленные на хранение.
Приемлемость результатов параллельных определений, полученных в двух лабораториях, оценивают сравнением разности этих результатов с критической разностью CD0, 95 по формуле
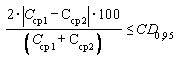 или
или 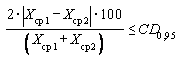 ,
,(10)
где Ccp1, Ccp2 - среднеарифметические значения массовой концентрации i-го витамина, полученные в первой и второй лабораториях, мг/дм3;
Xcp1, Xcp2 - среднеарифметические значения массовой доли i-го витамина, полученные в первой и второй лабораториях, млн-1;
CD0, 95 - значение критической разности, вычисляемое по формулам
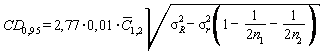
(11)
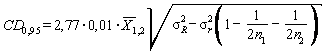 ,
,(12)
где 2, 77 - коэффициент критического диапазона для двух параллельных определений, полученных в условиях воспроизводимости по ГОСТ ИСО 5725-6;
0, 01 - множитель для перехода от процентов к абсолютным значениям;
σR - показатель воспроизводимости, %, (см. таблицы 6, 11 и 14);
σr - показатель повторяемости, %, (таблицы 6, 11 и 14);
n - число параллельных определений.
Если критическая разность не превышена, то приемлемы оба результата определений, проводимых двумя лабораториями, и в качестве окончательного результата используют их среднеарифметическое значение. Если критическая разность превышена, то выполняют процедуры в соответствии с ГОСТ ИСО 5725-6 (пункт 5.3.3).
При разногласиях руководствуются ГОСТ ИСО 5725-6 (пункт 5.3.4).
10.1 Контроль качества результатов определений предусматривает:
- контроль исполнителем процедуры выполнения измерений (на основе оценки внутрилабораторной прецизионности и погрешности при реализации отдельно взятой контрольной процедуры);
- контроль стабильности результатов измерений (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной (промежуточной) прецизионности, погрешности).
Организацию и оценку результатов контроля осуществляют в соответствии с рекомендациями [1].
10.2 Оперативный контроль погрешности (точности) результатов определений осуществляют методом добавок витаминов.
Периодичность контроля погрешности (точности) устанавливает сама лаборатория с учетом фактического состояния работ. При смене партий реактивов, экземпляров средств измерений и стандартов проведение оперативного контроля погрешности обязательно.
10.3 Контроль стабильности результатов определений в лаборатории осуществляют по ГОСТ ИСО 5725-6 и [1], используя методы контроля стабильности стандартного отклонения промежуточной прецизионности и погрешности по ГОСТ ИСО 5725-6 с применением контрольных карт Шухарта.
Периодичность контроля и процедуры контроля стабильности результатов определений регламентируют в руководстве по качеству лаборатории в соответствии с ГОСТ ИСО/МЭК 17025 (пункт 4.2).
При неудовлетворительных результатах контроля, например, при превышении предела действия или регулярном превышении предела предупреждения, выясняют причины этих отклонений, в том числе проводят смену реактивов, проверяют работу оператора.
11.1 Условия безопасного проведения работ
При выполнении определений массовой концентрации (массовой доли) витаминов соблюдают следующие требования.
Требования электробезопасности при работе с приборами - по ГОСТ 12.1.019 и в соответствии с инструкцией по эксплуатации прибора.
При работе с чистыми веществами соблюдают требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.007.
11.2 Требования к квалификации операторов
К выполнению определений, обработке и оформлению результатов допускаются инженеры-химики, лаборанты, имеющие высшее или среднеспециальное образование, опыт работы с данным оборудованием и знакомые с настоящим методом.
Первое применение метода в лаборатории должно проводиться под руководством специалиста, владеющего теорией высокоэффективной жидкостной хроматографии и имеющего практические навыки в этой области.
Построение градуировочной характеристики, приготовление стандартных растворов, проведение внутреннего контроля следует проводить специалисту высшей квалификации, имеющего стаж работы в данной области не менее двух лет.
_______________
*(1) На территории Российской Федерации действует ГОСТ Р 12.1.019-2009 "Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты".
*(2) На территории Российской Федерации действует ГОСТ Р 52501-2005 "Вода для лабораторного анализа. Технические условия".
*(3) На территории Российской Федерации действует ГОСТ Р ИСО 5725-2-2002 "Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений".
*(4) На территории Российской Федерации действует ГОСТ Р ИСО 5725-6-2002 "Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике".
*(5) Колонки Thermo Scientific AQUASIL С18 HPLC, RESTEK Pinnacle DB Aqueous C18 и Agilent Zorbax AAA опробованы и обеспечивают необходимое разделение. Данная информация не является рекламой указанных колонок и приведена для удобства пользователей настоящего стандарта.
*(6) Время подачи дериватизирующего реагента от момента ввода пробы (без учета времени заполнения реагентом реакционного модуля) до максимальной точки выхода хроматографического пика. Данная величина используется для отключения подачи дериватизирующего реагента.
Приложение А
(справочное)
А.1 Структурные формулы (в форме оснований) и некоторые характеристики водорастворимых витаминов приведены в таблице А.1.
Таблица А.1
|
Название |
Молекулярная масса |
Номер CAS |
Структурная и молекулярная формула |
|
Витамин В1 (Тиамин) |
265, 40 |
59-43-8 | 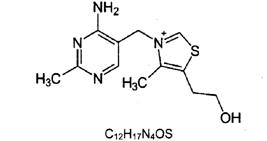
|
|
Витамин В2 (Рибофлавин) |
376, 37 |
83-88-5 | 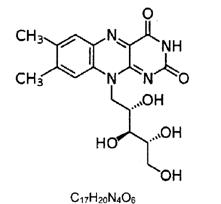
|
|
Витамин В6 (Пиридоксин) |
169, 14 |
58-56-0 | 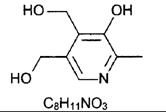
|
|
Витамин РР (Никотинамид) |
122, 13 |
98-92-0 | 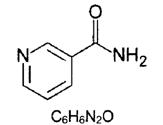 |
Приложение Б
(обязательное)
Б.1 Матричный раствор предназначен для учета мешающего влияния фруктовых кислот и сахаров, присутствующих в пробе, подготовленной по 4.2 или 4.3, на время выхода и светопоглощение витаминов, особенно при их низких концентрациях.
Б.2 Средства измерений, посуда и реактивы
Б.2.1 Средства измерений и посуда
- весы неавтоматического действия по ГОСТ OIML R 76-1, специального (1-го) класса точности с наибольшим пределом взвешивания 150 г и пределом допускаемой абсолютной погрешности ±0, 0005 г;
- колба мерная 2-100-2 по ГОСТ 1770;
- стаканы В-1-100 по ГОСТ 25336.
Б.2.2 Реактивы
- L(-)-яблочная кислота C4H6O5;
- кислота лимонная (моногидрат) по ГОСТ 3652;
- сахароза по ГОСТ 5833;
- D (+)-глюкоза по ГОСТ 6038;
- D (-)-фруктоза;
- сорбит C6H14O6;
- вода для лабораторного анализа по ГОСТ ISO 3696 не ниже второй степени чистоты.
Все используемые реактивы относят к подгруппе чистоты не ниже 3, квалификации ч.д.а. по ГОСТ 13867.
Допускается применение других средств измерений, не уступающих вышеуказанным по метрологическим и техническим характеристикам, а также реактивов и посуды по качеству не хуже вышеуказанных.
Б.3 Приготовление раствора
Б.3.1 Приготовление компонентов матричного раствора для определения витаминов приведено в таблице Б.1.
Таблица Б.1
|
N
п/п
|
Компонент |
Объем мерной колбы, см3 |
Масса компонента по А.2, необходимая для приготовления раствора, г |
Массовая концентрация в полученном растворе, г/дм3 |
|
1 |
Яблочная кислота |
100 |
(0, 700±0, 001) |
7, 0 |
|
2 |
Лимонная кислота |
(0, 020±0, 001) |
0, 2 | |
|
3 |
Сахароза |
(1, 500±0, 001) |
15, 0 | |
|
4 |
Глюкоза |
(2, 000±0, 001) |
20, 0 | |
|
5 |
Фруктоза |
(6, 000±0, 001) |
60, 0 | |
|
6 |
Сорбит |
(0, 450±0, 001) |
4, 5 |
Б.3.2 Результаты взвешивания записывают с точностью до четвертого десятичного знака. Доводят объем раствора до метки водой и перемешивают.
Б.3.3 Раствор готовят при температуре окружающей среды (20±5)°С.
Срок хранения раствора в холодильнике при температуре не более 4°С - в течение одной недели.
Приложение В
(справочное)
В.1 Примеры типовых хроматограмм и УФ-спектры поглощения витаминов в обогащенной соковой продукции приведены на рисунках В.1 - В.7.
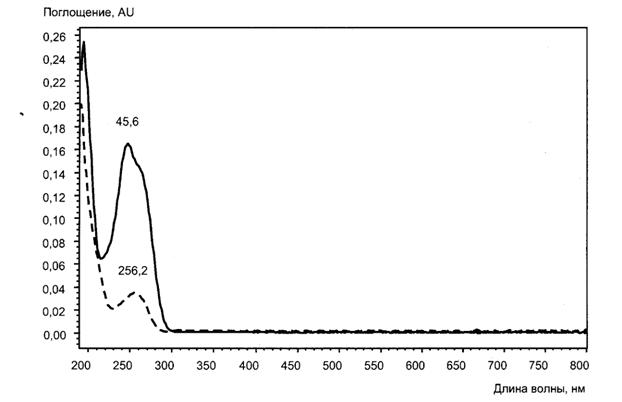
"Рисунок В.1 - УФ-спектр витамина В1, сдвиг максимума абсорбции за счет матричного влияния"
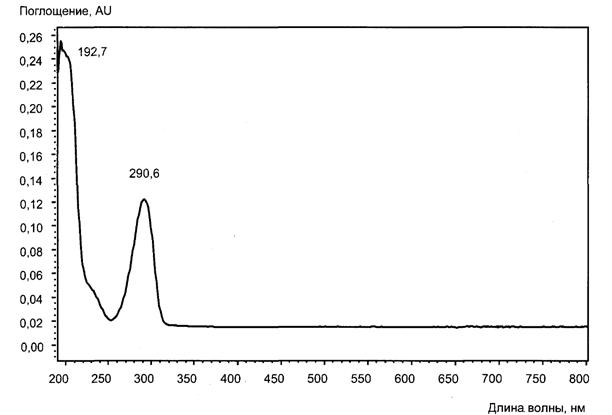
"Рисунок В.2 - УФ-спектр витамина В6"
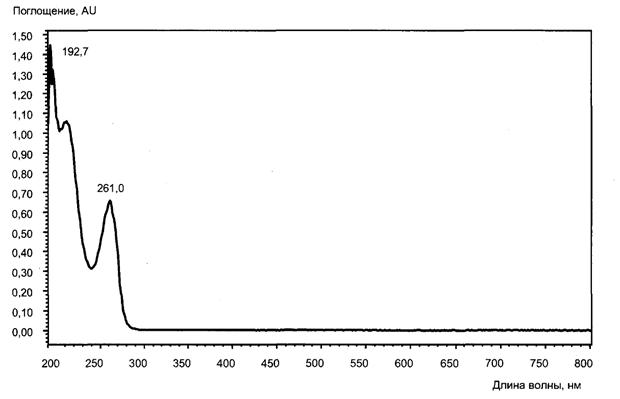
"Рисунок В.3 - УФ-спектр витамина РР"
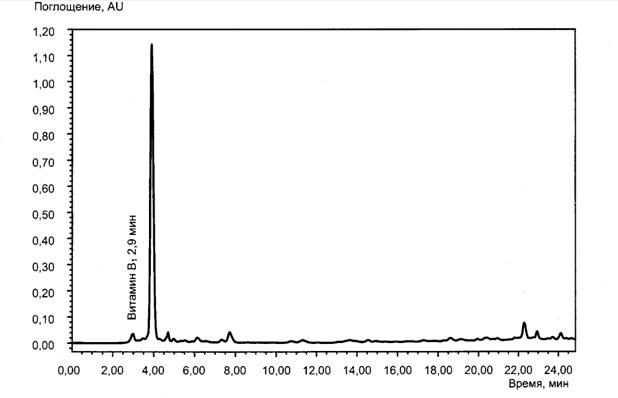
"Рисунок В.4 - Хроматограмма нектара из яблок, черноплодной рябины и черной смородины, обогащенного витаминами и минеральными веществами с выделенным хроматографическим пиком витамина В1"
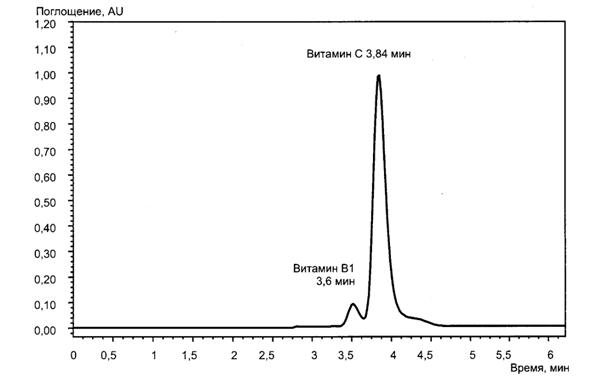
"Рисунок В.5 - Фрагмент хроматограммы витаминного премикса с хроматографическими пиками витамина В1 и витамина С, оказывающего мешающее влияние на определение витамина В1 в случае спектрофотометрического детектирования"
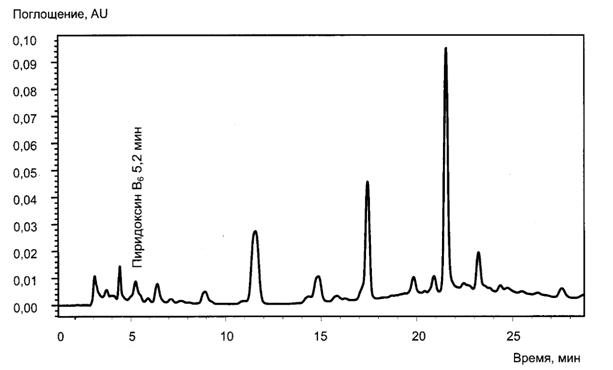
"Рисунок В.6 - Хроматограмма нектара из яблок, черноплодной рябины и малины, обогащенного витаминами и минеральными веществами с хроматографическим пиком витамина В6"
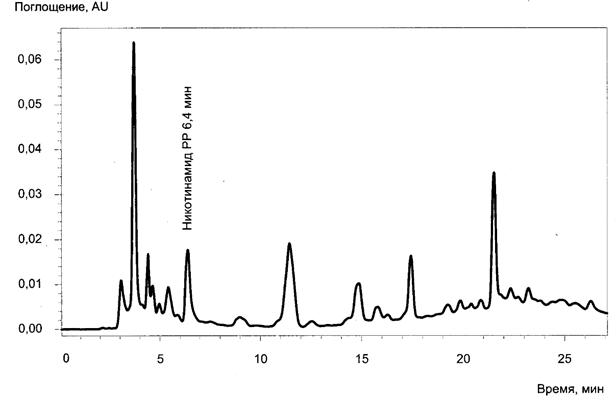
"Рисунок В.7 - Хроматограмма нектара из яблок, черноплодной рябины и черной смородины, обогащенного витаминами и минеральными веществами с хроматографическим пиком витамина РР"
Приложение Г
(обязательное)
Проверку оптимальности выбранных хроматографических условий (характеристик колонки) проводят по основным характеристикам, приведенным в таблицах Г.1 - Г.3 с применением рабочего градуировочного раствора N 4.
|
Витамин |
Время удерживания tR, мин |
Число теоретических тарелок N |
Коэффициент емкости k' |
Разрешение Rs |
|
Тиамин (В1) |
3, 6±0, 2 |
5184 |
0, 24 |
0, 36* |
|
Пиридоксин (В6) |
5, 7±0, 3 |
472 |
0, 97 |
1, 95 |
|
Никотинамид (РР) |
7, 0±0, 4 |
544 |
1, 41 |
1, 16 |
|
Примечание - Разрешение хроматографического пика для витамина В1 дано по отношению к витамину С (см. рисунок В.5), который определяют по ГОСТ 31643. Для остальных витаминов - разрешение дано по ближайшему пику. | ||||
|
Компонент |
Время удерживания tR, мин |
Число теоретических тарелок N |
Коэффициент асимметрии, As |
|
Тиамин (В1) |
5, 05±0, 25 |
7226 |
1, 1 |
|
Компонент |
Время удерживания tR, мин |
Число теоретических тарелок N |
Коэффициент асимметрии As |
|
Пиридоксин (В6) |
5, 00±0, 25 |
6471 |
0, 99 |
|
Рибофлавин (В2) |
24, 0±1, 2 |
113771 |
0, 72 |
Время удерживания соответствующего компонента определяют непосредственно из хроматограмм двух параллельных измерений.
В случае обнаружения отклонения времени удерживания более чем на 5% для любого из витаминов строят новую градуировочную зависимость во всем диапазоне измерений.
Число теоретических тарелок вычисляют по формуле
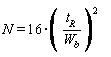 ,
,(Г.1)
где tR - время удерживания пика витамина В1, мин;
Wb - ширина пика витамина В1 у основания, мин.
Колонка считается удовлетворительной при значении числа теоретических тарелок не ниже 10% от указанного в таблице.
Разрешение между двумя хроматографическими пиками RS вычисляют по формуле
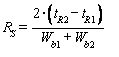 ,
,(Г.2)
где tR2 - время удерживания витамина С, мин;
tR1 - время удерживания витамина В1, мин;
Wb1, Wb2 - ширина пика витамина С и витамина В1 у основания, мм.
Колонка считается удовлетворительной при значениях Rs≥0, 34.
Коэффициент емкости вычисляют по формуле
(Г.3)
где t'R - приведенное время удерживания витамина В1, мин;
tM - мертвое время удерживания витамина В1, мин.
Колонка считается удовлетворительной при значении коэффициента емкости, не превышающем 10% от указанного в таблице.
При невозможности достижения требуемых условий эффективности хроматографического разделения проводят определения других хроматографических колонок аналогичным образом.
Контроль эффективности хроматографического разделения проводят не реже одного раза в месяц.
Приложение Д
(рекомендуемое)
Д.1 Общая схема кондиционирования системы перед выводом на рабочий режим сводится к следующему*:
- насос системы промывают рабочим элюентом (если система была под другим элюентом, насос перемывают в соответствии с совместимостью растворителей);
- на колонку подают раствор дигидрофосфата калия, приготовленный по 6.3.4, со скоростью 0, 10 см3/мин до установления постоянного давления;
- скорость потока постепенно увеличивают с шагом 0, 1 см3/мин, с установлением постоянного давления после каждого прибавления до 1, 0 см3/мин;
- перед первым измерением с помощью программного обеспечения, в соответствии с руководством пользователя выполняют операции в соответствии с таблицей Д.1.
|
N пп |
Выполняемая операция |
Время, мин |
|
1 |
Промывка инжектора |
6, 5 |
|
2 |
Ввод образца с нулевым объемом или "холостая инжекция"* |
15, 0 |
|
3 |
Уравновешивание колонки |
5, 0 |
|
* В зависимости от конструктивных особенностей хроматографической системы выполняют ввод образца с нулевым объемом (программная функция) или "холостое инжектирование" - ввод 20 мм подвижной фазы по 6.3.4. | ||
Выполнение данной операции осуществляют с использованием условий, указанных в таблице Д.2.
|
Время, мин |
Скорость потока подачи элюента, см3/мин |
Состав подвижной фазы (элюента), массовая доля, % | |
|
Раствор дигидрофосфата калия |
Ацетонитрил | ||
|
0 |
1 |
96, 0 |
4, 0 |
|
2 |
80, 0 |
20, 0 | |
|
7 |
80, 0 |
20, 0 | |
|
9 |
96, 0 |
4, 0 | |
|
15 |
96, 0 |
4, 0 | |
Д.2 Выключение хроматографической системы проводят в соответствии с руководством по эксплуатации, при этом:
- скорость потока подвижной фазы снижают до 0, 1 см3/мин и затем подачу останавливают;
- насос промывают водой;
- колонку отмывают водой при скорости (0, 5 - 1, 0) см3/мин в течение 30 мин и выключают прибор
_______________
* Данную операцию выполняют с целью уравновешивания сорбента колонки.
Библиография
|
[1] |
РМГ 76-2004 |
Внутренний контроль качества результатов количественного химического анализа |
(Нет голосов) |
-
29.05.2025
Слухи о скорой заморозке вкладов в России объяснили
 Банкир Хотимский объяснил слухи о заморозке вкладов в России идеей застройщиков
Банкир Хотимский объяснил слухи о заморозке вкладов в России идеей застройщиков
-
29.05.2025
Дачникам рассказали о штрафах за нескошенную траву
 Эксперт по ЖКХ Бондарь: За нескошенную траву дачникам грозит штраф до 50 тысяч
Эксперт по ЖКХ Бондарь: За нескошенную траву дачникам грозит штраф до 50 тысяч
-
29.05.2025
Вероятность исчезновения в России наличных денег оценили
 Экс-глава ЦБ Дубинин: В России никогда не откажутся от наличных рублей
Экс-глава ЦБ Дубинин: В России никогда не откажутся от наличных рублей
-
29.05.2025
Перспективы исламского банкинга в России оценили
 Комитет ГД поддержал продление на три года эксперимента по исламскому банкингу
Комитет ГД поддержал продление на три года эксперимента по исламскому банкингу
-
30.04.2025
Россиянам объяснили опасность зарплаты в конвертах
 Депутат Бессараб: Россияне с зарплатой в конвертах могут остаться без пенсии
Депутат Бессараб: Россияне с зарплатой в конвертах могут остаться без пенсии