Утв. Постановлением Государственного комитета СССР по стандартам от 23 мая 1983 г. N 2302
Государственный стандарт Союза ССР ГОСТ 25794.3-83
"РЕАКТИВЫ. МЕТОДЫ ПРИГОТОВЛЕНИЯ ТИТРОВАННЫХ РАСТВОРОВ ДЛЯ ТИТРОВАНИЯ ОСАЖДЕНИЕМ, НЕВОДНОГО ТИТРОВАНИЯ И ДРУГИХ МЕТОДОВ"
Reagents. Methods of preparation of standard volumetric solutions for precipitation titration, non-aqueous titration and other titrimetric methods
Срок действия с 1 июля 1984 г.
до 1 июля 2001 г.
Ограничение срока действия в 1995 г.
Введен впервые
Настоящий стандарт распространяется на реактивы и устанавливает методы приготовления следующих титрованных растворов для титрования осаждением, неводного титрования и других методов и методы проверки их молярной концентрации:
аммоний роданистый, раствор молярной концентрации
с (NH4SCN)=0, 1 моль/дм3 (0, 1 н.) или
калий роданистый, раствор молярной концентрации
с (KSCN)=0, 1 моль/дм3 (0, 1 н.);
серебро азотнокислое, раствор молярной концентрации
с (AgNO3)=0, 1 моль/дм3 (0, 1 н.) и с (AgNO3)=0, 05 моль/дм3 (0, 05 н.);
кислота хлорная, уксуснокислый раствор молярной концентрации
с (HClO4)=0, 1 моль/дм3 (0, 1 н.);
калия гидроокись, спиртовой раствор молярной концентрации
с (KON)=0, 5 моль/дм3 (0, 5 н.);
калия метилат, раствор молярной концентрации
с (CH3OK)=0, 1 моль/дм3 (0, 1 н.);
ртуть (I) азотнокислая, растворы молярных концентраций:
с (1/2Hg2(NO3)2·2H2O)=0, 1 моль/дм3 (0, 1 н.);
с (1/2Hg2(NO3)2·2H2O)=0, 05 моль/дм3 (0, 05 н.);
ртуть (II) азотнокислая, раствор молярной концентрации
с (1/2Hg(NO3)2·H2O)=0, 1 моль/дм3 (0, 1 н.);
натрий азотнокислый, растворы молярных концентраций:
с (NaNO2)=0, 5 моль/дм3 (0, 5 н.),
с (NaNO2)=0, 1 моль/дм3 (0, 1 н.).
1. Общие указания
1.1. Общие указания - по ГОСТ 25794.1-83.
2. Методы приготовления титрованных растворов
2.1. Аммоний роданистый, раствор молярной концентрации:
с (NH4SCN)=0, 1 моль/дм3 (0, 1 н.) или
калий роданистый, раствор молярной концентрации
с (KSCN)=0, 1 моль/дм3 (0, 1 н.).
Формула NH4SCN.
Относительная молекулярная масса - 76, 12.
Молярная масса эквивалента - 76, 12 г/моль.
Формула KSCN.
Относительная молекулярная масса - 97, 18.
Молярная масса эквивалента - 97, 18 г/моль.
2.1.1. Реактивы и растворы
Аммоний роданистый по ГОСТ 27067-86.
Калий роданистый по ГОСТ 4139-75, выдержанный при 150°С до постоянной массы.
Аммоний железо (III) сульфат (1:1:2) 12-водный (железо-аммонийные квасцы по ТУ 6-09-5359-88), насыщенный раствор.
Кислота азотная по ГОСТ 4461-77, раствор с массовой долей 25%, не содержащий окислов азота.
Серебро азотнокислое по ГОСТ 1277-75, раствор молярной концентрации с (AgNO3)=0, 1 моль/дм3 (0, 1 н.), приготовленный по настоящему стандарту (п. 2.2).
2.1.2. Приготовление раствора
7, 60-8, 00 г роданистого аммония растворяют в воде и доводят объем водой до 1 дм3. Раствор хранят в склянке из темного стекла.
2.1.3. Определение коэффициента поправки
30-40 см3 раствора азотнокислого серебра, отмеренного бюреткой, помещают в коническую колбу, прибавляют 10 см3 раствора азотной кислоты, 1 см3 раствора железоаммонийных квасцов и титруют из другой бюретки раствором роданистого аммония, приливая его медленно, небольшими порциями, при постоянном взбалтывании до появления неисчезающей коричневато-красной окраски жидкости над осадком.
2.1.4. Приготовление раствора точной молярной концентрации
9, 7176 г роданистого калия растворяют в воде в мерной колбе вместимостью 1 дм3 и доводят объем раствора водой до метки.
2.2. Серебро азотнокислое, раствор молярной концентрации с (AgNO3)=0, 1 моль/дм3 (0, 1 н.) и с (AgNO3)=0, 05 моль/дм3 (0, 05 н.)
Формула AgNO3.
Относительная молекулярная масса - 169, 87.
Молярная масса эквивалента - 169, 87 г/моль.
2.2.1. Аппаратура, реактивы, растворы
Иономер универсальный ЭВ-74.
Электрод серебряный и хлорсеребряный, или насыщенный каломельный, или стеклянный.
Ключ электролитический (мостик), заполненный насыщенным раствором азотнокислого калия.
Калий азотнокислый по ГОСТ 4217-77, насыщенный раствор.
Спирт этиловый ректификованный технический по ГОСТ 18300-87.
Серебро азотнокислое по ГОСТ 1277-75.
Калий хлористый по ГОСТ 4234-77 или натрий хлористый по ГОСТ 4233-77, предварительно прокаленные до постоянной массы в муфельной печи при 500 - 600°С или стандартный образец натрия хлористого для титрования ГСО I разряда N° 4391-88 или ГСО II разряда.
Кислота серная по ГОСТ 4204-77, раствор с массовой долей 10%.
Флуоресцеин по ТУ 6-09-2281-82, раствор в этиловом спирте с массовой долей 0, 1%.
Калий хромовокислый по ГОСТ 4459-75, насыщенный раствор.
2.2.2. Приготовление раствора
17, 00 г азотнокислого серебра для раствора концентрации 0, 1 моль/дм3 и 8, 50 г для раствора концентрации 0, 05 моль/дм3 растворяют в 1 дм3 воды. Раствор хранят в склянке из темного стекла длительное время.
2.1-2.2.2. (Измененная редакция, Изм. N 1).
2.2.3. Определение коэффициента поправки
2.2.3.1. Визуальное определение
|
Формула KCl
|
Формула NaCl
|
|
Относительная молекулярная масса - 74, 55.
|
Относительная молекулярная масса - 58, 44.
|
|
Молярная масса эквивалента - 74, 55 г/моль.
|
Молярная масса эквивалента - 58, 44 г/моль.
|
Около 0, 2000 г хлористого калия или хлористого натрия для раствора концентрации 0, 1 моль/дм3 и около 0, 1000 г хлористого калия или хлористого натрия для раствора концентрации 0, 05 моль/дм3 помещают в коническую колбу, растворяют в 50 см3 воды, прибавляют 8 - 10 капель раствора флуоресцеина и титруют в защищенном от света месте раствором азотнокислого серебра до окрашивания осадка в розовый цвет.
Допускается определять коэффициент поправки в присутствии хромовокислого калия в качестве индикатора с изменением желтой окраски раствора в точке эквивалентности на красно-коричневую.
2.2.3.2. Потенциометрическое определение
Около 0, 1300 г хлористого натрия, для раствора концентрации 0, 1 моль/дм3 и около 0, 1000 г хлористого натрия для раствора концентрации 0, 05 моль/дм3 помещают в стакан вместимостью 150 см3, растворяют в 50 см3 воды, добавляют 5 см3 раствора серной кислоты и титруют приготовленным раствором азотнокислого серебра потенциометрически в соответствии с инструкцией универсальному иономеру.
Вблизи точки экивалентности в раствор азотнокислого серебра добавляют порциями по 0, 1 см3, отмечая потенциал раствора (Е, мВ).
Точный объем раствора азотнокислого серебра, израсходованного на титрование (V) в кубических сантиметрах вычисляют по формуле
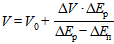 ,
,
где V0 - объем раствора азотнокислого серебра, израсходованный на титрование при последней положительной разности величин ΔЕ, см3;
ΔЕр - последнее положительное значение разности величин ΔЕ, мВ;
ΔЕп - первое отрицательное значение разности величин ΔЕ, мВ;
ΔV - объем добавляемой порции раствора азотнокислого серебра, см3.
Коэффициент поправки вычисляют по ГОСТ 25794.1-83, п. 1.8.1.
Пример расчета точного объема азотнокислого серебра, израсходованного на титрование, и коэффициента поправки приведен в приложении.
2.3. Кислота хлорная, уксуснокислый раствор молярной концентрации с (HClO4)=0, 1 моль/дм3 (0, 1 н.)
Формула HClO4.
Относительная молекулярная масса - 100, 46.
Молярная масса эквивалента - 100, 46 г/моль.
2.3.1. Аппаратура, реактивы и растворы
Иономер универсальный ЭВ-74.
Бюретка 1 (7)-2-10 по ГОСТ 20292-74.
Электроды стеклянный и хлорсеребряный (или насыщенный каломельный).
Ангидрид уксусный по ГОСТ 5815-77 с предварительно определенной плотностью.
Анилин по ГОСТ 5819-78, свежеперегнанный, раствор в уксусной кислоте с массовой долей 5%, годен для применения в течение 15 - 20 сут при хранении в склянке из темного стекла с пришлифованной пробкой.
Кислота уксусная ледяная по ГОСТ 61-75, проверенная на соответствие массовой доли основного вещества норме (99, 8±0, 3) %.
Кислота хлорная по ТУ 6-09-2878-84, раствор с массовой долей 70 или 30%; предварительно определяют массовую долю основного вещества или плотность раствора хлорной кислоты. Для определения массовой доли основного вещества 2 г раствора хлорной кислоты с массовой долей 70% или 5 г раствора хлорной кислоты с массовой долей 30% титруют раствором гидроокиси натрия в присутствии раствора метилового оранжевого и по таблицам находят соответствующую плотность, либо плотность определяют ареометром с погрешностью не более 0, 001 г/см3 и по таблицам находят соответствующую массовую долю кислоты.
Калий гидрофталат (калий фталевокислый кислый по ТУ 6-09-09-304-87), выдержанный при 120°С в течение 2 ч и проверенный на содержание основного вещества.
Кристаллический фиолетовый (индикатор) по ТУ 6-09-07-1388-84, раствор в уксусной кислоте с массовой долей 0, 5%.
Метиловый оранжевый (индикатор) по ТУ 6-09-5171-84, раствор с массовой долей 0, 1%.
Метиловый фиолетовый (индикатор) по ТУ 6-09-945-86, раствор в уксусной кислоте с массовой долей 0, 2%.
Натрия гидроокись по ГОСТ 4328-77, раствор концентрации с (NaOH)=0, 5 моль/дм3 (0, 5 н.).
Натрий углекислый по ГОСТ 83-79, предварительно прокаленный при 270 - 300°С до постоянной массы, с массовой долей основного вещества (100, 0±0, 2) %. Условия и контроль полноты прокаливания, а также определение массовой доли основного вещества - по ГОСТ 25794.1-83.
2.2.3.1 - 2.3.1. (Измененная редакция, Изм. N 1).
2.3.2. Приготовление раствора
2.3.2.1. Объем раствора хлорной кислоты, необходимый для приготовления 1 дм3 уксуснокислого раствора хлорной кислоты концентрации с (HClO4)=0, 1 моль/дм3, (V) в кубических сантиметрах вычисляют по формуле
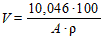 , (1)
, (1)
где А - массовая доля хлорной кислоты в применяемом растворе, %;
ρ - плотность применяемого раствора хлорной кислоты, г/см3;
10, 046 - 0, 1 молярной массы эквивалента хлорной кислоты.
В связи с тем, что применяемый раствор хлорной кислоты содержит воду и при введении его в ледяную уксусную кислоту попадает некоторое количество воды, мешающее в дальнейшем титрованию, это количество воды следует связать уксусным ангидридом.
2.3.2.2. Необходимый для этого объем уксусного ангидрида (V1) в кубических сантиметрах вычисляют по формуле
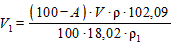 , (2)
, (2)
где (100-А) - массовая доля воды в применяемом растворе хлорной кислоты, %;
А - массовая доля хлорной кислоты в применяемом растворе, %;
V - объем применяемого раствора хлорной кислоты, рассчитанный для приготовления титрованного раствора, см3;
ρ - плотность применяемого раствора хлорной кислоты, г/см3;
ρ1 - плотность уксусного ангидрида, г/см3;
102, 09 - относительная молекулярная масса уксусного ангидрида;
18, 02 - относительная молекулярная масса воды.
2.3.2.3. Для приготовления уксуснокислого раствора хлорной кислоты рассчитанный объем применяемого раствора исходной хлорной кислоты (V см3) медленно, при перемешивании, вливают из бюретки в мерную колбу вместимостью 1 дм3 с ледяной уксусной кислотой, прибавляют из бюретки рассчитанный объем уксусного ангидрида (V1 см3), перемешивают, доводят объем раствора уксусной кислотой до метки и снова перемешивают. Раствор годен для применения 24 ч.
2.3.2.1 - 2.3.2.3. (Измененная редакция, Изм. N 1).
2.3.3. При титровании легкоацетилирующихся первичных и вторичных аминов не должно быть избытка уксусного ангидрида в уксуснокислом растворе хлорной кислоты. Массовая доля уксусного ангидрида в уксусной кислоте не должна превышать 0, 001% (п. 2.3.4). В противном случае для связывания воды должен быть добавлен соответственно меньший объем уксусного ангидрида.
2.3.4. Определение примеси уксусного ангидрида в уксусной кислоте
50 см3 уксусной кислоты отмеривают цилиндром в сухую коническую колбу вместимостью 100 см3 (с пришлифованной пробкой), добавляют пипеткой 10 см3 раствора анилина, закрывают колбу пробкой, раствор перемешивают и выдерживают в течение 10 мин. Затем добавляют 1 каплю раствора кристаллического фиолетового и титруют из бюретки уксуснокислым раствором хлорной кислоты до перехода окраски раствора в зеленую.
Если при обратном титровании изменение окраски раствора наступает от нескольких капель уксуснокислого раствора хлорной кислоты (что указывает на значительное содержание ангидрида в анализируемой кислоте), следует ввести дополнительное количество анилина и снова выдержать в течение 10 мин.
Одновременно таким же образом титруют введенный объем раствора анилина.
Массовую долю уксусного ангидрида (X) в процентах вычисляют по формуле
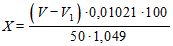 , (3)
, (3)
где V - объем уксуснокислого раствора хлорной кислоты молярной концентрации точно 0, 1 моль/дм3, израсходованный на титрование раствора анилина, см3;
V1 - объем уксуснокислого раствора хлорной кислоты молярной концентрации точно 0, 1 моль/дм3, израсходованный на обратное титрование, см3;
0, 01021 - масса уксусного ангидрида, соответствующая 1 см3 уксуснокислого раствора хлорной кислоты молярной концентрации точно 0, 1 моль/дм3, г;
1, 049 - плотность уксусной кислоты, г/см3.
2.3.5. Определение коэффициента поправки
Формула Na2CO3.
Относительная молекулярная масса - 105, 99.
Молярная масса эквивалента - 52, 95 г/моль.
0, 0800 - 0, 1000 г углекислого натрия помещают в сухую коническую колбу с пришлифованной пробкой, прибавляют 25 см3 уксусной кислоты, перемешивают до растворения, добавляют 1 каплю раствора кристаллического фиолетового или метилового фиолетового и титруют уксуснокислым раствором хлорной кислоты визуально до перехода окраски раствора в зеленую (цвет раствора при титровании меняется от фиолетового к синему, от синего к зеленому, концом титрования считают переход от сине-зеленого к чисто-зеленому); или потенциометрически со стеклянным и хлор-серебряным (или насыщенным каломельным) электродами.
При этом стеклянный электрод перед определением выдерживают в ледяной уксусной кислоте в течение 1 сут.
Допускается проводить определение коэффициента поправки по калию фталевокислому кислому (масса навески для титрования около 0, 5000 г).
Если коэффициент поправки устанавливают и раствор применяют при различных температурах, то вводят температурную поправку. Для этого объем раствора хлорной кислоты, израсходованный на титрование анализируемого раствора, в кубических сантиметрах, умножают на 1-(Δt·0, 001), если титруют при более высокой температуре, или на 1+(Δt-0, 001), если титруют при более низкой температуре, чем та, при которой устанавливают коэффициент поправки (Δt - разность температур в градусах Цельсия).
При необходимости проведения контроля массовой доли воды в уксуснокислом растворе хлорной кислоты используют метод с применением реактива Фишера по ГОСТ 14870-77.
Титрование следует проводить в условиях, исключающих попадание влаги.
2.4. Калия гидроокись, спиртовой раствор молярной концентрации с (KOH)=0, 5 моль/дм3 (0, 5 н.)
Формула KOH.
Относительная молекулярная масса - 56, 11.
Молярная масса эквивалента - 56, 11 г/моль.
2.4.1. Реактивы и растворы
Калия гидроокись по ГОСТ 24363-80.
Кислота серная по ГОСТ 4204-77, раствор молярной концентрации с (1/2H2SO4)=0, 5 моль/дм3 (0, 5 н.) или
кислота соляная по ГОСТ 3118-77, раствор молярной концентрации с (HCl)=0, 5 моль/дм3 (0, 5 н.); растворы готовят и устанавливают коэффициент поправки по ГОСТ 25794.1-83.
Спирт этиловый ректификованный технический по ГОСТ 18300-87, высший сорт или 1-пропанол по ТУ 6-09-783-76.
Фенолфталеин (индикатор) по ТУ 6-09-5360-88, спиртовой раствор с массовой долей 1%.
2.4.2. Приготовление раствора
30 г гидроокиси калия растворяют в широкогорлой колбе в 1 дм3 спирта. После отстаивания в колбе, закрытой пробкой, в течение 24 ч раствор быстро декантируют в склянку из темного стекла и сразу закрывают резиновой пробкой, обернутой тонкой фторопластовой или полиэтиленовой пленкой.
Раствор неустойчив при хранении.
Коэффициент поправки устанавливают в день применения. Допускается готовить раствор гидроокиси калия в 1-пропаноле.
2.4.3. 30 - 40 см3 раствора серной или соляной кислоты отмеряют бюреткой в коническую колбу, добавляют 2 - 3 капли раствора фенолфталеина и титруют из другой бюретки раствором гидроокиси калия до появления розовой окраски раствора.
2.5. Калия метилат, раствор молярной концентрации с (CH3OK)=0, 1 моль/дм3 (0, 1 н.)
Формула CH3OK.
Относительная молекулярная масса - 70, 13.
Молярная масса эквивалента - 70, 13 г/моль.
2.5.1. Реактивы и растворы
Азот газообразный по ГОСТ 9293-74.
Кислота бензойная по ГОСТ 10521-78.
Бензол по ГОСТ 5955-75 предварительно обезвоженный следующим образом: бензол кипятят в перегонном аппарате с дефлегматором до тех пор, пока перегонится около 25% объема. Остаток охлаждают в аппарате. Колбу с остатком отделяют от аппарата и предохраняют от попадания в нее влаги при хранении.
Диметилформамид по ГОСТ 20289-74, предварительно обезвоженный по ГОСТ 14870-77.
Калий металлический по ГОСТ 10588-75 или натрий металлический по ГОСТ 3273-75.
Метанол-яд по ГОСТ 6995-77, предварительно обезвоженный по ГОСТ 14870-77.
Тимоловый синий (индикатор) по ТУ 6-09-3501-78, раствор в безводном метиловом спирте с массовой долей 0, 3%.
2.5.2. Приготовление раствора
В мерной колбе вместимостью 1 дм3 осторожно в атмосфере азота в охлажденной смеси 20 см3 метанола и 50 см3 безводного бензола растворяют очень малыми дозами 4, 00 г металлического калия (после тщательного удаления поверхностного слоя и ополаскивания безводным бензолом).
После растворения калия добавляют столько безводного метанола, чтобы раствор стал прозрачным и исчезла вторая фаза. Затем добавляют безводный бензол до помутнения раствора, затем снова метанол до осветления раствора. Этот процесс повторяют до получения 1 дм3 прозрачного раствора.
Приготовленный раствор предохраняют от действия света, влаги, углекислоты. Коэффициент поправки устанавливают в день применения. Необходимо соблюдать меры предосторожности при работе с огнеопасными растворителями.
2.5.3. Определение коэффициента поправки
Формула C7H6O2.
Относительная молекулярная масса - 122, 12.
Молярная масса эквивалента - 122, 12 г/моль.
0, 1000 - 0, 1100 г бензойной кислоты помещают в коническую колбу вместимостью 100 см3 растворяют в 20 см3 диметилформамида, добавляют 2 капли раствора тимолового синего и титруют приготовленным раствором метилата калия в атмосфере азота до синего окрашивания, при этом шлифы бюретки смазывают бензолостойкой смазкой.
В результат определения, при необходимости, вносят поправку, устанавливаемую контрольным опытом.
2.5.4. Допускается применять раствор метилата натрия, который готовят аналогичным образом из навески 2, 20 - 2, 50 г металлического натрия.
2.6. Ртуть (I) азотнокислая, растворы молярных концентраций:
с (1/2Hg2(NO3)2·2H2O)=0, 1 моль/дм3 (0, 1 н.),
с (1/2Hg2(NO3)2·2H2O)=0, 05 моль/дм3 (0, 05 н.).
Формула Hg2(NO3)2·2H2O.
Относительная молекулярная масса - 561, 22.
Молярная масса эквивалента - 280, 61 г/моль.
2.6.1. Реактивы и растворы
Дифенилкарбазон или дифенилкарбазид по ТУ 6-09-07-1672-88, раствор в этиловом спирте с массовой долей 1%.
Калий хлористый по ГОСТ 4234-77 или натрий хлористый по ГОСТ 4233-77, предварительно прокаленный до постоянной массы при 500 - 600°С, или стандартный образец натрия хлористого для титриметрии ГСО I разряда N 4391-88 или ГСО II разряда.
Кислота азотная по ГОСТ 4461-77, раствор с массовой долей 25%, готовят по ГОСТ 4517-87.
Ртуть (I) азотнокислая 2-водная по ГОСТ 4521-78.
Ртуть по ГОСТ 4658-73.
Спирт этиловый ректификованный технический по ГОСТ 18300-87, высший сорт.
2.3.4 - 2.6.1. (Измененная редакция, Изм. N 1).
2.6.2. Приготовление растворов
К 1 дм3 воды, содержащему 40 см3 раствора азотной кислоты для раствора концентрации 0, 1 моль/дм3 и 20 см3 для раствора концентрации 0, 05 моль/дм3, добавляют азотнокислую ртуть (I) в количестве 28, 10 г для раствора концентрации 0, 1 моль/дм3 и 14, 05 г для раствора концентрации 0, 05 моль/дм3. После растворения добавляют 1 - 2 капли металлической ртути. Раствор годен к употреблению через 2 сут. Раствор хранят в склянке из темного стекла длительное время.
2.6.3. Определение коэффициента поправки
|
Формула KCl.
|
Формула NaCl.
|
|
Относительная молекулярная масса - 74, 55.
|
Относительная молекулярная масса - 58, 44.
|
|
Молярная масса эквивалента - 74, 55 г/моль.
|
Молярная масса эквивалента - 58, 44 г/моль.
|
0, 2000 - 0, 2500 г хлористого калия или хлористого натрия для раствора концентрации 0, 1 моль/дм3 и 0, 1000 - 0, 1200 г для раствора концентрации 0, 05 моль/дм3 растворяют в 50 см3 воды, прибавляют 5 см3 раствора азотной кислоты и титруют раствором азотнокислой ртути (1), добавляя его в объеме, меньшем теоретически вычисленного на 0, 5 - 1, 0 см3, затем добавляют 0, 2 см3 раствора дифенилкарбазона или дифенилкарбазида и продолжают титрование при тщательном перемешивании до перехода окраски от голубоватой к сине-фиолетовой.
2.7. Ртуть (II) азотнокислая, раствор молярной концентрации
с (1/2Hg(NO3)2·H2O)=0, 1 моль/дм3 (0, 1 н.)
Формула Hg2(NO3)·H2O.
Относительная молекулярная масса - 342, 52.
Молярная масса эквивалента - 171, 26 г/моль.
2.7.1. Реактивы и растворы
Аммоний железо (III) сульфат (1:1:2) 12-водный (квасцы железоаммонийные по ТУ 6-09-5359-88), насыщенный раствор, к которому добавлена концентрированная азотная кислота по каплям до исчезновения бурой окраски раствора.
Калий роданистый по ГОСТ 4139-75, выдержанный при 150°С до постоянной массы.
Кислота азотная по ГОСТ 4461-77, концентрированная и раствор с массовой долей 25%.
Ртуть (II) азотнокислая, 1-водная по ГОСТ 4520-78.
2.7.2. Приготовление раствора
17, 00 г азотнокислой ртути (II) растворяют в воде, содержащей 30 см3 раствора азотной кислоты, и объем доводят водой до 1 дм3. Раствор годен к употреблению через 2 сут. Раствор хранят в склянке из темного стекла длительное время.
2.7.3. Определение коэффициента поправки
Формула KSCN.
Относительная молекулярная масса - 97, 18.
Молярная масса эквивалента - 97, 18 г/моль.
0, 3000 - 0, 4000 г роданистого калия помещают в коническую колбу, растворяют в 50 см3 воды, прибавляют 5 см3 раствора азотной кислоты, 1 см3 раствора железоаммонийных квасцов и титруют раствором азотнокислой ртути (II) до обесцвечивания раствора.
2.8. Натрий азотистокислый, растворы молярных концентраций:
с (NaNO2)=0, 5 моль/дм3 (0, 5 н.)
с (NaNO2)=0, 1 моль/дм3 (0, 1 н.)
Формула NaNO2.
Относительная молекулярная масса - 69, 00.
Молярная масса эквивалента - 69, 00 г/моль.
2.8.1. Аппаратура, реактивы, растворы
Иономер универсальный ЭВ-74.
Электроды платиновый и хлорсеребряный (или насыщенный каломельный).
Кислота соляная по ГОСТ 3118-77.
Натрий азотистокислый по ГОСТ 4197-74.
Аммиак водный по ГОСТ 3760-79.
Сульфаниламид перекристаллизованный, высушенный при 105°С до постоянной массы.
Бумага йодокрахмальная, готовят по ГОСТ 4517-87.
Бумага "конго", готовят по ГОСТ 4919.1-77.
Кислота сульфаниловая по ГОСТ 5821-78, дважды перекристаллизованная из кипящей воды (растворимость в 100 г воды 0, 8 г при 10°С, 6, 6 г при 100°С). Препарат выдерживают в сушильном шкафу при 120°С в течение 2 ч, затем растирают в ступке в мелкий порошок и снова выдерживают при 140°С до постоянной массы.
2.8.2. Приготовление растворов
34, 50 г азотистокислого натрия для раствора концентрации 0, 5 моль/дм3 или 7, 00 г для раствора 0, 1 моль/дм3 растворяют в воде и доводят объем до 1 дм3.
2.8.3. Определение коэффициента поправки
По сульфаниловой кислоте (визуально).
Формула C6H7NO3S.
Относительная молекулярная масса - 173, 18.
Молярная масса эквивалента - 173, 18 г/моль.
0, 4000 - 0, 5000 г сульфаниловой кислоты для раствора концентрации 0, 1 моль/дм3 или 1, 7000-2, 0000 г для раствора концентрации 0, 5 моль/дм3 помещают в стакан вместимостью 600 см3 и растворяют в 100 см3 воды, прибавляют по каплям раствор аммиака до полного растворения. Затем приливают 300 - 400 см3 воды к раствору концентрации 0, 5 моль/дм3. К раствору концентрации 0, 1 моль/дм3 воды не добавляют. Подкисляют растворы соляной кислотой по бумаге "конго" и прибавляют еще 5 см3 соляной кислоты. Полученный раствор титруют соответствующим раствором азотистокислого натрия при 15 - 20°С при перемешивании стеклянной палочкой. В конце титрования раствор азотистокислого натрия прибавляют медленно по каплям.
Конец реакции определяют по йодокрахмальной бумаге, применяемой в качестве внешнего индикатора, для чего после прибавления раствора азотистокислого натрия наносят тонкой стеклянной палочкой каплю титруемого раствора на полоску йодокрахмальной бумаги.
Если в центре капли сразу же не появится фиолетовое пятно, то прибавляют еще некоторый объем раствора азотистокислого натрия и снова проверяют реакцию с йодокрахмальной бумагой.
Титрование продолжают до тех пор, пока капля, нанесенная на йодокрахмальную бумагу, дает сразу же фиолетовое окрашивание. После этого раствор выдерживают не менее 2 мин и снова проверяют реакцию с йодокрахмальной бумагой. Вторичное появление фиолетового пятна служит признаком конца реакции. В случае отсутствия пятна при вторичной пробе добавляют еще раствор азотистокислого натрия и снова проверяют реакцию с йодокрахмальной бумагой.
В результате определения при необходимости вносят поправку, устанавливаемую контрольным опытом.
По сульфаниламиду (электрометрически)
Формула C6H8N2O2S.
Относительная молекулярная масса - 172, 20.
Молярная масса эквивалента - 172, 20 г/моль.
0, 3000 - 0, 3500 г сульфаниламида помещают в стакан вместимостью 150 см3 и, перемешивая электромагнитной мешалкой, растворяют в 25 см3 раствора соляной кислоты и 25 см3 воды. Раствор охлаждают до комнатной температуры и медленно титруют приготовленным раствором азотистокислого натрия электрометрически.
При добавлении раствора азотистокислого натрия стрелка измерительного прибора отклоняется и вновь возвращается в исходное положение. При приближении к точке эквивалентности амплитуда отклонений уменьшается и в самой точке эквивалентности стрелка займет устойчивое положение.
Последняя капля раствора азотистокислого натрия, вызвавшая значительное отклонение стрелки измерительного прибора, вычитается из общего объема раствора, израсходованного на титрование.
2.6.3 - 2.8.3. (Измененная редакция, Изм. N 1).
Приложение
Рекомендуемое
Пример расчета точного объема раствора азотнокислого серебра молярной концентрации 0, 1 моль/дм3 (0, 1 н.), израсходованного на титрование 0, 0960 г хлористого натрия и коэффициента поправки раствора

Введя в формулу полученные значения, рассчитывают точный объем
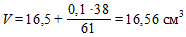 .
.
Коэффициент поправки рассчитывают следующим образом.
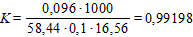 .
.
![]() — Все документы — ГОСТы — ГОСТ 25794.3-83 РЕАКТИВЫ. МЕТОДЫ ПРИГОТОВЛЕНИЯ ТИТРОВАННЫХ РАСТВОРОВ ДЛЯ ТИТРОВАНИЯ ОСАЖДЕНИЕМ, НЕВОДНОГО ТИТРОВАНИЯ И ДРУГИХ МЕТОДОВ
— Все документы — ГОСТы — ГОСТ 25794.3-83 РЕАКТИВЫ. МЕТОДЫ ПРИГОТОВЛЕНИЯ ТИТРОВАННЫХ РАСТВОРОВ ДЛЯ ТИТРОВАНИЯ ОСАЖДЕНИЕМ, НЕВОДНОГО ТИТРОВАНИЯ И ДРУГИХ МЕТОДОВ Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
 Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
 «МК»: в России не отменят льготную ипотеку
«МК»: в России не отменят льготную ипотеку
 Аренда квартир в Москве подешевела на 10 %
Аренда квартир в Москве подешевела на 10 %
 Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
