Утв. Приказом федерального агентства по техническому регулированию и метрологии от 26 ноября 2010 г. N 542-ст
Национальный стандарт РФ ГОСТ Р ЕН 14130-2010
"ПРОДУКТЫ ПИЩЕВЫЕ. ОПРЕДЕЛЕНИЕ ВИТАМИНА С С ПОМОЩЬЮ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ"
Foodstuffs. Determination of vitamin C by HPLC
Дата введения - 1 января 2012 г.
Введен впервые
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. N 184-ФЗ "О техническом регулировании", а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 Подготовлен Государственным научным учреждением Всероссийским научно-исследовательским институтом консервной и овощесушильной промышленности (ГНУ ВНИИКОП) на основе собственного аутентичного перевода на русский язык стандарта, указанного в пункте 4
2 Внесен Техническим комитетом по стандартизации ТК 93 "Продукты переработки фруктов, овощей и грибов"
3 Утвержден и введен в действие приказом Федерального агентства по техническому регулированию и метрологии от 26 ноября 2010 г. N 542-ст
4 Настоящий стандарт идентичен европейскому региональному стандарту ЕН 14130:2003 "Продукты пищевые. Определение витамина С. Метод высокоэффективной жидкостной хроматографии" (EN 14130:2003 "Foodstuffs - Determination of vitamin C by HPLC").
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ Р 1.5 (пункт 3.5).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении ДА
5 Введен впервые
1 Область применения
Настоящий стандарт распространяется на пищевые продукты и устанавливает метод определения витамина С с использованием высокоэффективной жидкостной хроматографии (ВЭЖХ). Содержание витамина С определяется в виде суммарного содержания L(+)-аскорбиновой и L(+)-дегидроаскорбиновой кислот.
2 Нормативные ссылки
В настоящем стандарте использована нормативная ссылка на следующий стандарт:
ЕН ИСО 3696 Вода для лабораторного анализа. Технические требования и методы испытаний (ИСО 3696:1987)
3 Сущность метода
Метод основан на экстракции витамина С из пробы раствором метафосфорной кислоты, последующем восстановлении L(+)-дегидроаскорбиновой кислоты до L(+)-аскорбиновой кислоты и определении общего содержания L(+)-аскорбиновой кислоты методом высокоэффективной жидкостной хроматографии (ВЭЖХ) со спектрофотометрическим детектированием при длине волны 265 нм [1], [2].
4 Реактивы
4.1 Общие положения
При проведении анализа, если не оговорены другие условия, используют только реактивы установленной аналитической чистоты для ВЭЖХ-анализа и воду не ниже первой степени чистоты по ЕН ИСО 3696 или воду, подвергнутую дополнительной дистилляции.
4.2 Реактивы и растворы
4.2.1 Кислота метафосфорная (HPO3)n.
4.2.2 Натрий фосфорнокислый трехзамещенный (тринатрийфосфат) с массовой долей w (Na3PO4·12H2O)≥98, 0%.
4.2.3 Калий фосфорнокислый однозамещенный с массовой долей w (KH2PO4)≥98, 0%.
4.2.4 L-цистеин с массовой долей w (C3H7NO2S)≥99, 0% или другой приемлемый восстанавливающий реактив.
4.2.5 N-цетил-N, N, N-триметиламмонийбромид (цетримид) с массовой долей w (C19H42BrN)≥99, 0%.
4.2.6 Метанол для ВЭЖХ с массовой долей w (CH4O)≥99, 9%.
4.2.7 Раствор метафосфорной кислоты массовой концентрацией ρ ((HPO3)n) = 200 г/дм3
200 г метафосфорной кислоты (см. 4.2.1) растворяют в воде в мерной колбе вместимостью 1 дм3, объем содержимого доводят водой до метки. Срок годности раствора 1 мес при температуре 4°С.
4.2.8 Раствор метафосфорной кислоты массовой концентрацией ρ ((HPO3)n) = 20 г/дм3
50 см3 метафосфорной кислоты (см. 4.2.7) переносят пипеткой в мерную колбу вместимостью 500 см3, объем содержимого доводят водой до метки. Раствор готовят в день проведения анализа.
4.2.9 Раствор натрия фосфорнокислого трехзамещенного массовой концентрацией ρ (Na3PO4·12H2O) = 200 г/дм3
200 г тринатрийфосфата (см. 4.2.2) растворяют в воде в мерной колбе вместимостью 1 дм3, объем содержимого доводят водой до метки.
4.2.10 Раствор L-цистеина массовой концентрацией ρ (C3H7NO2S) = 40 г/дм3
20 г цистеина (см. 4.2.4) растворяют в воде в мерной колбе вместимостью 500 см3, объем содержимого доводят водой до метки. Раствор готовят в день проведения анализа.
4.2.11 Подвижная фаза для ВЭЖХ
Раствор А
13, 6 г однозамещенного фосфата калия (см. 4.2.3) растворяют в стакане в 900 см3 воды. Раствор фильтруют через мембранный фильтр размером пор 0, 45 мкм.
Раствор В
100 см3 цетримида (см. 4.2.5) растворяют в стакане в 100 см3 метанола (см. 4.2.6). Раствор фильтруют через мембранный фильтр размером пор 0, 45 мкм.
Приготовленные растворы смешивают, используя 900 см3 раствора А и 100 см3 раствора В. Полученную подвижную фазу для ВЭЖХ при необходимости перед употреблением дегазируют.
4.2.12 Крахмал (применяется по выбору пользователя), раствор массовой концентрацией 1 г/100 см3.
4.2.13 Йод (применяется по выбору пользователя), раствор концентрацией с (I2) = 0, 05 моль/дм3.
4.2.14 Кислота серная, раствор концентрацией с (H2SO3) = 0, 1 моль/дм3.
4.3 Стандартные вещества
4.3.1 Кислота аскорбиновая (L(+)-аскорбиновая) с массовой долей w (C6H8O6)≥99, 0%
(R)-5-[(S)-1, 2-дигидроксиэтил]-3, 4-дигидрокси-5-Н-фуран-2-он.
4.3.2 Кислота изоаскорбиновая (D(-)-аскорбиновая) с массовой долей = w (C6H8O6)≥99, 0%
(R)-5-[(R)-1, 2-дигидроксиэтил]-3, 4-дигидрокси-5-Н-фуран-2-он.
4.4 Основные стандартные растворы
4.4.1 Основной стандартный раствор аскорбиновой кислоты с массовой концентрацией ρ (C6H8O6) = 1 мг/см3
100 мг аскорбиновой кислоты (см. 4.3.1), измеренной с точностью до 0, 1 мг, растворяют в определенном объеме (например, 100 см3) раствора метафосфорной кислоты (см. 4.2.8). Раствор готовят в день проведения анализа.
Стабильность основного раствора аскорбиновой кислоты может быть повышена добавлением L-цистеина.
4.4.2 Основной стандартный раствор изоаскорбиновой кислоты с массовой концентрацией ρ (C6H8O6) = 1 мг/см3
100 мг изоаскорбиновой кислоты (см. 4.3.2), измеренной с точностью до 0, 1 мг, растворяют в определенном объеме (например, 100 мл) раствора метафосфорной кислоты (см. 4.2.8). Раствор готовят в день проведения анализа.
4.4.3 Проверка концентрации основного стандартного раствора (выполняется по выбору пользователя)
Около 150 мг аскорбиновой кислоты помещают в колбу Эрленмейера, добавляют 10 см3 раствора серной кислоты (см. 4.2.14) и 80 см3 воды, не содержащей диоксида углерода, содержимое колбы перемешивают до полного растворения аскорбиновой кислоты. После добавления раствора крахмала (см. 4.2.12) полученный раствор титруют раствором йода (см. 4.2.13) до появления устойчивой синей окраски. Масса аскорбиновой кислоты, эквивалентная 1 см3 раствора йода, пошедшего на титрование, составляет 8, 81 мг.
Массовую долю основного компонента в стандартном веществе wst, %, вычисляют по формуле
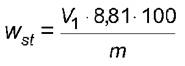 ,
,
(1)
где V1 - объем раствора йода, пошедший на титрование, см3;
8, 81 - коэффициент пересчета;
100 - коэффициент пересчета результата в процентное содержание;
m - масса навески стандартного вещества, мг.
4.5 Градуировочные растворы
4.5.1 Градуировочные растворы аскорбиновой кислоты массовыми концентрациями ρ (C6H8O6) = 5 - 50 мкг/см3
От 0, 5 до 5, 0 см3 основного раствора аскорбиновой кислоты (см. 4.4.1) переносят пипеткой в мерные колбы вместимостью 100 см3, объем содержимого в колбах доводят до метки раствором метафосфорной кислоты (см. 4.2.8). Растворы готовят в день проведения анализа.
4.5.2 Градуировочный раствор изоаскорбиновой кислоты с массовой концентрацией ρ (C6H8O6) = 10 мкг/см3
1 см3 основного раствора изоаскорбиновой кислоты (см. 4.4.2) переносят пипеткой в мерную колбу вместимостью 100 см3, объем содержимого доводят до метки раствором метафосфорной кислоты (см. 4.2.8). Раствор готовят в день проведения анализа.
5 Приборы и оборудование
5.1 Общие положения
Для проведения испытаний используют лабораторные приборы, лабораторную посуду и оборудование из стекла, в частности перечисленные ниже.
5.2 Спектрофотометр с рабочим спектральным диапазоном в ультрафиолетовой области, пригодный для измерения оптической плотности при приведенных ниже длинах волн.
5.3 Жидкостный хроматограф
Система для ВЭЖХ, состоящая из насоса, устройства ввода пробы, спектрофотометрического детектора, пригодного для измерения оптической плотности при длине волны 265 нм, и системы сбора и обработки данных, например интегратора.
5.4 Колонка для ВЭЖХ-анализа
5.4.1 Общие положения
Критерием пригодности колонки является разделение пиков L-аскорбиновой и изоаскорбиновой кислот на уровне базовой линии [3].
5.4.2 Параметры хроматографической колонки
Колонка с внутренним диаметром 4, 0 мм, длиной 250 мм, заполненная обращенно-фазовым сорбентом на основе силикагеля с привитыми октадецильными группами и блокированными остаточными силанольными группами размером частиц сорбента 5 мкм.
Допустимо использовать колонку с другими размерами частиц сорбента или размерами колонки, чем те, что указаны в настоящем стандарте.
5.5 Устройство для фильтрации
Фильтрование подвижной фазы и раствора пробы перед использованием или вводом в хроматограф через мембранный фильтр размером пор, например, 0, 2 или 0, 4 мкм, продлевает срок службы колонки.
6 Процедура проведения испытания
6.1 Общие положения
При проведении испытания обеспечивают предельно короткий промежуток времени между приготовлением растворов проб и градуировочных растворов и их анализом. Температура в помещении при проведении анализа не должна превышать 25°С. Предельный срок использования анализируемых растворов - 8 ч с момента их приготовления.
6.2 Подготовка пробы
Исследуемую пробу гомогенизируют. Если проба представляет собой продукт твердой консистенции, ее измельчают на мельнице подходящей конструкции и снова тщательно перемешивают. Анализ пробы проводят непосредственно после ее гомогенизации. Подготовку к анализу проб свежих фруктов и овощей проводят одновременно с экстракцией (см. 6.3.1).
6.3 Приготовление раствора пробы для анализа
6.3.1 Экстракция
Навеску пробы массой, например, 3 г (при содержании витамина С в пробе около 50 мг/100 г), измеренной с точностью до 1 мг, помещают в мерную колбу вместимостью 100 см3, добавляют 80 см3 раствора метафосфорной кислоты (см. 4.2.8), тщательно перемешивают, после чего объем в колбе доводят до метки. Содержимое колбы снова перемешивают, после чего фильтруют. Полученный раствор представляет собой экстракт из пробы.
При анализе свежих фруктов и овощей от 2 до 10 г измельченной ножом пробы помещают в стакан вместимостью 100 см3, затем вносят некоторое количество раствора метафосфорной кислоты (см. 4.2.8). Содержимое стакана гомогенизируют, количественно переносят в мерную колбу вместимостью 100 см3, перемешивают и фильтруют. Полученный раствор представляет собой экстракт из пробы.
Примечание - Стабильность аскорбиновой кислоты в растворе можно повысить, например, путем добавления к раствору метафосфорной кислоты 125 см3 раствора L-цистеина (см. 4.2.10), дитиотрейтола или диэтилтиаминфосфорной кислоты. При этом следует иметь в виду, что эти стабилизаторы могут влиять на качество хроматографического разделения. Данная процедура не была использована при проведении межлабораторных испытаний.
6.3.2 Проведение реакции восстановления
Аликвоту отфильтрованного экстракта (см. 6.3.1) объемом 20 см3 переносят в стакан вместимостью 50 см3, добавляют 10 см3 раствора L(+)-цистеина. Значение рН полученного раствора доводят до 7, 0 - 7, 2 при измерении с помощью рН-метра путем добавления по каплям раствора тринатрийфосфата (см. 4.2.9) при постоянном перемешивании с помощью магнитной мешалки. По достижении указанного значения рН раствор выдерживают точно 5 мин при постоянном перемешивании. По истечении указанного времени значение рН раствора доводят до 2, 5 - 2, 8 (по рН-метру) путем добавления по каплям раствора метафосфорной кислоты (см. 4.2.7) при постоянном перемешивании. Полученный раствор количественно переносят в мерную колбу вместимостью 50 см3, при этом электроды рН-метра, рабочий элемент магнитной мешалки и стакан, в котором находился раствор, ополаскивают водой, перенося смывы в ту же колбу. Объем содержимого в мерной колбе доводят до метки водой, содержимое колбы перемешивают. Полученный раствор фильтруют через мембранный фильтр (см. 5.5), фильтрат используют для хроматографического анализа.
При наличии информации о присутствии в анализируемом продукте добавок-загустителей рекомендуется их удалить из анализируемого раствора перед его хроматографическим анализом во избежание порчи хроматографической колонки. Для этого к порции восстановленного раствора пробы объемом 4 см3 добавляют 1 см3 метанола (см. 4.2.6), полученный раствор перемешивают и фильтруют через мембранный фильтр (см. 5.5). Фильтрат используют для хроматографического анализа.
6.4 Идентификация
Пик L-аскорбиновой кислоты на хроматограмме раствора пробы идентифицируют по совпадению его времени удерживания со временем удерживания пика аналита на хроматограмме градуировочного раствора, полученной при тех же параметрах хроматографического анализа. Идентификацию пика аналита можно также проводить путем добавления стандартного раствора в раствор пробы.
Ниже приведены параметры хроматографического анализа, обеспечивающие требуемую степень хроматографического разделения и пригодные для количественного определения (см. также рисунок А.1). Данные параметры были использованы при проведении межлабораторных испытаний.
Параметры хроматографической колонки: колонка, заполненная обращенно-фазовым сорбентом на основе силикагеля с привитыми октадецильными группами и блокированными остаточными силанольными группами размером частиц сорбента 5 мкм, длина колонки 250 мм, внутренний диаметр 4, 0 мм;
подвижная фаза.............смесь раствора А и раствора В (4.2.11);
скорость потока подвижной фазы........................0, 7 см3/мин;
инжектируемый объем........................................30 мм3;
длина волны детектирования.................................265 нм.
Данные параметры хроматографического анализа позволяют также идентифицировать пик изоаскорбиновой кислоты, не являющейся витамином С.
Примечание - В качестве других приемлемых параметров хроматографического анализа можно использовать подвижную фазу, состоящую из 10% ацетонитрила и 90% смешанного водного раствора однозамещенного фосфата калия массовой концентрацией 13, 6 г/дм3 и цетримида концентрацией 2 г/дм3 в сочетании с колонкой, заполненной обращенно-фазовым сорбентом с привитыми октильными группами (C8) размером частиц 10 мкм, длиной 250 мм, внутренним диаметром 4, 6 мм, при скорости потока (1, 0±0, 1) см3/мин.
6.5 Количественное определение
Проводят хроматографический анализ раствора пробы и градуировочного раствора при одинаковых объемах инжекции (до 50 мм3). Обработку результатов проводят по методу внешнего стандарта либо с использованием градуировочной характеристики.
При использовании метода внешнего стандарта массовую концентрацию анализируемого вещества в растворе пробы рассчитывают, исходя из площади или высоты пика аналита на хроматограмме раствора пробы и соотношения между массовой концентрацией аналита в градуировочном растворе и площадью или высотой пика на хроматограмме этого раствора.
При использовании градуировочной характеристики контролируют соблюдение условия нахождения ее области определения в границах линейной зависимости аналитического сигнала от массовой концентрации аналита.
7 Обработка результатов
Расчет результата анализа проводят с использованием градуировочной характеристики или с помощью соответствующей программы интегратора, либо применяют следующий упрощенный способ.
Массовую долю аскорбиновой кислоты w, мг/100 г, вычисляют по формуле
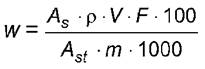 ,
,
(2)
где As - площадь или высота пика L-аскорбиновой кислоты на хроматограмме раствора пробы (см. 6.3.2), в единицах площади или высоты;
ρ- массовая концентрация L-аскорбиновой кислоты в градуировочном растворе, мкг/см3;
V - общий объем приготовленного по 6.3.1 раствора пробы перед проведением реакции восстановления, см3;
F - коэффициент разбавления, применяемого при проведении реакции восстановления (в данном случае F = 2, 5);
100 - коэффициент пересчета результата в мг на 100 г;
Ast - площадь или высота пика L-аскорбиновой кислоты на хроматограмме градуировочного раствора (см. 4.5.1), в единицах площади или высоты;
m - масса навески пробы, г;
1000 - коэффициент пересчета из микрограммов в миллиграммы.
Результат выражают в мг/100 г.
В случае, если процедура анализа включала в себя операцию осаждения загустителей по 6.3.2, результат, полученный по формуле (2), умножают на 5/4.
8 Прецизионность
8.1 Общие положения
Значения характеристик прецизионности при определении витамина С были получены в 1997 г. в результате межлабораторных испытаний, проведенных в соответствии с ИСО 5725 [2], [4]. Для других областей содержания аналита и типов матриц значения характеристик прецизионности методики могут отличаться от значений, приведенных в приложении В.
8.2 Повторяемость
Абсолютное расхождение между результатами двух независимых единичных испытаний, полученными одним методом на идентичном объекте испытаний в одной лаборатории одним оператором с использованием одного оборудования в течение короткого промежутка времени, должно превышать предел повторяемости r не более чем в 5% случаев.
Значения предела повторяемости равны:
апельсиновый сок: x̅ = 54, 6 мг/100 г, r = 6, 4 мг/100 г;
овощной консервированный суп: x̅ = 35, 6 мг/100 г, r = 3, 7 мг/100 г;
сухое молоко (порошок): x̅ = 100, 3 мг/100 г, r = 17, 9 мг/100 г;
суп-концентрат сублимационной сушки: x̅ = 169, 3 мг/100 г, r = 42, 0 мг/100 г;
сухой завтрак (концентрат): x̅ = 102, 6 мг/100 г, r = 28, 7 мг/100 г;
фруктовые консервы для детского питания: x̅ = 47, 1 мг/100 г, r = 7, 1 мг/100 г.
8.3 Воспроизводимость
Абсолютное расхождение между результатами двух единичных испытаний, полученными одним методом на идентичном объекте испытаний в разных лабораториях разными операторами с использованием разного оборудования, должно превышать предел воспроизводимости R не более чем в 5% случаев.
Значения предела воспроизводимости равны:
апельсиновый сок: x̅ = 54, 6 мг/100 г, R = 30, 3 мг/100 г;
овощной консервированный суп: x̅ = 35, 6 мг/100 г, R = 21, 7 мг/100 г;
сухое молоко (порошок): x̅ = 100, 3 мг/100 г, R = 32, 2 мг/100 г;
суп-концентрат сублимационной сушки: x̅ = 169, 3 мг/100 г, R = 74, 3 мг/100 г;
сухой завтрак (концентрат): x̅ = 102, 6 мг/100 г, R = 56, 2 мг/100 г;
фруктовые консервы для детского питания: x̅ = 47, 1 мг/100 г, R = 23, 9 мг/100 г.
9 Протокол результатов испытаний
Протокол результатов испытаний должен содержать, как минимум, следующие сведения:
- всю информацию, необходимую для идентификации пробы;
- ссылку на настоящий стандарт или использованный метод;
- дату и время отбора пробы (если известны);
- дату поступления пробы в лабораторию;
- дату проведения испытания;
- результаты испытания с указанием единиц измерения;
- все особенности, наблюдавшиеся при проведении испытания;
- все операции, не оговоренные в методике или считающиеся необязательными, которые могли повлиять на результат испытания.
Приложение А
(справочное)
Пример хроматограммы
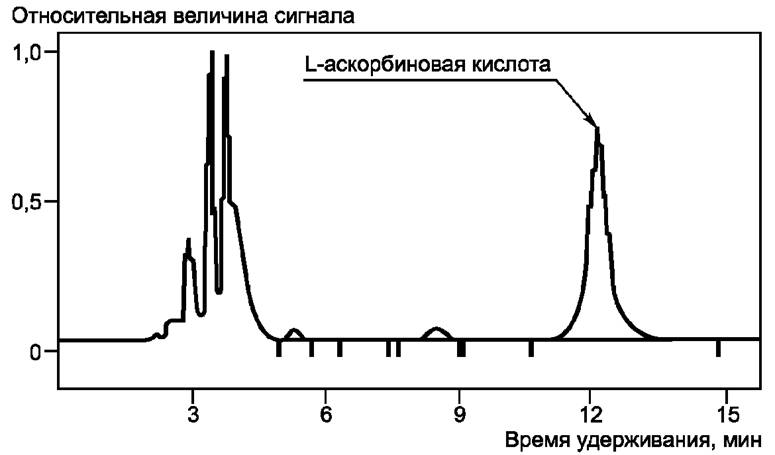
Рисунок А.1 - Пример хроматограммы при анализе аскорбиновой кислоты в апельсиновом соке с помощью ВЭЖХ
Условия хроматографического анализа:
колонка, заполненная сорбентом Lichrospher 100 RP 18 с блокированными остаточными силанольными группами размером частиц сорбента 5 мкм, внутренний диаметр колонки 4, 0 мм, длина 250 мм;
подвижная фаза - смесь раствора А и раствора В (см. 4.2.11);
скорость потока - 0, 7 см3/мин;
инжектируемый объем - 30 мм3;
длина волны детектирования - 265 нм;
время удерживания аскорбиновой кислоты - tret = 11, 953 мин.
Приложение В
(справочное)
Данные по прецизионности методики
Приведенные ниже данные получены в результате межлабораторных испытаний [2], [4]. Процедура проведения испытания не включала в себя операцию восстановления L-дегидроаскорбиновой кислоты.
Примечание - После проведения данных межлабораторных испытаний ИСО 5725:1986 был заменен на ИСО 5725-1, ИСО 5725-2, ИСО 5725-3, ИСО 5725-4 и ИСО 5725-6 (все издания 1994 г.), а также ИСО 5725-5:1998.
Таблица В.1 - Данные по прецизионности определения общего содержания витамина С
|
Образец
|
1
|
2
|
3
|
4
|
5
|
6
|
|
Год проведения испытаний
|
1997
|
1997
|
1997
|
1997
|
1997
|
1997
|
|
Число лабораторий-участников
|
15
|
15
|
15
|
15
|
15
|
15
|
|
Число лабораторий, за исключением выбросов
|
14
|
15
|
14
|
14
|
14
|
14
|
|
Число принятых результатов
|
28
|
30
|
28
|
28
|
28
|
28
|
|
Среднее значение х, мг/100 г
|
54, 6
|
35, 6
|
100, 3
|
169, 3
|
102, 6
|
47, 1
|
|
Стандартное отклонение повторяемости sr, мг/100 г
|
2, 3
|
1, 3
|
6, 3
|
14, 8
|
10, 2
|
2, 5
|
|
Относительное стандартное отклонение повторяемости, %
|
4, 2
|
3, 6
|
6, 3
|
8, 8
|
9, 9
|
5, 3
|
|
Предел повторяемости (r=2, 83·sr), мг/100 г
|
6, 4
|
3, 7
|
17, 9
|
42, 0
|
28, 7
|
7, 1
|
|
Стандартное отклонение воспроизводимости sR, мг/100 г
|
10, 7
|
7, 7
|
11, 4
|
26, 2
|
19, 8
|
8, 5
|
|
Относительное стандартное отклонение воспроизводимости, %
|
19, 7
|
21, 6
|
11, 4
|
15, 5
|
9, 3
|
18, 0
|
|
Предел воспроизводимости (R=2, 83·sR), мг/100 г
|
30, 3
|
21, 7
|
32, 2
|
74, 3
|
56, 2
|
23, 9
|
|
1 - апельсиновый сок; 2 - овощной консервированный суп; 3 - сухое молоко; 4 - суп-концентрат сублимационной сушки; 5 - сухой завтрак (концентрат); 6 - фруктовые консервы для детского питания.
|
Приложение ДА
(справочное)
Сведения о соответствии ссылочных международных стандартов ссылочным национальным стандартам Российской Федерации
Таблица ДА.1
|
Обозначение ссылочного международного стандарта
|
Степень соответствия
|
Обозначение и наименование соответствующего национального стандарта
|
|
ЕН ИСО 3696
|
MOD
|
ГОСТ Р 52501-2005 (ИСО 3696:1987) "Вода для лабораторного анализа. Технические условия"
|
|
Примечание - В настоящей таблице использовано следующее условное обозначение степени соответствия стандартов:
- MOD - модифицированный стандарт.
|
Библиография
|
[1]
|
Dennison D.B., Brawley T.G., Hunter G.L.K., (1981), J. Agric. Food Chem., 29, 925 - 927
|
|
[2]
|
Arella F., Deborde J.L., Bourguignon J.В., Hasselmann C. (1997) Ann. Fals. Exp. Chim., 90, No 940, 217 - 233
|
|
[3]
|
Coustard J.M., Sudraud G., (1981), Journal of Chromatogtaphy, 219, 338-3-42
|
|
[4]
|
ISO 5725:1986, Precision of test methods. Determination of repeatability and reproducibility for a standard test method by inter-laboratory tests
|
![]() — Все документы — ГОСТы — ГОСТ Р ЕН 14130-2010 ПРОДУКТЫ ПИЩЕВЫЕ. ОПРЕДЕЛЕНИЕ ВИТАМИНА С С ПОМОЩЬЮ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ
— Все документы — ГОСТы — ГОСТ Р ЕН 14130-2010 ПРОДУКТЫ ПИЩЕВЫЕ. ОПРЕДЕЛЕНИЕ ВИТАМИНА С С ПОМОЩЬЮ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
 Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
 «МК»: в России не отменят льготную ипотеку
«МК»: в России не отменят льготную ипотеку
 Аренда квартир в Москве подешевела на 10 %
Аренда квартир в Москве подешевела на 10 %
 Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
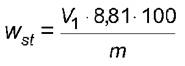 ,
,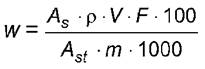 ,
,