Утв. Приказом Федерального агентства по техническому регулированию и метрологии от 12 декабря 2011 г. N 783-ст
Национальный стандарт РФ ГОСТ Р 54634-2011
"ПРОДУКТЫ ПИЩЕВЫЕ ФУНКЦИОНАЛЬНЫЕ. МЕТОД ОПРЕДЕЛЕНИЯ ВИТАМИНА Е"
Functional food products. Method of vitamin E determination
Дата введения - 1 января 2013 г.
Введен впервые
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом N 184-ФЗ "О техническом регулировании" от 27 декабря 2002 г., а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 Разработан Учреждением Российской академии медицинских наук Научно-исследовательским институтом питания
2 Внесен Техническим комитетом по стандартизации ТК 36 "Функциональные пищевые продукты"
3 Утвержден и введен в действие приказом Федерального агентства по техническому регулированию и метрологии от 12 декабря 2011 г. N 783-ст
4 Введен впервые
1 Область применения
Настоящий стандарт распространяется на функциональные пищевые продукты и устанавливает метод определения массовой доли витамина Е в виде α-, β -, γ-, δ -токоферолов, ацетата α -токоферола с помощью высокоэффективной жидкостной хроматографии (далее - ВЭЖХ).
Диапазон измерений массовой доли витамина Е составляет от 5 до 500 млн-1.
Примечание - Настоящий стандарт допускается распространять на пищевые продукты при условии соблюдения диапазона измерений.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р 8.563-2009 Государственная система обеспечения единства измерений. Методики (методы) измерений
ГОСТ Р 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ Р ИСО/МЭК 17025-2006 Общие требования к компетентности испытательных и калибровочных лабораторий
ГОСТ Р 51652-2000 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ Р 52062-2003 Масла растительные. Правила приемки и методы отбора проб
ГОСТ Р 52179-2003 Маргарины, жиры для кулинарии, кондитерской, хлебопекарной и молочной промышленности. Правила приемки и методы контроля
ГОСТ Р 52349-2005 Продукты пищевые. Продукты пищевые функциональные. Термины и определения
ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 427-75 Линейки измерительные металлические. Технические условия
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
ГОСТ 4517-87 Реактивы. Методы приготовления вспомогательных реактивов и растворов, применяемых при анализе
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 8981-78 Эфиры этиловый и нормальный бутиловый уксусной кислоты технические. Технические условия
ГОСТ 9293-74 Азот газообразный и жидкий. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 13496.0-80 Комбикорма, сырье. Методы отбора проб
ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия
ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия
ГОСТ 19627-74 Гидрохинон (парадиоксибензол). Технические условия
ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26809-86 Молоко и молочные продукты. Правила приемки, методы отбора и подготовка проб к анализу
ГОСТ 27025-86 Реактивы. Общие указания по проведению испытаний
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодно издаваемому информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены термины по ГОСТ Р 52349, а также следующий термин с соответствующим определением:
3.1 содержание витамина Е: Массовая доля токоферолов (α -, β -, γ- и δ -токоферолов, ацетата α -токоферола), определенная в соответствии с настоящим стандартом и выраженная в миллионных долях, млн-1.
Примечание - При вычислении содержания витамина Е в единицах токофероловых эквивалентов (один токофероловый эквивалент соответствует 1 мг d- α -токоферола), количество мг токоферолов следует умножить на соответствующий коэффициент пересчета: для dl- α -токоферола - 0, 74, dl- α -токоферола ацетата - 0, 67, d- β -токоферола - 0, 5, d- γ -токоферола - 0, 1, d- δ -токоферола - 0, 03.
4 Сущность метода
Определение витамина Е в экстракте, полученном из анализируемой пробы, проводят разделением токоферолов методом нормально-фазной (далее - НФ) или обращенно-фазной (далее - ОФ) ВЭЖХ с последующим фотометрическим или флуориметрическим детектированием. При необходимости экстракт получают после щелочного гидролиза анализируемой пробы.
Количественный анализ проводят методом внешнего стандарта с использованием площади или высоты пиков токоферолов.
5 Требования безопасности
5.1 Условия безопасного проведения работ
При выполнении испытаний необходимо соблюдать требования пожарной безопасности, установленные ГОСТ 12.1.004, электробезопасности - ГОСТ Р 12.1.019, техники безопасности при работе с реактивами - ГОСТ 12.1.007, а также требования, изложенные в технической документации на спектрофотометр, хроматограф, другие приборы и оборудование.
Помещение, в котором проводят испытания, должно быть снабжено приточно-вытяжной вентиляцией. Контроль за содержанием вредных веществ в воздухе рабочей зоны следует проводить в соответствии с требованиями ГОСТ 12.1.005.
При работе с газовыми баллонами необходимо руководствоваться [1].
5.2 Требования к квалификации оператора
К выполнению испытаний и обработке результатов допускаются лица с высшим или средним специальным образованием по профессиям химик, инженер-химик, техник, лаборант, имеющие опыт работы в химической лаборатории. Первое применение метода в лаборатории следует проводить под наблюдением квалифицированного специалиста в области ВЭЖХ.
6 Условия выполнения испытания
6.1 Общие условия
Испытания проводят в нормальных лабораторных условиях: температура окружающей среды - (25±5)°С; относительная влажность - (65±15)%; частота переменного тока - (50±5) Гц; напряжение в сети - (220±10) В.
При приготовлении и хранении растворов следует выполнять требования ГОСТ 27025, ГОСТ 4517.
Для предотвращения разрушения токоферолов анализ испытуемого материала и стандартов проводят в присутствии антиоксиданта (аскорбиновой кислоты, гидрохинона, пирогаллола), предохраняя пробы от попадания на них прямого солнечного света.
6.2 Условия фотометрических измерений
Условия фотометрических измерений приведены в таблице 1.
Таблица 1 - Условия фотометрических измерений
|
Токоферолы
|
Растворитель
|
Длина волны, нм
|
Удельный коэффициент поглощения 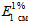
|
|
α -токоферол
|
Метанол
|
292
|
76
|
|
β -токоферол
|
Метанол
|
296
|
89
|
|
γ-токоферол
|
Метанол
|
298
|
91
|
|
δ-токоферол
|
Метанол
|
298
|
87
|
|
Ацетат α -токоферола
|
Этанол
|
285
|
44
|
6.3 Условия хроматографического анализа
Температура хроматографической колонки: 25°С или окружающей среды.
Скорость потока подвижной фазы: 0, 7 см3/мин (ориентировочное значение).
Объем вводимой пробы: от 10·10-3 до 50·10-3 см3.
Подвижная фаза для ОФ ВЭЖХ: смесь ацетонитрила, метилового спирта, метилена хлористого в объемном соотношении 50:45:5.
Подвижная фаза для НФ ВЭЖХ: смесь н-гексана и 2-пропанола в объемном соотношении 98:2.
Проверку оптимальности условий хроматографического разделения осуществляют путем хроматографического анализа смешанного раствора токоферолов с массовой концентрацией каждого токоферола не менее 10 мкг/см3. Данный раствор готовят из основных растворов α - (β -, γ - и δ -)токоферола и ацетата α -токоферола по аналогии с методикой приготовления рабочих растворов по 8.1.2. Эффективность хроматографического разделения признается удовлетворительной, если коэффициент разделения соседних пиков токоферолов (за исключением пиков β - и γ -токоферолов, которые не разделяются в режиме ОФ ВЭЖХ) составляет 1, 3. В противном случае для достижения требуемой эффективности разделения экспериментальным путем подбирают скорость потока подвижной фазы или проводят испытания других колонок.
7 Средства измерений, вспомогательные устройства, реактивы и материалы
7.1 Для определения содержания массовой доли витамина Е применяют следующие средства измерений, вспомогательное оборудование и материалы:
- весы по ГОСТ Р 53228, обеспечивающие точность взвешивания с пределами допускаемой абсолютной погрешности ±0, 1 мг;
- спектрофотометр со спектральным диапазоном работы от 190 до 1100 нм, основной погрешностью измерений коэффициента пропускания не более 1%;
- кюветы кварцевые с длиной оптического пути 1 см;
- хроматограф высокоэффективный жидкостный, включающий следующие элементы: насос, устройство для ввода проб, колонку аналитическую для НФ ВЭЖХ диаметром 0, 30 - 0, 46 см, длиной 10 - 25 см, заполненную силикагелем или силикагелем, модифицированным диол-, CN- или NH2-группами или колонку аналитическую для ОФ ВЭЖХ диаметром 0, 30 - 0, 46 см, длиной 10 - 25 см, заполненную октадецилсиликагелем с размером частиц 5 мкм; флуориметрический детектор (длины волн, нм: возбуждения - 295 нм, эмиссии - 330 нм) или спектрофотометрический детектор (длина волны детектирования - 292 нм) и погрешностью измерений не более 10% отн.; регистрирующее устройство: интегратор или самописец, позволяющий проводить измерение площади (или высоты) пика с погрешностью не более 1%; программное обеспечение для обработки полученных результатов измерений;
- фильтры для фильтрования подвижной фазы и анализируемых растворов (например, с размером пор 0, 45 мкм);
- микрошприц типа "Гамильтон" вместимостью 0, 1 см3 для ввода проб в жидкостный хроматограф;
- пипетки градуированные 1(2, 3)-1(2)-1-0, 5(1, 2, 5, 10, 25) по ГОСТ 29227 или дозаторы автоматические с аналогичными или изменяемыми объемами доз с относительной погрешностью дозирования не более ±1%;
- цилиндры 1-50(100, 250)-1(2) по ГОСТ 1770;
- колбы мерные 2-50(100, 250, 500, 1000)-2 по ГОСТ 1770;
- пробирки мерные с притертыми пробками П-2-5(10, 15, 20, 25)-0, 1(0, 2)ХС по ГОСТ 1770;
- стаканы В(Н)-1-50(100, 150, 250)ТХС по ГОСТ 25336;
- колбы круглодонные К-1-100(250, 500)-29/32ТС по ГОСТ 25336;
- воронки В-36(56)-80ХС, В-75-110(140)ХС, В-100-150ХС по ГОСТ 25336;
- линейка металлическая с ценой деления 1 мм по ГОСТ 427;
- встряхиватель для колб и пробирок с диапазоном частот колебаний платформ 100 - 150 колебаний в минуту;
- центрифуга, обеспечивающая 4 - 6 тыс. об/мин;
- баня водяная с регулятором нагрева, способная поддерживать температуру от 40°С до 100°С;
- баня ультразвуковая лабораторная рабочим объемом не менее 2 дм3;
- испаритель ротационный с диапазоном рабочего давления от 7 до 760 мм рт. ст. (от 9·102 до 10·104 Па) или насос водоструйный по ГОСТ 25336;
- холодильники стеклянные лабораторные по ГОСТ 25336;
- термометр лабораторный жидкостный, диапазон измерений от 0°С до 100°С, цена деления шкалы 1°С по ГОСТ 28498;
- баллон с газообразным азотом по ГОСТ 9293, ос.ч. или по [1];
- бумага фильтровальная лабораторная по ГОСТ 12026;
- плитка электрическая закрытого типа по ГОСТ 14919;
- мельница лабораторная электрическая;
- холодильник бытовой по ГОСТ 16317.
7.2 При выполнении измерений применяют следующие реактивы и материалы:
- спирт этиловый абсолютный (C2H5OH) массовой долей основного вещества не менее 99, 9%;
- спирт этиловый ректификованный (C2H5OH) массовой долей основного вещества не менее 96% или по ГОСТ Р 51652, ГОСТ 18300;
- спирт метиловый (CH3OH) массовой долей основного вещества не менее 99, 9%;
- ацетонитрил (CH3CN) массовой долей основного вещества не менее 99, 8%;
- метилен хлористый (CH2Cl2) массовой долей основного вещества не менее 99, 8 '%;
- н-гексан (C6H14) массовой долей основного вещества не менее 99%;
- этилацетат (C4H8O2) массовой долей основного вещества не менее 99% или по ГОСТ 8981;
- 2-пропанол (C3H8O) массовой долей основного вещества не менее 99%;
- эфир петролейный, перегнанный при температуре (50±10)°С, очищенный от перекисей;
- эфир диэтиловый, очищенный от перекисей, содержащий 0, 1% пирогаллола по [2];
- калия гидроокись (КОН) по ГОСТ 24363, х.ч. или ч.д.а., раствор КОН массовой долей 50%;
- натрий сернокислый (Na2SO4) безводный массовой долей основного вещества не менее 99, 5% или по ГОСТ 4166, х.ч.;
- воду дистиллированную по ГОСТ 6709;
- кислоту аскорбиновую (C6H8O6) по [3] или [4], х.ч.;
- гидрохинон (C6H6O2) массовой долей основного вещества не менее 99% или по ГОСТ 19627;
- пирогаллол (C6H6O3) массовой долей основного вещества не менее 99%;
- бутилгидрокситолуол (C15H24O) массовой долей основного вещества не менее 99%;
- α -токоферол М(C29H50O2) = 430, 7 г/моль, массовой долей основного вещества не менее 95%;
- α -токоферола ацетат М(C31H52O3) = 472, 7 г/моль, массовой долей основного вещества не менее 95% или по [5], или по [6];
- β -токоферол М(C28H48O2) = 416, 7 г/моль, массовой долей основного вещества не менее 90%;
- γ -токоферол М(C28H48O2) = 416, 7 г/моль, массовой долей основного вещества не менее 90%;
- δ -токоферол М(C27H46O2) = 402, 7 г/моль, массовой долей основного вещества не менее 90%.
7.3 Допускается применение других средств измерений, вспомогательного оборудования, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающих необходимую точность измерения, а также реактивов и материалов по качеству не хуже вышеуказанных.
8 Подготовка к выполнению измерений
8.1 Приготовление растворов
8.1.1 Исходные растворы стандартов
8.1.1.1 Исходные растворы стандартов токоферолов готовят растворением около 10 мг α -токоферола (β -токоферола, γ -токоферола, δ -токоферола) в 100 см3 метилового спирта. Массовые концентрации α -, β -, γ - и δ -токоферолов составляют 0, 1 мг/см3.
8.1.1.2 Исходные растворы стандартов ацетата α -токоферола готовят растворением около 20 мг α -токоферола ацетата в 100 см3 этилового спирта абсолютного (для проведения ОФ хроматографии) или в 100 см3 н-гексана (для проведения НФ хроматографии). Массовая концентрация ацетата α -токоферола составляет 0, 2 мг/см3.
8.1.1.3 Определение концентрации стандартных веществ в исходных растворах (c, мкг/см3) проводят после измерения их оптической плотности при оптимальной длине волны на спектрофотометре и вычисляют по формуле
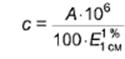 ,
,
(1)
где А - оптическая плотность стандартного раствора;
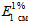 - оптическая плотность раствора стандартных веществ в метиловом спирте или этиловом спирте абсолютном массовой концентрации 1 г в 100 см3 при толщине поглощающего слоя 1 см, представленная в таблице 1;
- оптическая плотность раствора стандартных веществ в метиловом спирте или этиловом спирте абсолютном массовой концентрации 1 г в 100 см3 при толщине поглощающего слоя 1 см, представленная в таблице 1;
106 - коэффициент пересчета граммов в микрограммы;
100 - коэффициент пересчета на 1 см3.
8.1.2 Рабочие растворы стандартов
8.1.2.1 Из исходных растворов готовят не менее четырех рабочих растворов каждого (α -, β -, γ - и δ -) токоферола в диапазоне концентрации 1 - 10 мкг/см3 при использовании флуориметрического детектора. Для этого точный объем 1 - 10 см3 исходного раствора α -, β -, γ - и δ -токоферола, приготовленного по 8.1.1.1 для НФ или ОФ ВЭЖХ, с помощью пипетки или дозатора помещают в мерную колбу объемом 100 см3 и доводят до метки соответствующим растворителем (н-гексаном для анализа в варианте НФ ВЭЖХ и метиловым спиртом - для ОФ ВЭЖХ). Если анализ проводят с помощью спектрофотометрического детектора, концентрация α -, β -, γ - и δ -токоферола в градуировочных растворах должна находиться в диапазоне 2 - 20 мкг/см3. Для этого точный объем 2 - 20 см3 исходного раствора α -, β -, γ - и δ -токоферола, приготовленного по 8.1.1.1 для НФ или ОФ ВЭЖХ, помещают в мерную колбу объемом 100 см3 и доводят до метки соответствующим растворителем (н-гексаном для анализа в варианте НФ ВЭЖХ и метиловым спиртом - для ОФ ВЭЖХ).
8.1.2.2 Из исходных растворов готовят не менее четырех рабочих растворов α -токоферола ацетата в диапазоне концентрации 5 - 50 мкг/см3 при использовании спектрофотометрического детектора. Для этого точный объем 2, 5 - 25 см3 исходного раствора, приготовленного по 8.1.1.2 для НФ или ОФ ВЭЖХ, с помощью пипетки или дозатора помещают в мерную колбу объемом 100 см3 и доводят до метки соответствующим растворителем (н-гексаном для анализа в варианте НФ ВЭЖХ и метиловым спиртом - для ОФ ВЭЖХ). Если анализ проводят с помощью флуориметрического детектора, из исходных растворов готовят не менее четырех градуировочных растворов α -токоферола ацетата в диапазоне концентрации 20 - 100 мкг/см3. Для этого точный объем 10 - 50 см3 исходного раствора α -токоферола ацетата, приготовленного по 8.1.1.2 для НФ или ОФ ВЭЖХ, с помощью пипетки или дозатора помещают в мерную колбу объемом 100 см3 и доводят до метки соответствующим растворителем (н-гексаном для анализа в варианте НФ ВЭЖХ и метиловым спиртом - для ОФ ВЭЖХ).
Все растворы входе приготовления и анализа защищают от воздействия ультрафиолетового излучения. Растворы токоферолов хранят при температуре не выше 4°С в течение 2 мес.
8.2 Отбор и подготовка проб
8.2.1 Отбор проб проводят по нормативным документам на конкретные виды продукции и по ГОСТ 13496.0, ГОСТ 26809, ГОСТ Р 52062, ГОСТ Р 52179.
8.2.2 Крупные частицы средней пробы, выделенной методом квартования из лабораторной пробы, измельчают с использованием подходящего оборудования (например, лабораторной мельницы) до такого состояния, чтобы весь продукт проходил через сито с отверстиями диаметром 1 мм. Размолотую пробу тщательно перемешивают.
Анализируемые пробы гомогенизируют, избегая воздействия повышенной температуры.
8.2.3 Пищевые продукты на масложировой основе с массовой долей воды не более 1%, обогащенные α -, β -, γ - и δ -токоферолами, а также ацетатом α -токоферола
2 - 5 г анализируемой пробы переносят в мерную колбу на 25 см3, растворяют в 10 - 15 см3 н-гексана, используя ультразвуковую баню для ускорения растворения. Раствор доводят до метки н-гексаном. При необходимости раствор можно использовать для последующего разведения н-гексаном.
8.2.4 Пищевые продукты на масложировой основе с массовой долей воды не более 20%, обогащенные α -, β -, γ - и δ -токоферолами, а также ацетатом α -токоферола
2 - 5 г анализируемой пробы переносят в колбу и растворяют при интенсивном перемешивании в 10 см3 н-гексана, используя ультразвуковую баню для ускорения растворения. Удаляют избыток воды добавлением безводного сульфата натрия. Содержимое колбы фильтруют через бумажный фильтр для отделения нерастворившегося осадка. Колбу промывают дважды 5 см3 н-гексана. Фильтраты собирают в мерную колбу вместимостью 25 см3. Раствор доводят до метки н-гексаном.
8.2.5 Другие пищевые продукты, обогащенные α -, β -, γ - и δ -токоферолами, а также ацетатом α -токоферола
Для проведения щелочного гидролиза 5 - 20 г анализируемой сухой или жидкой пробы помещают в плоскодонную колбу вместимостью 100 - 500 см3. К сухому материалу добавляют 5 - 20 см3 воды и нагревают на водяной бане при температуре от 60°С до 70°С при перемешивании в течение 5 мин. Затем прибавляют 50 - 150 см3 этилового ректификованного спирта, 0, 2 - 2, 0 г антиоксиданта (аскорбиновой кислоты, гидрохинона, бутилгидрокситолуола), 3 - 40 см3 50% раствора гидроокиси калия и нагревают в течение 15 - 40 мин на водяной бане с обратным холодильником при температуре 80°С - 100°С. Рекомендуемые соотношения испытуемой пробы и реактивов приведены в таблице 2.
Таблица 2 - Рекомендуемые соотношения испытуемого материала и реактивов
|
Массовая доля витамина Е, млн-1
|
Навеска испытуемого материала, г
|
Объем этанола, см3
|
Объем 50%-ного раствора КОН, см3
|
|
От 5 до 100 включ.
|
10 - 20
|
150
|
40
|
|
Св. 100 до 1000 включ.
|
5 - 10
|
100
|
15
|
|
Св. 1000 до 5000 включ.
|
1 - 5
|
50
|
3
|
Если после охлаждения на поверхности смеси остается слой масла или жира, то объем добавленного раствора КОН и время щелочного гидролиза увеличивают.
После окончания гидролиза содержимое колбы быстро охлаждают до (20±5)°С и количественно переносят в делительную воронку. Колбу ополаскивают водой, объем которой равен объему добавленного этилового спирта, и воду сливают в туже воронку. Токоферолы экстрагируют диэтиловым (или петролейным) эфиром, этилацетатом, н-гексаном, н-гексаном с добавкой диэтилового (или петролейного) эфира в объемном соотношении 1:1 в течение 2 мин. Если в качестве экстрагента используется н-гексан или н-гексан с добавкой диэтилового (или петролейного) эфира, то для учета возможной неполной экстракции токоферолов следует применять метод добавок стандартов.
Экстракцию повторяют три - четыре раза порциями экстрагента 50 - 100 см3. Объединенный экстракт отмывают от щелочи три - четыре раза порциями воды 50 - 150 см3 до исчезновения щелочной реакции промывных вод (по универсальной индикаторной бумаге).
Для удаления воды экстракт фильтруют через фильтр с 2 - 5 г безводного сульфата натрия. Далее экстракт упаривают досуха, используя роторный испаритель и перерастворяют в н-гексане. При необходимости раствор можно использовать для последующего разведения.
8.2.6 Раствор, полученный по 8.2.3 (8.2.4, 8.2.5) анализируют методом НФ ВЭЖХ. Для анализа методом ОФ ВЭЖХ аликвоту гексанового раствора упаривают в токе азота и сухой остаток перерастворяют в элюенте для ОФ ВЭЖХ. Навеску испытуемого материала и объем растворителя подбирают таким образом, чтобы массовая концентрация токоферолов в анализируемом растворе находилась в диапазоне, соответствующем диапазону массовых концентраций рабочих растворов стандартных веществ, используемых при построении градуировочного графика по 8.4.
8.3 Подготовка жидкостного хроматографа
Подготовку жидкостного хроматографа к работе осуществляют в соответствии с инструкцией по эксплуатации оборудования. Перед началом работы колонку промывают элюентом.
8.4 Построение градуировочной зависимости
Процедуры построения градуировочной зависимости выполняют в соответствии с руководством по эксплуатации оборудования и руководством пользователя по программному обеспечению. Проводят хроматографический анализ не менее четырех рабочих растворов витамина Е, приготовленных по 8.1.2.
Градуировочный график строят в координатах "аналитический сигнал" - "массовая концентрация витамина в градуировочном растворе, мкг/см3". Для каждого анализируемого раствора проводят два параллельных измерения и находят среднеарифметическое значение. Различие между измеренными значениями аналитических сигналов и времени удерживания не должно превышать 5% от средних значений. Линейные участки градуировочного графика должны соответствовать всему диапазону определяемых концентраций витамина Е. Коэффициент градуировочного графика (kгр, мкг/см3/(mAU·c) или мкг/см3/(AU·c)) определяют как среднеарифметическое значение коэффициентов ki, вычисляемых по формуле
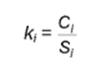 ,
,
(2)
где Ci - массовая концентрация стандартных веществ в i-м градуировочном растворе, мкг/см3;
Si - площадь аналитического сигнала при анализе i-го градуировочного раствора, mAU·c или AU·c.
Правильность построения градуировочной зависимости контролируется величиной достоверной аппроксимации R2≥0, 997.
Градуировка проводится в следующих случаях: на этапе освоения метода, при изменении условий хроматографического анализа или при выявлении несоответствия метрологическим требованиям результатов оперативного контроля или внутреннего аудита.
9 Выполнение измерений
В колонку хроматографа последовательно вводят равные объемы испытуемого и градуировочного растворов. В качестве градуировочного выбирают раствор, высота пика которого наименее отличается от высоты пика испытуемого раствора. Концентрацию витамина Е (Cгр) в растворе, используемом для градуировки, уточняют в день его использования по 8.1.1.3.
Для идентификации пиков сопоставляют время удерживания α -, β -, γ - и δ -токоферолов, ацетата α -токоферола испытуемого раствора и раствора стандарта, а также добавляют к испытуемому раствору раствор стандарта с близким содержанием соответствующего токоферола.
10 Обработка и оформление результатов
Массовую долю α -, β-, γ - и δ -токоферолов, ацетата α -токоферола X, млн-1, вычисляют с использованием градуировочной зависимости по формуле
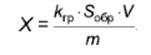 ,
,
(3)
где kгр - коэффициент градуировочного графика по 8.4;
Sобр - среднеарифметическое значение результатов измерений площади пика анализируемого компонента для двух параллельных хроматографических анализов испытуемого раствора, mAU·c или AU·c;
V - объем разведения, см3;
m - масса анализируемой пробы, г.
С использованием градуировочного раствора
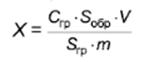 ,
,
(4)
где Cгр - массовая концентрация градуировочного раствора, мкг/см3;
Sгр - среднеарифметическое значение результатов измерений площади (высоты) пика анализируемого компонента для двух параллельных хроматографических анализов градуировочного раствора, мм2 (мм).
Результат вычисляют до второго десятичного знака и округляют до первого десятичного знака.
При анализе каждой пробы выполняют два параллельных определения, начиная со взятия навески испытуемой пробы.
Расхождение между результатами двух параллельных измерений X1, X2 (в процентах от среднего значения Хср), выполненными одним оператором с использованием идентичных реактивов и оборудования и в минимально возможный промежуток времени, не должно превышать r (предел повторяемости приведен в таблице 3) с доверительной вероятностью Р = 95%.
При соблюдении этого условия за окончательный результат испытания принимают среднеарифметическое значение Хср.
Границы относительной погрешности определения массовой доли витамина Е (±δ), в процентах от результата испытания, и при доверительной вероятности Р = 95% не должны превышать значений, указанных в таблице 3.
Результат определения витамина Е представляют в следующем виде:
Хср±Δ, млн-1, Р=95%,
(5)
где Хср - среднеарифметическое значение результатов двух параллельных определений, млн-1;
Δ - значение границы абсолютной погрешности определений, млн-1, вычисляемое по формуле
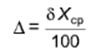 .
.
(6)
Результаты испытаний заносят в протокол, в котором указывают:
- ссылку на настоящий стандарт;
- вид, происхождение и название пробы;
- способ и дату отбора пробы;
- дату поступления и испытания пробы;
- результаты исследования;
- причины отклонений в процедуре определения от установленных условий.
11 Метрологические характеристики метода
11.1 Повторяемость
Каждую пробу анализируют дважды, начиная со взятия навески испытуемой пробы. Расхождение между результатами двух параллельных измерений (X1, X2), выполненными одним оператором с использованием идентичных реактивов и оборудования и в минимально возможный промежуток времени, считают удовлетворительным, если |X1 - X2|≤0, 01·r·Хср, где Хср - среднеарифметическое значение. Значение r (предел повторяемости) приведено в таблице 3.
При превышении норматива оперативного контроля сходимости испытание повторяют. При повторном превышении указанного норматива выясняют причины, приводящие к неудовлетворительным результатам, и устраняют их.
11.2 Воспроизводимость
Пробу делят на две равные части. Расхождение между результатами двух определений (X1, X2), выполненными разными операторами в разное время с использованием различных реактивов и оборудования, считают удовлетворительным, если |X1-X2|≤0, 01·R·X, где Х - среднеарифметическое значение. Значение R (предел воспроизводимости) приведено в таблице 3.
Таблица 3 - Метрологические характеристики
|
Метрологическая характеристика (Р = 0, 95)
|
Диапазон измерений массовой доли, млн-1
|
|
от 5 до 100 включ.
|
св. 100 до 500 включ.
|
|
Стандартное отклонение повторяемости sr, %
|
5, 4
|
4, 3
|
|
Предел повторяемости r, %
|
15
|
12
|
|
Стандартное отклонение воспроизводимости sR, %
|
8, 9
|
7, 1
|
|
Предел воспроизводимости R, %
|
25
|
20
|
|
Границы относительной погрешности (±δ), %
|
20
|
15
|
|
Предел обнаружения, млн-1
|
1
|
При превышении норматива оперативного контроля воспроизводимости испытание повторяют. При повторном превышении указанного норматива выясняют причины, приводящие к неудовлетворительным результатам, и устраняют их.
11.3 Контроль погрешности результатов испытаний
Контроль погрешности (точности) результатов испытаний проводят методом добавок. Пробу делят на две равные части. В одну из них добавляют стандарт витамина Е в количестве, составляющем 50% - 150% от исходного содержания компонента в пробе, и проводят испытания в соответствии с настоящим стандартом.
Результаты испытаний признают удовлетворительными, если погрешность определения массовой доли витамина Е в добавке не превышает норматива оперативного контроля погрешности Кдоб, млн-1:
|Хдоб-Хср-сдоб|≤Кдоб,
(7)
где Хдоб - среднеарифметическое значение результатов двух испытаний пробы с добавкой, млн-1;
Хср - среднеарифметическое значение результатов двух испытаний пробы без внесения добавки, млн-1.
сдоб - массовая доля добавки, млн-1.
При проведении внутрилабораторного контроля значение Кдоб рассчитывают (при доверительной вероятности 90%) по формуле
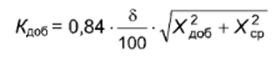 ,
,
(8)
где δ - значение границы относительной погрешности определения массовой доли витамина Е, указанное в таблице 3.
При проведении внешнего контроля значение Кдоб рассчитывают (при доверительной вероятности 95%) по формуле
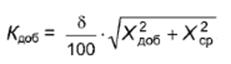 .
.
(9)
11.4 Контроль стабильности результатов измерений при реализации методики в лаборатории
Контроль стабильности результатов измерений в лаборатории осуществляют в соответствии с требованиями ГОСТ Р ИСО 5725-6, используя метод контроля стабильности стандартного отклонения промежуточной прецизионности по ГОСТ Р ИСО 5725-6 (пункт 6.2.3) с применением контрольных карт Шухарта. Периодичность контроля и процедуры контроля стабильности результатов измерений должны быть предусмотрены в руководстве по качеству лаборатории в соответствии с ГОСТ Р ИСО/МЭК 17025 (подраздел 4.2) и ГОСТ Р 8.563 (пункт 7.1.1).
Библиография
|
[1]
|
ПВ 10-115-96
|
Правила устройства и безопасной эксплуатации сосудов, работающих под давлением
|
|
[2]
|
ГФ СССР X, ст. 34
|
Эфир медицинский
|
|
[3]
|
ГФ СССР Х, ст. 6
|
Кислота аскорбиновая (витамин С)
|
|
[4]
|
ФС 42-2668-95
|
Кислота аскорбиновая (витамин С)
|
|
[5]
|
ФС 42-2495-87
|
Токоферола ацетат
|
|
[7]
|
ГФ СССР X, ст. 695
|
Токоферола ацетат (витамина Е ацетат)
|
![]() — Все документы — ГОСТы — ГОСТ Р 54634-2011 ПРОДУКТЫ ПИЩЕВЫЕ ФУНКЦИОНАЛЬНЫЕ. МЕТОД ОПРЕДЕЛЕНИЯ ВИТАМИНА Е
— Все документы — ГОСТы — ГОСТ Р 54634-2011 ПРОДУКТЫ ПИЩЕВЫЕ ФУНКЦИОНАЛЬНЫЕ. МЕТОД ОПРЕДЕЛЕНИЯ ВИТАМИНА Е Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
 Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
 «МК»: в России не отменят льготную ипотеку
«МК»: в России не отменят льготную ипотеку
 Аренда квартир в Москве подешевела на 10 %
Аренда квартир в Москве подешевела на 10 %
 Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
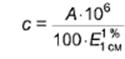 ,
,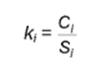 ,
,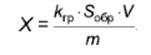 ,
,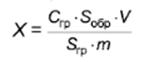 ,
,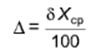 .
.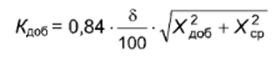 ,
,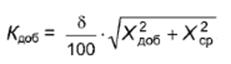 .
.