Введен в действие приказом Федерального агентства по техническому регулированию и метрологии от 25 августа 2017 г. N 963-ст
Межгосударственный стандарт ГОСТ 34133-2017
"МЯСО И МЯСНЫЕ ПРОДУКТЫ. МЕТОД ОПРЕДЕЛЕНИЯ АСКОРБИНОВОЙ КИСЛОТЫ И АСКОРБАТОВ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИЕЙ"
Meat and meat products. Method for determination of ascorbic acid and ascorbates by high performance liquid chromatography
МКС 67.120.10
Дата введения - 1 июля 2018 г.
Введен впервые
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2015 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 Разработан Федеральным государственным бюджетным научным учреждением "Всероссийский научно-исследовательский институт мясной промышленности имени В.М. Горбатова" (ФГБНУ "ВНИИМП им. В.М. Горбатова")
2 Внесен Федеральным агентством по техническому регулированию и метрологии
3 Принят Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 14 июля 2017 г. N 101-П)
За принятие проголосовали:
|
Краткое наименование страны по МК (ИСО 3166) 004-97
|
Код страны по МК (ИСО 3166) 004-97
|
Сокращенное наименование национального органа по стандартизации
|
|
Армения
|
AM
|
Минэкономики Республики Армения
|
|
Беларусь
|
BY
|
Госстандарт Республики Беларусь
|
|
Казахстан
|
KZ
|
Госстандарт Республики Казахстан
|
|
Киргизия
|
KG
|
Кыргызстандарт
|
|
Россия
|
RU
|
Росстандарт
|
|
Узбекистан
|
UZ
|
Узстандарт
|
|
Украина
|
AU
|
Минэкономразвития Украины
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 25 августа 2017 г. N 963-ст межгосударственный стандарт ГОСТ 34133-2017 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2018 г.
5 Введен впервые
1 Область применения
Настоящий стандарт распространяется на мясо, включая мясо птицы, субпродукты, мясные и мясосодержащие продукты, и устанавливает метод определения массовой доли аскорбиновой кислоты и аскорбатов (аскорбат натрия Е301, аскорбат калия Е303, аскорбат кальция Е302) с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) в ультрафиолетовой (УФ) области спектра при определенной (заданной) длине волны.
Диапазон измерений массовой доли аскорбиновой кислоты и аскорбатов составляет от 0, 01 % до 0, 50 %.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79* Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
──────────────────────────────
* В Российской Федерации действует ГОСТ Р 12.1.019-2009 "Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты".
ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ ISO 3696-2013** Вода для лабораторного анализа. Технические требования и методы контроля
──────────────────────────────
** В Российской Федерации действует ГОСТ Р 52501-2005 (ИСО 3696:1987) "Вода для лабораторного анализа. Технические условия".
ГОСТ 4025-95 Мясорубки бытовые. Технические условия
ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
ГОСТ ИСО 5725-2-2003* Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
ГОСТ ИСО 5725-6-2003** Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
──────────────────────────────
* В Российской Федерации действует ГОСТ Р ИСО 5725-2-2002 "Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений".
** В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002 "Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике".
ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 7269-2015 Мясо. Методы отбора образцов и органолептические методы определения свежести
ГОСТ 9792-73 Колбасные изделия и продукты из свинины, баранины, говядины и мяса других видов убойных животных и птиц. Правила приемки и методы отбора проб
ГОСТ 20469-95 Электромясорубки бытовые. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26272-98 Часы электронно-механические кварцевые наручные и карманные. Общие технические условия
ГОСТ 26678-85 Холодильники и морозильники бытовые электрические компрессионные параметрического ряда. Общие технические условия
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31467-2012 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 супернатант: Жидкость, располагающаяся над твердым слоем (осадком, седиментом) после центрифугирования пробы.
3.2 гомогенат: Однородная (гомогенная) смесь пробы с экстрагирующим раствором, полученная после механического измельчения пробы на гомогенизаторе.
3.3 аналит: Вещество, определяемое в пробе объекта аналитического контроля.
4 Сущность метода
Метод основан на экстракции аскорбиновой кислоты и аскорбатов из тщательно гомогенизированной пробы водным раствором трихлоруксусной кислоты, центрифугировании с осаждением белков и последующем анализе методом высокоэффективной жидкостной хроматографии в ультрафиолетовой (УФ) области спектра. Идентификацию аскорбиновой кислоты и аскорбатов осуществляют по абсолютному времени удерживания, массовую долю определяют по площади хроматографического пика анализируемого образца, сопоставляя с пиком образца сравнения с заведомо известной концентрацией.
5 Требования безопасности
5.1 При подготовке и проведении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007.
5.2 Помещение, в котором проводят измерения, должно быть оснащено приточно-вытяжной вентиляцией. Работу необходимо проводить, соблюдая правила личной гигиены и противопожарной безопасности, в соответствии с требованиями ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
5.3 При работе с электроприборами необходимо соблюдать требования безопасности по ГОСТ 12.1.019.
6 Средства измерений, вспомогательное оборудование, материалы и реактивы
Хроматограф жидкостный высокоэффективный, укомплектованный:
- детектором УФ, обеспечивающим измерения при длине волны 245 нм, с относительной погрешностью спектрофотометрического определения не более ± 2 %;
- градиентным насосом;
- хроматографической колонкой для ВЭЖХ длиной 150-250 мм и диаметром 2, 1-4, 6 мм с обращенной фазой С18 либо С16, размером частиц 3, 5-5 мкм, имеющей эффективность не менее 5000 теоретических тарелок по пику аскорбиновой кислоты;
- блоком термостатирования колонок с поддержанием температуры 30 °С с точностью ± 0, 1 °С;
- записывающим устройством с компьютерным управлением и автоматической программой обработки хроматографических данных в соответствии с комплектацией хроматографа.
Весы неавтоматического действия по ГОСТ OIML R 76-1 специального или высокого класса точности или весы лабораторные по нормативным документам, действующим на территории государства, принявшего стандарт, с пределами допускаемой абсолютной погрешности не более ± 0, 1 мг.
Мясорубка бытовая по ГОСТ 4025 или электромясорубка бытовая по ГОСТ 20469.
рН-метр со стеклянным и хлорсеребряным электродами (или комбинированным стеклянным электродом) с диапазоном измерений от 0 до 14 ед. рН с пределом допускаемой абсолютной погрешности не более ± 0, 01 ед. рН.
Гомогенизатор лабораторный, с частотой вращения ротора не менее 10000 об/мин.
Холодильник бытовой электрический по ГОСТ 26678.
Баня ультразвуковая лабораторная с регулятором времени.
Часы электронно-механические по ГОСТ 26272.
Центрифуга лабораторная, с центробежным ускорением 4000 g.
Банки стеклянные вместимостью 250-500 см3 с крышкой.
Пипетки градуированные 1-2-1-5, 1-2-1-10 по ГОСТ 29227 или дозаторы автоматические с переменным объемом дозирования и относительной погрешностью дозирования не более ± 1 %.
Пробирки центрифужные из полипропилена вместимостью 50 см3.
Фильтр мембранный из политетрафторэтилена с диаметром пор 0, 45 мкм.
Колбы мерные 2-50-2, 2-100-2, 2-1000-2 по ГОСТ 1770.
Колба коническая Кн-1-100-24/29 ТС по ГОСТ 25336.
Пипетки градуированные 1-2-1-5 по ГОСТ 29227.
Флаконы - виалы хроматографические из темного стекла вместимостью 2, 0 см3.
Вода дистиллированная по ГОСТ 6709 или вода для лабораторного анализа по ГОСТ ISO 3696 первой степени очистки.
Ацетонитрил для хроматографии, х. ч.
Калий фосфорнокислый однозамещенный по ГОСТ 4198, х. ч.
Кислота ортофосфорная по ГОСТ 6552, х. ч.
Кислота трихлоруксусная с содержанием основного вещества не менее 99, 0 %.
Кислота аскорбиновая с содержанием основного вещества не менее 99, 5 %.
Допускается применение других средств измерений с метрологическими характеристиками, вспомогательного оборудования с техническими характеристиками не ниже, а также реактивов по качеству не ниже указанных в настоящем стандарте.
7 Отбор и подготовка проб
7.1 Отбор проб - по ГОСТ 7269, ГОСТ 9792, ГОСТ 31467.
7.2 Пробу измельчают, дважды пропуская через мясорубку с диаметром отверстий решетки 2-4 мм, и тщательно перемешивают.
7.3 Подготовленную пробу помещают в стеклянную банку вместимостью 250-500 см3 и закрывают крышкой.
Допускается хранить подготовленную пробу в замороженном состоянии при температуре от минус 25 °С до минус 18 °С не более 7 сут.
8 Подготовка к измерению
8.1 Приготовление градуировочных растворов
Для определения массовой доли аскорбиновой кислоты и аскорбатов готовят градуировочные растворы аскорбиновой кислоты массовой концентрации 1 мг/см3 (раствор 1), 0, 5 мг/см3 (раствор 2), 0, 2 мг/см3 (раствор 3), 0, 1 мг/см3 (раствор 4), 0, 02 мг/см3 (раствор 5).
Для приготовления раствора 1 взвешивают 100 мг аскорбиновой кислоты, переносят в мерную колбу вместимостью 100 см3, добавляют 70-80 см3 дистиллированной воды, тщательно перемешивают до полного растворения и доводят объем до метки дистиллированной водой.
Для приготовления раствора 2 градуированной пипеткой в мерную колбу вместимостью 100 см3 отбирают 10 см3 раствора 1 и разбавляют 10 см3 дистиллированной воды.
Для приготовления раствора 3 градуированной пипеткой отбирают 10 см3 раствора 1, переносят в мерную колбу вместимостью 50 см3 и доводят объем до метки дистиллированной водой.
Для приготовления раствора 4 градуированной пипеткой отбирают 5 см3 раствора 1, переносят в мерную колбу вместимостью 50 см3 и доводят объем до метки дистиллированной водой.
Для приготовления раствора 5 градуированной пипеткой отбирают 10 см3 раствора 4, переносят в мерную колбу вместимостью 50 см3 и доводят объем до метки дистиллированной водой.
Растворы используют свежеприготовленными.
8.2 Приготовление растворов
8.2.1 Приготовление 2 %-ного раствора трихлоруксусной кислоты
Взвешивают 2, 0 г трихлоруксусной кислоты, переносят в мерную колбу вместимостью 100 см3, растворяют в дистиллированной воде и доводят объем до метки.
Раствор хранят в колбе с притертой пробкой при комнатной температуре не более 1 мес.
8.2.2 Приготовление подвижной фазы хроматографической системы
В качестве подвижной фазы используют буферный раствор фосфорнокислого калия однозамещенного молярной концентрации с (KН2РO4) = 0, 025 моль/дм3 с рН = 3, 4 ед. рН (фосфатный буфер).
Для приготовления фосфатного буфера взвешивают 3, 4 г фосфорнокислого калия однозамещенного, переносят в мерную колбу вместимостью 1000 см3, доводят объем до метки дистиллированной водой и тщательно перемешивают до полного растворения. С помощью градуированной пипетки добавляют по каплям ортофосфорную кислоту, доводя рН до 3, 4 ед. рН и контролируя рН-метром. Перед использованием раствор дегазируют на ультразвуковой бане в течение 10-15 мин.
Раствор хранят в колбе с притертой пробкой при комнатной температуре не более 7 сут.
8.3 Подготовка пробы
Пробу массой 10 г взвешивают с точностью до второго десятичного знака, помещают в центрифужную пробирку вместимостью 50 см3. Добавляют 30 см3 2 %-ного раствора трихлоруксусной кислоты и тщательно перемешивают. Гомогенат ставят на ультразвуковую баню при температуре 20 °С на 15 мин. Затем центрифугируют 5 мин с центробежным ускорением 4000 g. Полученный супернатант пропускают через мембранный фильтр с диаметром пор 0, 45 мкм в хроматографическую виалу вместимостью 2 см3.
9 Проведение измерений
9.1 Условия проведения измерений подбирают в зависимости от вида применяемого жидкостного хроматографа и хроматографической колонки.
Проводят градуировку хроматографа с помощью градуировочных растворов, далее проводят измерения анализируемой пробы.
В качестве примера могут быть приведены следующие условия хроматографического определения аскорбиновой кислоты и аскорбатов, выполненного на жидкостном хроматографе с хроматографической колонкой типа С18 4, 6 х 150 мм, 5 мкм:
Подвижная фаза: фосфатный буфер (рН = 3, 4 ед. рН), ацетонитрил, вода.
Перед введением пробы колонку кондиционируют 4 мин фосфатным буфером (рН = 3, 4 ед. рН) в соотношении с водой - 35:65 соответственно.
0, 02 см3 анализируемой пробы вводят в подготовленный к работе жидкостный хроматограф и записывают хроматограмму в следующих условиях.
Градиентные условия элюирования: в течение 16 мин ацетонитрил от 0 % до 30 %, вода от 65 % до 35 %, фосфатный буфер (рН = 3, 4 ед. рН) - 35 %.
Скорость подачи элюента 1, 0 см3/мин.
Температура колонки 30 °С.
Длина волны детектирования - 245 нм.
Хроматограмма аскорбиновой кислоты с концентрацией 0, 2 мг/см3 приведена в приложении А.
9.2 Идентификацию пиков хроматограммы анализируемой пробы проводят сравнением с хроматограммой градуировочного раствора по двум параметрам: времени удерживания и спектральному отношению R (отношение высот хроматографического пика на разных длинах волн 210 и 245 нм).
9.3 Если время удерживания и спектральные отношения пиков хроматограммы анализируемой пробы совпадают в пределах допускаемых отклонений (∆R ≤ 0, 05, ∆tR ≤ 3 %) с временем удерживания и спектральными отношениями соответствующих им пиков хроматограммы градуировочного раствора, результат идентификации считают положительным.
9.4 Если спектральные отношения совпадают в пределах допускаемого отклонения, а разница времени удерживания пиков хроматограммы анализируемой пробы и хроматограммы градуировочного раствора больше допускаемого отклонения, проводят хроматографический анализ соответствующего градуировочного раствора по 8.1 и сравнивают время удерживания. В случае совпадения в дальнейшем в качестве образца используют новую хроматограмму.
В случае повторного несовпадения времени удерживания используют метод добавок, для чего к анализируемой пробе добавляют известные количества определяемой аскорбиновой кислоты с концентрацией, сравнимой с концентрацией "сомнительных" пиков, и анализируют по 9.1.
Если на хроматограмме пробы с добавкой площади "сомнительных" пиков увеличились на величину, соответствующую величине добавки, эти пики относятся к определяемым компонентам.
Если на хроматограмме пробы с добавкой наряду с "сомнительными" пиками присутствуют пики, время удерживания и спектральные отношения которых совпадают с соответствующими параметрами добавленных веществ, сомнительные пики не относятся к определяемым компонентам.
9.5 Если время удерживания соответствующих пиков хроматограммы анализируемого раствора и хроматограммы градуировочного раствора совпадают в пределах допускаемого отклонения, а разница спектральных отношений больше допускаемого отклонения, не допускается использовать результаты анализа данной пробы.
9.6 Концентрация аскорбиновой кислоты и аскорбатов в анализируемой пробе не должна превышать предельных значений концентраций градуировочных растворов. В случае превышения анализируемую пробу, содержащую аскорбиновую кислоту и аскорбаты, с помощью механического дозатора разбавляют дистиллированной водой в рассчитанное количество раз и проводят хроматографический анализ разбавленных растворов. Если массовая концентрация аскорбиновой кислоты и аскорбатов в анализируемой пробе ниже предельного значения градуировочного раствора, необходимо увеличить массу пробы.
10 Обработка результатов
10.1 В соответствии с данными, полученными при анализе градуировочных растворов, создают таблицу пиков с использованием программного обеспечения хроматографа. Расчеты площадей пиков и массовых долей аскорбиновой кислоты и аскорбатов выполняются системой обработки данных в автоматическом режиме.
10.2 Массовую долю аскорбиновой кислоты X1, %, рассчитывают по формуле
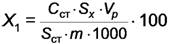
,
(1)
где Сст - концентрация аскорбиновой кислоты в градуировочном растворе, мг/см3;
Sx - площадь пика аскорбиновой кислоты и аскорбатов в анализируемой пробе, усл. ед.;
Vp - объем экстрагирующей смеси (2 %-ный раствор трихлоруксусной кислоты, приготовленный по 8.2.1), см3;
Sст - площадь пика аскорбиновой кислоты в градуировочном растворе, усл. ед.;
m - масса анализируемой пробы, г;
100 - коэффициент пересчета в проценты;
1000 - коэффициент пересчета из мг в г.
10.3 Массовую долю аскорбатов Х2, %, рассчитывают по формуле
X2=X1·K,
(2)
где X1 - массовая доля аскорбиновой кислоты, %;
K - коэффициент пересчета значения аскорбиновой кислоты на ее соли:
K = 1, 125 - для аскорбата натрия;
K = 1, 216 - для аскорбата калия;
K = 1, 108 - для аскорбата кальция.
За окончательный результат принимают среднеарифметическое значение результатов двух параллельных измерений, округленное до второго десятичного знака.
11 Метрологические характеристики
11.1 Метрологические характеристики метода при доверительной вероятности Р = 0, 95 приведены в таблице 1.
Таблица 1
|
Наименование показателя
|
Границы относительной погрешности ±δ, %
|
Предел повторяемости r, %
|
Предел воспроизводимости R, %
|
|
Массовая доля аскорбиновой кислоты и аскорбатов в диапазоне измерений от 0, 01 % до 0, 50 %
|
15
|
0, 12хср
|
0, 20Хср
|
|
Примечание - хср - среднеарифметическое значение результатов двух параллельных измерений, %.
Хср - среднеарифметическое значение результатов двух измерений, выполненных в разных лабораториях, %.
|
11.2 Расхождение между результатами двух параллельных измерений, выполненных одним оператором при анализе одной и той же пробы с использованием одних и тех же средств измерений и реактивов, не должно превышать предела повторяемости (сходимости) r, значения которого приведены в таблице 1.
Условия приемлемости результатов измерений, полученных в условиях повторяемости, при доверительной вероятности Р = 0, 95, должны удовлетворять условию
|x1-x2|≤r,
(3)
где x1 и x2 - результаты двух параллельных измерений, %;
r - предел повторяемости, %.
11.3 Расхождение между результатами двух измерений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости R, значения которого приведены в таблице 1.
Условия приемлемости результатов измерений, полученных в условиях воспроизводимости, при доверительной вероятности Р = 0, 95, должны удовлетворять условию
|X1-X2|≤R,
(4)
где X1 и X2 - результаты двух определений, выполненных в разных лабораториях, %;
R - предел воспроизводимости, %.
11.4 Границы относительной погрешности, находящиеся с доверительной вероятностью Р = 0, 95, при соблюдении условий настоящего стандарта не должны превышать значений, приведенных в таблице 1.
12 Контроль точности результатов измерений
12.1 Процедуру контроля стабильности результатов измерений (повторяемости, промежуточной прецизионности и погрешности) проводят в соответствии с порядком, установленным в лаборатории, по ГОСТ ИСО 5725-6.
12.2 Проверку приемлемости результатов измерений, полученных в условиях повторяемости (сходимости), осуществляют в соответствии с требованиями ГОСТ ИСО 5725-2. Расхождение между результатами измерений не должно превышать предела повторяемости (r). Значения r приведены в таблице 1.
12.3 Проверку приемлемости результатов измерений, полученных в условиях воспроизводимости, проводят с учетом требований ГОСТ ИСО 5725-2. Расхождение между результатами измерений, полученными двумя лабораториями, не должно превышать предела воспроизводимости (R). Значения R приведены в таблице 1.
Приложение А
(справочное)
Хроматограмма аскорбиновой кислоты с концентрацией 0, 2 мг/см3
А.1 Хроматограмма аскорбиновой кислоты с концентрацией 0, 2 мг/см3 приведена на рисунке А.1.
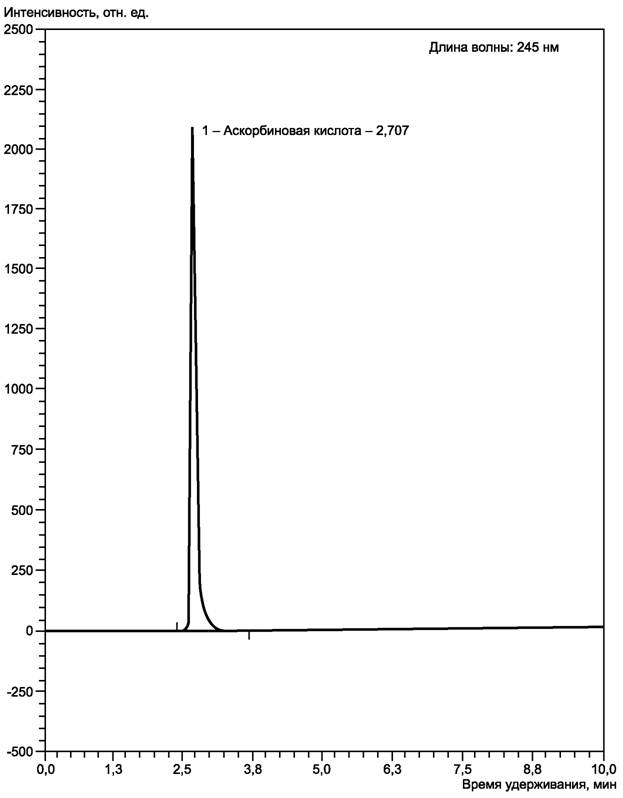
Рисунок А.1 - Хроматограмма аскорбиновой кислоты с концентрацией 0, 2 мг/см3, 2, 707 мин - пик аскорбиновой кислоты
![]() — Все документы — ГОСТы — ГОСТ 34133-2017 МЯСО И МЯСНЫЕ ПРОДУКТЫ. МЕТОД ОПРЕДЕЛЕНИЯ АСКОРБИНОВОЙ КИСЛОТЫ И АСКОРБАТОВ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИЕЙ
— Все документы — ГОСТы — ГОСТ 34133-2017 МЯСО И МЯСНЫЕ ПРОДУКТЫ. МЕТОД ОПРЕДЕЛЕНИЯ АСКОРБИНОВОЙ КИСЛОТЫ И АСКОРБАТОВ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИЕЙ Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
 Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
 «МК»: в России не отменят льготную ипотеку
«МК»: в России не отменят льготную ипотеку
 Аренда квартир в Москве подешевела на 10 %
Аренда квартир в Москве подешевела на 10 %
 Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
