Введен в действие приказом Федерального агентства по техническому регулированию и метрологии от 21 июля 2015 г. N 949-ст
Межгосударственный стандарт ГОСТ EN 15607-2015
"ПРОДУКТЫ ПИЩЕВЫЕ. ОПРЕДЕЛЕНИЕ D-БИОТИНА МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ"
Foodstuffs. Determination of D-biotin by high performance liquid chromatography
Дата введения - 1 января 2017 г.
Введен впервые
Предисловие
Цели, основные принципы и порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 Подготовлен Открытым акционерным обществом "Всероссийский научно-исследовательский институт сертификации" на основе аутентичного перевода на русский язык европейского регионального стандарта, указанного в пункте 5
2 Внесен Федеральным агентством по техническому регулированию и метрологии (Росстандарт)
3 Принят Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 29 мая 2015 г. N 77)
За принятие проголосовали:
|
Краткое наименование страны по МК (ИСО 3166) 004-97
|
Код страны по МК (ИСО 3166) 004-97
|
Сокращенное наименование национального органа по стандартизации
|
|
Армения
Беларусь
Казахстан
Киргизия
Молдова
Россия
Таджикистан
Украина
|
AM
BY
KZ
KG
MD
RU
TJ
UA
|
Минэкономики Республики Армения
Госстандарт Республики Беларусь
Госстандарт Республики Казахстан
Кыргызстандарт
Молдова-Стандарт
Росстандарт
Таджикстандарт
Минэкономразвития Украины
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 21 июля 2015 г. N 949-ст межгосударственный стандарт ГОСТ EN 15607-2015 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2017 г.
5 Настоящий стандарт идентичен европейскому региональному стандарту EN 15607:2009 Foodstuffs - Determination of D-biotin by HPLC (Продукты пищевые. Определение D-биотина высокоэффективной жидкостной хроматографией).
Европейский региональный стандарт разработан техническим комитетом CEN/TC 275 "Анализ пищевых продуктов. Горизонтальные методы", секретариатом которого является DIN (Германия).
Перевод с немецкого языка (de).
Официальные экземпляры европейского регионального стандарта, на основе которого подготовлен настоящий межгосударственный стандарт, и европейского регионального стандарта, на который дана ссылка, имеются в Федеральном информационном фонде технических регламентов и стандартов.
Сведения о соответствии межгосударственных стандартов ссылочным европейским региональным стандартам приведены в дополнительном приложении ДА.
Степень соответствия - идентичная (IDT)
6 Введен впервые
1 Область применения
Настоящий стандарт устанавливает метод определения содержания D-биотина в пищевых продуктах методом высокоэффективной жидкостной хроматографии (ВЭЖХ). Метод прошел валидацию при межлабораторных сравнительных испытаниях с использованием как обогащенных проб, так и проб с естественным содержанием D-биотина, а именно концентратов типа сухого завтрака - мюсли, сухого молока для грудных детей, лиофилизированных зеленых овощей с ветчиной, лиофилизированного куриного бульона и обогащенного апельсинового сока в диапазоне значений содержания D-биотина от 16 до 200 мкг/100 г (см. приложение В).
Примечания
1 Настоящим методом может также определяться D-биоцитин, хотя ни в одной из проб, использовавшихся при межлабораторных сравнительных испытаниях, D-биоцитин не содержался. Тем не менее открываемость как D-биотина, так и D-биоцитина превышает 90% (см. [2] и [3]).
2 При анализе проб, содержащих куриные яйца, метод приводит к заниженным значениям содержания D-биотина.
2 Нормативные ссылки
Приведенные ниже ссылочные нормативные документы являются обязательными для применения настоящего стандарта. Для датированных ссылок применимо только цитируемое издание. В случае недатированных ссылок используют последнее издание документа, включая все изменения.
EN ISO 3696 Water for analytical laboratory use - Specification and test methods (ISO 3696:1987) (Вода для лабораторного анализа. Технические требования и методы испытаний)
3 Сущность метода
Метод основан на выделении D-биотина из проб пищевых продуктов обработкой ферментами и количественном определении методом ВЭЖХ с послеколоночной дериватизацией ([2], [3]).
Комплексообразование D-биотина с белком авидином является весьма специфическим. Поэтому авидин, ковалентно связанный с флуоресцентной меткой - флуоресцеин-5-изотиоцианитом, используется в качестве реагента для послеколоночной дериватизации D-биотина ([4], [5]).
4 Реактивы
4.1 Общие положения
Если не указано иное, то при анализе используют только реактивы гарантированной чистоты и воды, по крайней мере, степени чистоты 1 по EN ISO 3696 или повторно перегнанную дистиллированную воду.
4.2 Требования к химическим реактивам и приготовление растворов
4.2.1 Метанол для ВЭЖХ, массовая доля основного вещества w(CH3OH) не менее 99, 8%.
4.2.2 Раствор серной кислоты молярной концентрации c(H2SO4) = 1 моль/дм3.
4.2.3 Раствор серной кислоты молярной концентрации c(H2SO4) = 1, 5 моль/дм3.
4.2.4 Лимонная кислота моногидрат, массовая доля основного вещества w(C6H8O7·H2O) не менее 99, 7%.
4.2.5 Гидрофосфат натрия 2-водный, массовая доля основного вещества w(Na2HPO4·2H2O) не менее 99, 8%.
4.2.6 Глутатион, массовая доля основного вещества w(C10H17N3O6S) не менее 98%.
4.2.7 Этилендиаминтетраацетат натрия (ЭДТА) 2-водный, массовая доля основного вещества w(C10H14N2Na2O8·2H2O) не менее 99%.
4.2.8 Гидрофосфат калия, массовая доля основного вещества w(K2HPO4) не менее 96%.
4.2.9 Дигидрофосфат калия, массовая доля основного вещества w(K2HPO4) не менее 99, 5%.
4.2.10 Приготовление цитратного буферного раствора
0, 462 г моногидрата лимонной кислоты (4.2.4) и 1, 05 г гидрофосфата натрия 2-водного (4.2.5) растворяют в 450 см3 дистиллированной воды. Устанавливают значение рН раствора, равное 5, 7, при помощи раствора серной кислоты (4.2.3) и затем разбавляют раствор до объема 500 см3.
Срок хранения раствора - 1 день.
4.2.11 Приготовление раствора глутатиона массовой концентрации ρ(C10H17N3O6S) = 10 г/дм3
30 мг глутатиона (4.2.6) растворяют в 3 см3 дистиллированной воды.
Срок хранения раствора - 1 день.
4.2.12 Приготовление раствора ЭДТА массовой концентрации ρ(C10H14N2Na2O8·2H2O) = 10 г/дм3
0, 1 г ЭДТА (4.2.7) растворяют в 10 см3 дистиллированной воды.
Срок хранения раствора - 1 день.
4.2.13 Приготовление раствора гидрофосфата калия молярной концентрации c(K2HPO4) = 0, 1 моль/дм3
17, 4 г гидрофосфата калия (4.2.8) растворяют в 1000 см3 воды.
Срок хранения раствора - 2 дня.
4.2.14 Приготовление раствора дигидрофосфата калия молярной концентрации с(K2HPO4) = 0, 1 моль/дм3
13, 6 г дигидрофосфата калия (4.2.9) растворяют в 1000 см3 воды.
Срок хранения раствора - 2 дня.
4.2.15 Приготовление фосфатного буферного раствора с рН 6, 0
Растворы гидрофосфата калия (4.2.13) и дигидрофосфата калия (4.2.14) смешивают в такой пропорции, чтобы значение рН приготовленного раствора составляло 6, 0 (например, 30 объемных частей раствора по 4.2.13 и 70 объемных частей раствора по 4.2.14).
Срок хранения раствора - 7 дней при комнатной температуре.
4.2.16 Приготовление фосфатного буферного раствора с рН 7, 0
Растворы гидрофосфата калия (4.2.13) и дигидрофосфата калия (4.2.14) смешивают в такой пропорции, чтобы значение рН приготовленного раствора составляло 7, 0 (например, 40 объемных частей раствора по 4.2.13 и 60 объемных частей раствора по 4.2.14).
Срок хранения раствора - 7 дней при комнатной температуре.
4.2.17 Папаин порошкообразный (CAS 9001-73-4) с удельной каталитической активностью 15 нкат/мг* по отношению к этиловому эфиру N-бензоил-L-аргинина (ВАЕЕ) при рН 6, 2 и 25°С. Удельная каталитическая активность 15 нкат/мг соответствует 1 МЕ/мг (ME - международная единица каталитической активности).
4.2.18 Раствор папаина массовой концентрации 20 г/ дм3
4.2.18.1 Приготовление раствора
1 г порошкообразного папаина (4.2.17) растворяют в 50 см3 цитратного буферного раствора (4.2.10). Срок хранения раствора - 5 дней при 4°С.
4.2.18.2 Проверка активности папаина
Активность папаина может быть проверена путем приготовления второго экстракта (см. 6.2) с удвоенным количеством фермента. Найденное содержание биотина должно соответствовать расчетному значению и ни в коем случае не превышать его.
Примечание - При межлабораторных сравнительных испытаниях был использован порошкообразный папаин, поставщиком которого была компания VWR International GmbH, Hilpertstraβe 20a, 64295 Darmstadt, Ref.-Nr26.146.180t.**
4.2.19 Конъюгат Авидин - флуоресцеинизотиоцианат (Avidin-FITC), содержащий 80% протеина (от 2 до 4 моль флуоресцеинизотиоцианата на каждый моль авидина).
4.2.20 Исходный раствор для послеколоночной дериватизации массовой концентрации ρ(Avidin-FITC) = 50 мг/см3
2, 5 мг конъюгата авидин - флуоресцеинизотиоцианат (4.2.19) растворяют в 50 см3 фосфатного буферного раствора с рН 7, 0 (4.2.16). Срок хранения раствора - 14 дней при 4°С.
4.2.21 Рабочий раствор для послеколоночной дериватизации массовой концентрации ρ(Avidin-FITC) = 2 мг/см3
25 см3 исходного раствора для послеколоночной дериватизации (4.2.20) смешивают с 600 см3 фосфатного буферного раствора с рН 7, 0 (4.2.16). Полученный раствор фильтруют через фильтр с размером пор 0, 45 мкм (5.5). Раствор устойчив при хранении в темноте в течение 8 ч.
4.2.22 Подвижная фаза для ВЭЖХ
80 объемных частей фосфатного буферного раствора с рН 6, 0 (4.2.15) смешивают с 20 объемными частями метанола (4.2.1) и фильтруют через фильтр с размером пор 0, 45 мкм (5.5).
4.2.23 Така-диастаза, выделенная из Aspergillus Oryzae, удельная каталитическая активность 1500 нкат/мг (соответствует 100 МЕ/мг), для проб с высоким содержанием крахмала.
4.3 Образцы сравнения
4.3.1 Общие положения
D-биотин и D-биоцитин могут быть приобретены у разных поставщиков. Необходимо убедиться в том, что пики D-биотина и D-биоцитина разделяются до базовой линии на хроматограмме раствора их смеси. Массовая доля основного вещества в образце сравнения биотина может быть установлена в соответствии с методом Европейской Фармакопеи [6].
4.3.2 D-Биотин, массовая доля основного вещества w(C10H16N2O3S) не менее 99%.
4.3.3 D-Биоцитин, массовая доля основного вещества w(C16H28N4O4S) не менее 98%.
4.4 Исходные растворы
4.4.1 Приготовление исходного раствора D-биотина массовой концентрации ρ(C10H16N2O3S) = 100 мкг/см3
Приблизительно 10 мг образца сравнения D-биотина (4.3.2), взвешенного с погрешностью ±0, 1 мг, растворяют в 100 см3 дистиллированной воды. Растворение может продолжаться от 4 до 5 ч. Срок хранения раствора - 2 мес при минус 18°С.
4.4.2 Приготовление исходного раствора D-биоцитина массовой концентрации ρ(C16H28N4O4S) = 100 мкг/см3
Приблизительно 10 мг образца сравнения D-биоцитина (4.3.3), взвешенного с погрешностью ±0, 1 мг, растворяют в 100 см3 дистиллированной воды. Срок хранения раствора - 2 мес при минус 18°С.
4.5 Стандартные растворы
4.5.1 Стандартные растворы D-биотина массовой концентрации ρ(C10H16N2O3S) от 0, 05 до 0, 30 мкг/см3
Приготавливают промежуточный раствор D-биотина путем разбавления 1 см3 исходного раствора (4.4.1) до 10 см3 дистиллированной водой. Затем готовят шесть градуировочных растворов, разбавляя 0, 5; 1, 0; 1, 5; 2, 0; 2, 5 и 3, 0 см3 промежуточного раствора до 100 см3 дистиллированной водой. Срок хранения растворов 1 день.
4.5.2 Стандартный раствор D-биоцитина массовой концентрации ρ(C16H28N4O4S) = 0, 30 мкг/см3
Приготавливают промежуточный раствор путем разбавления 1 см3 исходного раствора (4.4.2) до 10 см3 дистиллированной водой. Затем 3, 0 см3 промежуточного раствора разбавляют до 100 см3 дистиллированной воды. Срок хранения раствора 1 день.
5 Аппаратура
5.1 Общие положения
При проведении испытания используют обычное лабораторное оборудование, в частности, следующее.
5.2 Термостат, поддерживающий температуру на уровне (37±2)°С.
5.3 Система для ВЭЖХ, состоящая из насоса, устройства для ввода проб, флуориметрического детектора, позволяющего проводить измерения при длине волны возбуждения 490 нм и длине волны регистрации 520 нм, и системы для сбора и обработки данных, например интегратора.
5.4 Обращенно-фазовые аналитические колонки, например LiChrosper® 100 RP-18 endcapped***
Приведенные ниже характеристики аналитической колонки обеспечивают разделение пиков аналитов до базовой линии:
a) длина колонки 250 мм;
b) внутренний диаметр 4, 0 мм;
c) размер частиц 5 мкм.
Допускается использовать колонки иных размеров и с иным размером частиц. При этом параметры разделения на таких колонках должны быть проверены, с тем чтобы гарантировать получение сопоставимых результатов. Критерием эффективности подходящих аналитических колонок является разделение пиков аналитов до базовой линии.
5.5 Устройства для фильтрования
Устройства для фильтрования подвижной фазы большого и малого размера, снабженные, например, фильтрами с размером пор 0, 45 мкм.
Примечание - Фильтрование подвижной фазы и растворов проб через мембранный фильтр с размером пор 0, 45 мкм перед применением или инжектированием продлевает срок жизни колонок.
5.6 Послеколоночный реактор, состоящий из системы для ввода реагента, например Т-образного смесителя со следующим за ним капиллярным реактором длиной 10 м, выполненным из политетрафторэтиленовой трубки внутреннего диаметра 0, 5 мм, смотанной по спирали диаметром 14 мм, изготовленной, например, по [7] (модель КОТ2). Капиллярные реакторы могут быть приобретены у компаний Супелко или MicroSolvTech***.
6 Проведение испытаний
6.1 Подготовка испытуемой пробы
Испытуемую пробу гомогенизируют. Грубые материалы размалывают в подходящей мельнице и тщательно перемешивают. Чтобы исключить длительное воздействие высоких температур, пробу предварительно охлаждают.
6.2 Экстракция
Пробу массой от 0, 5 до 10 г (что приблизительно соответствует содержанию D-биотина от 2 до 15 мкг) взвешивают с точностью до 1 мг и помещают в колбу Эрленмейера. К пробе добавляют 300 мм3 раствора глутатиона (4.2.11), 300 мм3 раствора ЭДТА (4.2.12), 30 см цитратного буферного раствора (4.2.10) и 3 см3 раствора папаина (4.2.18). При высоком содержании крахмала добавляют 100 мг така-диатазы (4.2.23). Смесь выдерживают в течение ночи в термостате при 37°С при постоянном перемешивании. После охлаждения раствор переносят в мерную колбу вместимостью 50 см3 и разбавляют дистиллированной водой до метки. Раствор перемешивают и фильтруют через бумажный фильтр. Перед вводом в хроматограф его фильтруют еще раз через фильтр с размером пор 0, 45 мкм (5.5).
Примечание - Фильтрование как подвижной фазы, так и растворов проб через мембранный фильтр перед применением или вводом в хроматограф продлевает срок службы колонок.
6.3 Проведение хроматографического анализа
Дозируют в ВЭЖХ-систему равные объемы градуировочных растворов и растворов проб. D-биотин идентифицируют путем сравнения времен удерживания пика на хроматограмме раствора пробы и градуировочных растворов. Идентификацию пиков можно также осуществить при помощи добавки образца сравнения к раствору пробы.
Из-за ограниченной стабильности раствора для послеколоночной дериватизации (4.2.21) ее регулярно проверяют при проведении серии измерений путем ввода градуировочного раствора. Приведенные ниже условия обеспечивают разделение и количественное определение D-биотина:
Хроматографическая колонка: LiChrospher® 100 RP-18 endcapped, 5 мкм, 250 ˣ 4, 0 мм;
Подвижная фаза: 80 объемных частей фосфатного буферного раствора с рН 6 (4.2.15) и 20 объемных частей метанола (4.2.1);
Расход подвижной фазы: 0, 4 см3/мин;
Объем инжектирования: 30 мм3;
Флуоресцентное детектирование: длина волны возбуждения 490 нм, длина волны регистрации 520 нм;
Расход реагента для послеколоночной дериватизации: 1 см3/мин.
Примечание - Этот метод может быть также использован для оценки содержания D-биоцитина.
7 Обработка результатов
При использовании метода внешнего стандарта определяют площади или высоты пиков и затем устанавливают градуировочную характеристику, аппроксимируемую уравнением второго порядка.
Содержание D-биотина, w, мкг/100 г пробы, вычисляют по формуле (1):
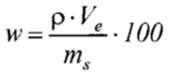
,
(1)
где ρ - массовая концентрация D-биотина в растворе пробы (6.2), мкг/см3, вычисленная при помощи градуировочной характеристики;
Ve - объем раствора пробы (6.2), см3;
ms - масса пробы, г;
100 - множитель для пересчета содержания D-биотина к 100 г пробы.
8 Прецизионность
8.1 Общие положения
Данные по прецизионности хроматографического метода определения D-биотина были получены согласно ИСО 5725-2 [1] в 2000 году в ходе межлабораторных сравнительных испытаний, организованных Генеральной комиссией по унификации методов анализа, Франция [3]. Все участники межлабораторных испытаний использовали градуировочные характеристики, установленные по трем точкам.
Полученные статистические данные приведены в приложении В.
8.2 Предел повторяемости
Абсолютная разность между двумя единичными результатами испытаний, полученными одним исполнителем на идентичном исследуемом материале на одном и том же оборудовании в течение возможно короткого промежутка времени, может превышать предел повторяемости r не чаще, чем в 5% случаев. Значения для D-биотина приведены ниже:
|
Мюсли
| 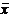 = 197 мкг/100 г = 197 мкг/100 г |
r = 25, 1 мкг/100 г
|
|
Питание для грудных детей (сухое молоко)
|
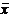 = 16, 0 мкг/100 г = 16, 0 мкг/100 г
|
r = 5, 24 мкг/100 г
|
|
Витаминизированный апельсиновый сок
|
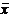 = 40, 7 мкг/100 г = 40, 7 мкг/100 г
|
r = 2, 51 мкг/100 г
|
|
Лиофилизированное пюре, зеленые овощи с
| | |
|
ветчиной
|
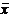 = 88, 9 мкг/100 г = 88, 9 мкг/100 г
|
r = 8, 99 мкг/100 г
|
|
Лиофилизированный куриный бульон
|
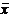 = 168 мкг/100 г = 168 мкг/100 г
|
r = 19, 4 мкг/100 г
|
8.3 Предел воспроизводимости
Абсолютная разность между двумя единичными результатами, полученными в двух лабораториях на идентичном исследуемом материале, может превышать предел воспроизводимости R не чаще, чем в 5% случаев. Значения приведены ниже:
|
Мюсли
|
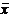 = 197 мкг/100 г = 197 мкг/100 г
|
R = 96, 7 мкг/100 г
|
|
Питание для грудных детей (сухое молоко)
|
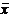 = 16, 0 мкг/100 г = 16, 0 мкг/100 г
|
R = 13, 5 мкг/100 г
|
|
Витаминизированный апельсиновый сок
|
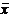 = 40, 7 мкг/100 г = 40, 7 мкг/100 г
|
R = 22, 8 мкг/100 г
|
|
Лиофилизированное пюре, зеленые овощи с
| | |
|
ветчиной
|
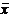 = 88, 9 мкг/100 г = 88, 9 мкг/100 г
|
R = 44, 1 мкг/100 г
|
|
Лиофилизированный куриный бульон
|
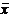 = 168 мкг/100 г = 168 мкг/100 г
|
R = 69, 5 мкг/100 г
|
9 Протокол испытаний
Протокол испытаний должен содержать, по меньшей мере, следующие сведения:
a) всю информацию, необходимую для идентификации пробы;
b) ссылку на настоящий стандарт или используемый метод;
c) результаты испытаний с указанием единиц измерений, в которых результат испытаний выражен;
d) дату и способ отбора проб (если он известен);
e) дату поступления пробы;
f) дату проведения испытаний;
g) все особенности, наблюдавшиеся при проведении испытаний;
h) любые применявшиеся операции, не оговоренные в методе или рассматриваемые как необязательные, которые могли повлиять на результат испытаний.
_______________________________
* Катал (кат) является производной единицей системы СИ для каталитической активности. 1 катал - это такая каталитическая активность, при которой скорость реакции при заданных условиях увеличивается на 1 моль/с.
** Эта информация приведена исключительно для удобства пользователя настоящего стандарта и не является поддержкой указанного поставщика. Могут быть использованы аналогичные продукты, если доказано, что их применение приводит к идентичным результатам.
*** Эта информация приведена только для удобства пользователя настоящего стандарта и не означает поддержки этих продуктов. Допускается использование аналогичных продуктов, если доказано, что их использование приводит к аналогичному результату.
Приложение А
(справочное)
Примеры хроматограмм
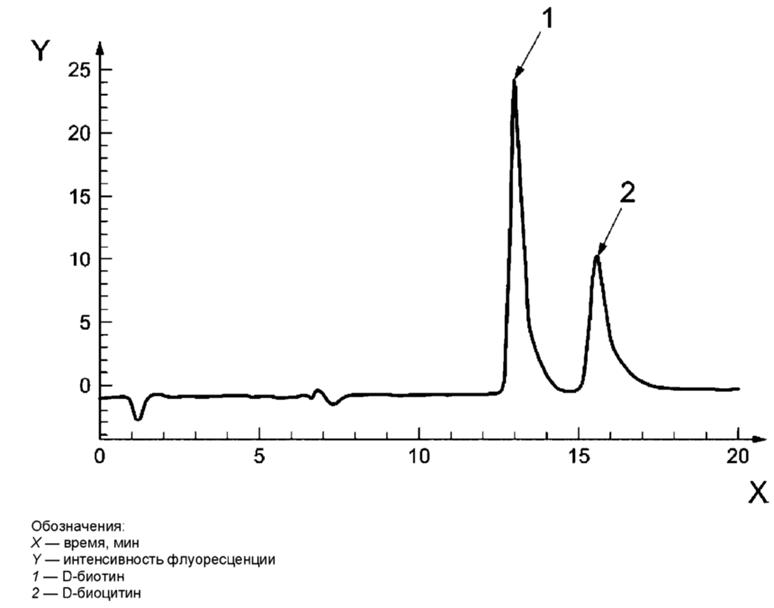
Рисунок А. 1 - Пример хроматографического разделения D-биотина и D-биоцитина в градуировочном растворе
Условия анализа:
Хроматографическая колонка: LiChrospher® 100 RP-18 endcapped, 5 мкм, 250 мм·4, 0 мм
Подвижная фаза: смесь восьми объемных частей фосфатного буферного раствора с рН 6 (4.2.15) и двух объемных частей метанола (4.2.1)
Расход подвижной фазы: 0, 4 см3/мин
Объем инжектирования: 30 мм3
Флуоресцентное детектирование: возбуждение при 490 нм, регистрация при 520 нм
Расход реагента для послеколоночной дериватизации: 1, 0 см3/мин
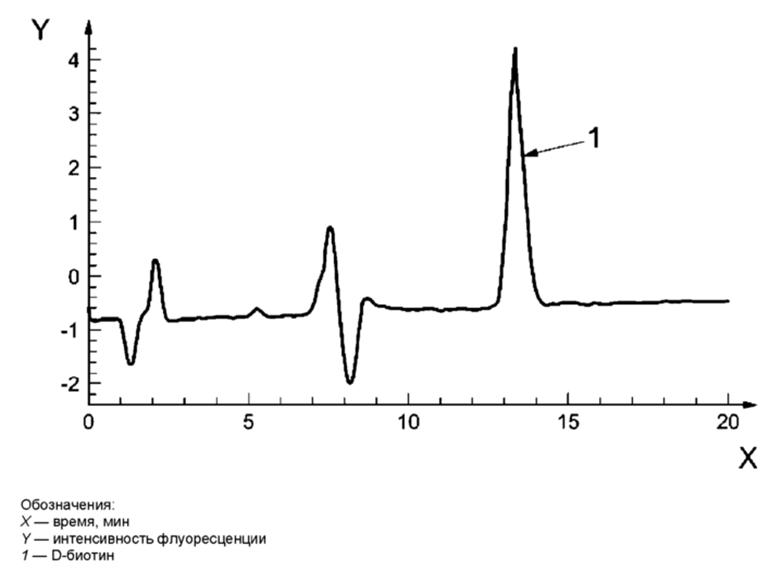
Рисунок А.2 - Пример хроматограммы D-биотина в пробе питания для грудных детей (сухое молоко)
Условия анализа:
Хроматографическая колонка: LiChrospher® 100 RP-18 endcapped, 5 мкм, 250 мм·4, 0 мм
Подвижная фаза: смесь восьми объемных частей фосфатного буферного раствора с рН 6 (4.2.15) и двух объемных частей метанола (4.2.1)
Расход подвижной фазы: 0, 4 см3/мин
Объем инжектирования: 30 мм3
Флуоресцентное детектирование: возбуждение при 490 нм, регистрация при 520 нм
Расход реагента для послеколоночной дериватизации: 1, 0 см /мин
Приложение В
(справочное)
Данные по прецизионности
Значения, приведенные в таблице В.1, были получены при межлабораторных сравнительных испытаниях, организованных в 2000 году Генеральной комиссией по унификации методов анализа, Франция [3], [8]. Эти испытания были проведены в соответствии со стандартом ИСО 5725-2 [1]. Все участники межлабораторных испытаний использовали градуировочные характеристики, установленные по трем точкам.
Таблица В.1 - Данные по прецизионности для проб мюсли, питания для грудных детей (сухое молоко), витаминизированного апельсинового сока, лиофилизированного пюре (зеленые овощи с ветчиной) и лиофилизированного куриного бульона
|
Проба
|
Мюсли
|
Питание для грудных детей (сухое молоко)
|
Витаминизированный апельсиновый сок
|
Лиофилизированное пюре (зеленые овощи с ветчиной)
|
Лиофилизированный куриный суп
|
|
Год проведения испытаний
|
2000
|
2000
|
2000
|
2000
|
2000
|
|
Число лабораторий
|
10
|
10
|
10
|
10
|
10
|
|
Число параллельных проб
|
2
|
2
|
2
|
2
|
2
|
|
Число лабораторий после исключения выбросов
|
10
|
9
|
10
|
10
|
10
|
|
Число лабораторий, результаты которых признаны выбросами
|
0
|
1
|
0
|
0
|
0
|
|
Число принятых результатов
|
20
|
18
|
20
|
20
|
20
|
|
Общее среднее 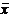 , мкг/100 г , мкг/100 г
|
197
|
16, 0
|
40, 7
|
88, 9
|
168
|
|
Стандартное отклонение повторяемости sr, мкг/100 г
|
8, 85
|
1, 85
|
0, 89
|
3, 18
|
6, 84
|
|
Относительное стандартное отклонение повторяемости RSDr, %
|
4, 5
|
11, 6
|
2, 2
|
3, 6
|
4, 1
|
|
Предел повторяемости r (r = 2, 8 sr), мкг/100 г
|
25, 1
|
5, 24
|
2, 51
|
8, 99
|
19, 4
|
|
Стандартное отклонение воспроизводимости sR, мкг/100 г
|
34, 2
|
4, 76
|
8, 05
|
15, 6
|
24, 6
|
|
Относительное стандартное отклонение воспроизводимости RSDR, %
|
7, 4
|
29, 8
|
19, 8
|
17, 5
|
14, 6
|
|
Предел воспроизводимости
R (R = 2, 8 sR), МКГ/100 Г
|
96, 7
|
13, 5
|
22, 8
|
44, 1
|
69, 5
|
|
Индекс Горвица [8]
|
1, 2
|
1, 4
|
1, 1
|
1, 1
|
1, 0
|
Приложение ДА
(справочное)
Сведения о соответствии межгосударственных стандартов ссылочным европейским региональным стандартам
Таблица ДА. 1
|
Обозначение и наименование европейского регионального стандарта
|
Степень соответствия
|
Обозначение и наименование межгосударственного стандарта
|
|
EN ISO 3696 Вода для лабораторного анализа. Технические требования и методы испытаний
|
-
|
*
|
|
* Соответствующий межгосударственный стандарт отсутствует. До его утверждения рекомендуется использовать перевод на русский язык данного европейского регионального стандарта. Перевод данного европейского регионального стандарта находится в Федеральном информационном фонде технических регламентов и стандартов.
|
Библиография
|
[1]
|
ISO 5725-2, Accuracy (trueness and precision) of measurement methods and results - Part 2: Basic method for the determination of repeatability and reproducibility of a standard measurement method
|
|
[2]
|
Lahely, S., Ndaw, S., Arella, F., Hasselmann, C: Determination of biotin in foods by high-performance liquid chromatography with post-column derivatization and fluorimetric detection, Food chem., 65, 253 - 258 (1999)
|
|
[3]
|
Arella, F., Deborde, J.L, Bourguignon, J.В., Bergaentlze, M., Ndaw, S., Hasselmann, C: Liquid chromatographic determination of biotin in foods. A collaborative study, Ann. Fals. Exp. Chim., 93. 951, 193 - 200 (2000)
|
|
[4]
|
Hentz. N.G., Bachas, L.G.: Class-selective detection systems for liquid chromatography based on the streptavidin-biotin interaction, Anal. Chem., 67, 1014 - 1018 (1995)
|
|
[5]
|
Przyjazny, A., Hentz, N.G., Bachas, L.G.: Sensitive and selective liquid chromatographic post-column reaction detection system for biotin and biocytin using an homogeneous fluorophore-linked assay, J. chromatogr., 654, 79 - 86 (1993)
|
|
[6]
|
European Pharmacopoeia 5.0, 01/2005:1073, Seite 110
|
|
[7]
|
Selavska, С.M., Jino. K.S., Krull, I.S.: Construction and comparison of open tubular reactors for post-column reaction detection in liquid chromatography. Anal. Chem., 59, 2221 - 2224 (1987)
|
|
[8]
|
Horwitz, W.: Evaluation of Analytical Methods used for Regulation of Foods and Drugs, Anal. Chem. 1982, 54 (1), 67A - 76A
|
![]() — Все документы — ГОСТы — ГОСТ EN 15607-2015 ПРОДУКТЫ ПИЩЕВЫЕ. ОПРЕДЕЛЕНИЕ D-БИОТИНА МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ
— Все документы — ГОСТы — ГОСТ EN 15607-2015 ПРОДУКТЫ ПИЩЕВЫЕ. ОПРЕДЕЛЕНИЕ D-БИОТИНА МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
 Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
 «МК»: в России не отменят льготную ипотеку
«МК»: в России не отменят льготную ипотеку
 Аренда квартир в Москве подешевела на 10 %
Аренда квартир в Москве подешевела на 10 %
 Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
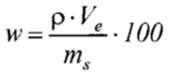 ,
,
