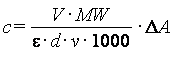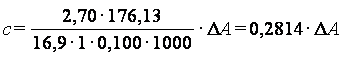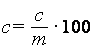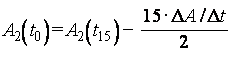Введен в действие приказом Федерального агентства по техническому регулированию и метрологии от 29 ноября 2012 г. N 1594-ст
Межгосударственный стандарт ГОСТ 31717-2012
"СОКИ И СОКОВАЯ ПРОДУКЦИЯ. ИДЕНТИФИКАЦИЯ. ОПРЕДЕЛЕНИЕ АСКОРБИНОВОЙ КИСЛОТЫ ФЕРМЕНТАТИВНЫМ МЕТОДОМ"
Juices and juice products. Identification. Determination of ascorbic acid by enzymatic method
Дата введения - 1 июля 2013 г.
Введен впервые
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 Подготовлен Государственным образовательным учреждением высшего профессионального образования "Московский государственный университет пищевых производств" Министерства образования Российской Федерации (ГОУ ВПО "МГУПП")
2 Внесен Федеральным агентством по техническому регулированию и метрологии
3 Принят Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 15 ноября 2012 г. N 42)
За принятие проголосовали:
|
Краткое наименование страны по МК (ИСО 3166) 004-97
|
Код страны
по МК (ИСО 3166) 004-97
|
Сокращенное наименование национального органа
по стандартизации
|
|
Беларусь
|
BY
|
Госстандарт Республики Беларусь
|
|
Киргизия
|
KG
|
Кыргызстандарт
|
|
Молдова
|
MD
|
Молдова-Стандарт
|
|
Россия
|
RU
|
Росстандарт
|
|
Таджикистан
|
TJ
|
Таджикстандарт
|
|
Узбекистан
|
UZ
|
Узстандарт
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 29 ноября 2012 г. N 1594-ст межгосударственный стандарт ГОСТ 31717-2012 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2013 г.
5 Настоящий стандарт подготовлен на основе применения ГОСТ Р 53139-2008
6 Введен впервые
1 Область применения
Настоящий стандарт распространяется на соки и соковую продукцию, включая соки и соковую продукцию для детского питания, в т.ч. фруктовые и овощные соки, нектары, морсы и сокосодержащие напитки, фруктовые и овощные пюре, а также на концентрированные фруктовые и овощные соки, концентрированные морсы, концентрированные фруктовые и овощные пюре и устанавливает метод ферментативного определения массовой концентрации аскорбиновой кислоты (витамина С) в виде кислоты или ее соли. Диапазон определения массовой концентрации аскорбиновой кислоты составляет от 0, 0003 до 0, 2 г/дм3 включительно.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие межгосударственные стандарты:
ГОСТ 245-76 Реактивы. Натрий фосфорнокислый однозамещенный 2-водный. Технические условия
ГОСТ 841-76 Реактивы. Кислота метафосфорная. Технические условия
ГОСТ 1625-89 Формалин технический. Технические условия
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 3652-69 Реактивы. Кислота лимонная моногидрат и безводная. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 24104-2001 Весы лабораторные. Общие технические требования
ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26313-84 Продукты переработки плодов и овощей. Правила приемки, методы отбора проб
ГОСТ 26671-85 Продукты переработки плодов и овощей, консервы мясные и мясорастительные. Подготовка проб для лабораторных анализов
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
ГОСТ 29227-91 (ИСО 835-2-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Обозначения и сокращения
В настоящем стандарте применены следующие сокращения и обозначения:
МТТ - бромид 3-(4, 5-диметилтиазол-2-ил)-2, 5-дифенил-2Н-тетразолия,
ФМС - переносчик электронов - феназинметосульфат,
МТТ - формазан - комплекс МТТ и формазана,
АО - аскорбатоксидаза.
4 Сущность метода
Аскорбиновая кислота (витамин С) и другие редуцирующие вещества (х – H2) восстанавливают бромид 3-(4, 5-диметилтиазол-2-ил)-2, 5-дифенил-2Н-тетразолия (МТТ) в присутствии переносчика электронов феназинметосульфата (ФМС) при рН 3, 5 до комплекса МТТ-формазана. В кювете с пробой измеряют сумму редуцирующих веществ:
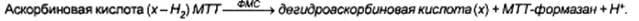
Для обеспечения специфичного определения аскорбиновой кислоты в контрольной кювете проводят окисление аналита аскорбатоксидазой (АО) в присутствии кислорода воздуха. Образующаяся дегидроаскорбиновая кислота не взаимодействует с МТТ и ФМС:
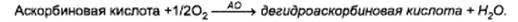
Количество образовавшегося комплекса МТТ-формазан, эквивалентное количеству аскорбиновой кислоты в исходной пробе, определяют спектрофотометрическим измерением оптической плотности исследуемого раствора пробы при длине волны 578 нм.
5 Отбор проб
5.1 Отбор проб - по ГОСТ 26313, подготовка проб - по ГОСТ 26671.
6 Проведение определения
6.1 Средства измерений, вспомогательные устройства, реактивы и материалы
Гидроокись калия по ГОСТ 24363, ч.д.а. раствор молярной концентрации с (КОН) = 10 моль/дм3.
Поливинилполипирролидон (код пищевой добавки Е1202) с содержанием основного вещества не менее 95%.
Фосфорнокислый однозамещенный 2-водный натрий, MaH2PO4·2H2O по ГОСТ 245, ч.д.а.
Лимонная кислота моногидрит, C6H8O7·H2O, по ГОСТ 3652, ч.д.а.
Аскорбиновая кислота, C6H8O6 х.ч.
Формалин по ГОСТ 1625, раствор с объемной долей 5%.
3-(4, 5-диметилтиазол-2-ил)-2, 5-дифенил-2Н-тетразолий бромид (МТТ) с содержанием основного вещества не менее 95%.
Феназинметосульфат (феназин/ФМС) с содержанием основного вещества не менее 95%.
Аскорбатоксидаза (сухой лиофилизат/АО), Е 1.10.3.3 с содержанием основного вещества не менее 95%.
Метафосфорная кислота, (HPO4)n, по ГОСТ 841, раствор массовой концентрации 15 г/дм3.
Дистиллированная вода по ГОСТ 6709.
Спектрофотометр, позволяющий проводить измерения при длине волны 578 нм, или фотометр фотоэлектрический с шириной спектральной полосы не более 10 нм и допустимой абсолютной погрешностью измерений не более ±1%, или спектрофотометр на ртутной лампе, позволяющий проводить измерения при 578 нм.
Кюветы из оптического стекла или полимерных материалов с длиной оптического пути 1 см.
Держатель для кювет.
Мономер или рН-метр с погрешностью измерения не более ±0, 05 рН.
Пипетки номинальной вместимостью 0, 01, 0, 02, 0, 1, 0, 2, 0, 5, 1, 2, 5 и 10 см3 с относительной погрешностью дозирования ±1% по ГОСТ 29227 1-го класса точности или дозаторы пипеточные с аналогичными или изменяемыми объемами доз с относительной погрешностью дозирования не более ±1% или импортные с аналогичными характеристиками.
Колбы мерные по ГОСТ 1770 вместимостью 100, 250 и 1000 см3.
Стаканы по ГОСТ 25336 вместимостью 20 и 200 см3.
Цилиндры по ГОСТ 1770 вместимостью 50 и 100 см3.
Лабораторная воронка по ГОСТ 25336 диаметром 5 см.
Часы лабораторные.
Электроплитка.
Термометр жидкостный стеклянный по ГОСТ 28498 для диапазона температур от 0°С до 100°С с пределом допускаемой погрешности не более ±1°С.
Весы лабораторные по ГОСТ 24104 с пределом допускаемой абсолютной погрешности однократного взвешивания не более ±0, 1 мг.
Шпатели пластиковые или палочки стеклянные оплавленные длиной от 8 до 10 см диаметром 2 - 3 мм для перемешивания содержимого кювет при проведении ферментативного определения.
Бумага фильтровальная лабораторная по ГОСТ 12026.
Водяной или воздушный термостат, обеспечивающий поддержание заданной температуры ферментативной реакции в диапазоне 30°С - 40°С и контроль температуры с погрешностью не более 0, 5°С.
Допускается применять другие средства измерений с метрологическими характеристиками, вспомогательные устройства с техническими характеристиками, а также реактивы, в том числе готовые наборы реактивов, по качеству не ниже перечисленных в настоящем разделе.
6.2 Приготовление растворов реактивов
6.2.1 Фосфатно-цитратный буферный раствор (натрий фосфорнокислый однозамещенный молярной концентрации 0, 2 моль/дм3, раствор моногидрата лимонной кислоты молярной концентрации 0, 1 моль/дм3, рН 3, 6)
Растворяют 35, 6 г натрия фосфорнокислого однозамещенного в мерной колбе вместимостью 1000 см3 в 500 см3 дистиллированной воды, полученной непосредственно перед приготовлением раствора реактива. После полного растворения реактива объем раствора в колбе доводят до метки дистиллированной водой.
Растворяют 21, 0 г лимонной кислоты моногидрата в мерной колбе вместимостью 1000 см3 в 500 см3 свежей дистиллированной воды. После полного растворения реактива объем раствора в колбе доводят до метки дистиллированной водой.
Для приготовления фосфатно-цитратного буферного раствора с рН 3, 6 смешивают 31, 6 части раствора натрия фосфорнокислого однозамещенного молярной концентрации 0, 2 моль/дм3 и 68, 4 части раствора моногидрата лимонной кислоты молярной концентрации 0, 1 моль/дм3.
Фосфатно-цитратный буферный раствор годен для применения в течение 1 мес при условии хранения при температуре 4°С. Перед использованием необходимо контролировать рН и температуру фосфатно-цитратного буферного раствора, значения которых должны составлять соответственно 3, 6 и 20°С - 25°С. Контроль температуры осуществляют термометром. При отклонении от требуемого значения рН фосфатно-цитратный буферный раствор готовят заново.
6.2.2 Рабочий раствор МТТ массовой концентрации 5 мг/см3
Растворяют 200 мг МТТ в 40 см3 фосфатно-цитратного буферного раствора с рН 3, 6 (см. 6.2.1). Объем рабочего раствора МТТ достаточен для проведения примерно 20 отдельных определений аскорбиновой кислоты (см. 6.4).
Рабочий раствор МТТ годен для применения в течение 1 мес при условии хранения при температуре 4°С (без доступа света!). Перед использованием необходимо контролировать рН и температуру рабочего раствора МТТ, значения которых должны составлять соответственно 3, 6 и 20°С - 25°С. Контроль температуры осуществляют термометром. При отклонении от требуемого значения рН рабочий раствор МТТ готовят заново.
6.2.3 Рабочий раствор ФМС массовой концентрации 0, 6 мг/см3
Растворяют 30 мг ФМС в 50 см3 дистиллированной воды, полученной непосредственно перед приготовлением раствора реактива и нагретой на электроплитке до 40°С - 50°С. Рабочий раствор ФМС годен для применения в течение 12 мес при условии хранения при температуре 4°С. Незначительно красное окрашивание, которое может появиться при хранении рабочего раствора ФМС, не влияет на результаты ферментативного определения аскорбиновой кислоты.
6.2.4 Рабочий раствор АО (1700 U/см3)
Навеску сухого лиофилизата, соответствующую активности фермента 1700 U, растворяют в 1, 0 см3 фосфатно-цитратного буферного раствора с рН 3, 6 (см. 6.2.1). Раствор готовят непосредственно перед использованием.
6.2.5 Раствор гидроокиси калия молярной концентрации с (КОН) = 10 моль/дм3
Растворяют 14, 03 г гидроокиси калия в мерной колбе вместимостью 250 см3 в 150 см3 дистиллированной воды, полученной непосредственно перед приготовлением раствора реактива. После полного растворения реактива объем раствора в колбе доводят до метки.
6.2.6 Раствор формалина с объемной долей 5%
В химический стакан на 20 см3 вносят 3 см3 раствора формалина с объемной долей формальдегида 35%. Добавляют 4 см3 дистиллированной воды. Раствор перемешивают стеклянной палочкой и используют для подготовки пробы согласно 6.3.3.
6.2.7 Раствор метафосфорной кислоты массовой концентрации (HPO4)n = 15 г/дм3
Растворяют 15 г метафосфорной кислоты массовой долей 33, 5% в мерной колбе вместимостью 1000 см3 в 500 см3 дистиллированной воды, полученной непосредственно перед приготовлением раствора реактива. После полного растворения реактива объем раствора в колбе доводят до метки.
6.3 Подготовка пробы
Концентрированные соки и пюре перед определением восстанавливают согласно нормативным документам свежей дистиллированной водой до содержания растворимых сухих веществ согласно нормативным документам для соответствующего вида продукции.
6.3.1 Прозрачные или мутные слабоокрашенные пробы
С помощью раствора гидроокиси калия (10 моль/дм3) проводят корректировку рН пробы до значения 3, 5 - 4, 0. В зависимости от количества аскорбиновой кислоты пробу разбавляют дистиллированной водой или раствором метафосфорной кислоты (15 г/дм3) согласно таблице 1.
Таблица 1
|
Массовая концентрация аскорбиновой кислоты в пробе(1), г/дм3
|
Разбавление
|
Фактор разбавления F
|
|
<0, 20
0, 20 - 2, 0
2, 0 - 20, 0
>20
|
-
1 + 9
1 + 99
1 + 999
|
1
10
100
1000
|
|
(1) Для оценки количества аскорбиновой кислоты используют документы, содержащие сведения о составе соков и соковой продукции [1].
|
Пробу, содержащую мутную взвесь, после разбавления фильтруют через бумажный складчатый фильтр. Для определения аскорбиновой кислоты используют визуально прозрачный слабоокрашенный фильтрат в количестве 0, 100 см3.
6.3.2 Прозрачные или мутные сильноокрашенные пробы
С помощью раствора гидроокиси калия молярной концентрации 10 моль/дм3 проводят корректировку рН пробы до значения 3, 5 - 4, 0. В зависимости от количества аскорбиновой кислоты пробу разбавляют дистиллированной водой или раствором метафосфорной кислоты массовой концентрации 15 г/дм3 согласно таблице 1.
Для удаления природных красящих пигментов к 10 см3 пробы добавляют 100 мг поливинилполипирролидона. Пробу перемешивают в течение 1 мин, затем фильтруют через бумажный складчатый фильтр. Для определения аскорбиновой кислоты используют визуально прозрачный слабоокрашенный фильтрат в количестве 0, 100 см3.
6.3.3 Подготовка проб, содержащих в повышенных количествах диоксид серы
К 10 см3 пробы добавляют одну каплю разбавленного раствора формалина объемной долей 5%. Пробу перемешивают и выдерживают 5 мин при комнатной температуре. Значение рН пробы при необходимости корректируют раствором гидроокиси калия (10 моль/дм3) и разбавляют согласно таблице 1. Мутные пробы дополнительно фильтруют (см. 6.3.1, 6.3.2). Сильноокрашенные пробы обрабатывают поливинилполипирролидоном согласно 6.3.2.
В определении по 4.5 используют от 0, 200 до 0, 500 см3 фильтрата.
6.4 Условия определения
Длина волны при фотометрическом измерении составляет 578 нм. Для измерения используют стеклянную кювету* с толщиной оптического слоя 1 см, равной ширине грани. Ферментативное определение проводят при температуре 37°С. Общий объем инкубационной смеси в кювете составляет 2, 70 см3.
Измерение оптической плотности инкубационной смеси проводят против воздуха (без кюветы в световом пути прибора). Проба в инкубационной смеси в кювете должна содержать от 0, 5 до 20 мкг аскорбиновой кислоты в 0, 1 - 1, 6 см3 пробы.
6.5 Ферментативное определение
Ферментативное определение аскорбиновой кислоты в пробе проводят по схеме дозирования и смешивания реактивов, приведенной в таблице 2. Если в определении используют иммобилизованную АО и готовые наборы реактивов, дозирование и смешивание реактивов проводят по схеме таблицы 3.
Таблица 2 - Схема дозирования и смешивания реактивов для ферментативного определения аскорбиновой кислоты
|
Дозирование в кювету
|
Контрольная проба
|
Проба
|
|
Рабочий раствор МТТ1(1) (см. 6.2.2)
Дистиллированная вода
Проба(2) (см. 6.3)
Рабочий раствор АО (см. 6.2.4)
|
1, 000 см3
1, 490 см3
0, 100 см3
0, 01 см3
|
1, 000 см3
1, 500 см3
0, 100 см3
-
|
|
Перемешивают. Помещают контрольную кювету и кювету с пробой в термостат при температуре 37°С. В течение 6 мин(3) интенсивно перемешивают содержимое кюветы с контрольной пробой пластиковой или стеклянной палочкой с целью насыщения инкубационной смеси воздухом (необходимое условие полного окисления аскорбиновой кислоты в контрольной пробе!). После выдержки в контрольной кювете и в кювете с пробой измеряют значение оптической плотности A1. Продолжают реакцию добавлением:
|
|
Рабочий раствор ФМС(4) (см. 6.2.3)
|
0, 100 см3
|
0, 100 см3
|
|
Перемешивают. Инкубируют (в темноте!) при температуре 37°С в течение 15 мин, после чего немедленно измеряют значение оптической плотности A2 в кювете с контрольной пробой и в кювете с пробой.
|
|
(1) Температура раствора должна составлять 37°С.
(2) Перед дозированием в кювету пипетку или наконечник дозатора следует ополоснуть фильтратом пробы (см. 6.3).
(3) При определении аскорбиновой кислоты в пробах, содержащих повышенные количества диоксида серы, время выдержки кюветы с контрольной пробой увеличивают до 10 мин.
(4) После внесения рабочего раствора ФМС кюветы изолируют от доступа света.
|
Таблица 3 - Схема дозирования и смешивания реактивов для ферментативного определения аскорбиновой кислоты при использовании иммобилизованной АО
|
Дозирование в кювету
|
Контрольная проба
|
Проба
|
|
Рабочий раствор МТТ (см. 6.2.2)
Дистиллированная вода
Проба (см. 6.3)
Иммобилизованная АО
|
1, 000 см3
1, 500 см3
0, 100 см3
Один шпатель
|
1, 000 см3
1, 500 см3
0, 100 см3
-
|
|
Перемешивают. Помещают контрольную кювету и кювету с пробой в термостат при температуре 37°С. В течение 6 мин интенсивно перемешивают содержимое кюветы с контрольной пробой шпателем с иммобилизованной АО с целью насыщения инкубационной смеси воздухом (необходимое условие полного окисления аскорбиновой кислоты в контрольной пробе!). После выдержки в контрольной кювете и в кювете с пробой измеряют значение оптической плотности A2. Продолжают реакцию добавлением:
|
|
Рабочий раствор ФМС (см. 6.2.3)
|
0, 100 см3
|
0, 100 см3
|
|
Перемешивают. Инкубируют (в темноте!) при температуре 37°С в течение 15 мин, после чего немедленно измеряют значение оптической плотности A2 в кювете с контрольной пробой и в кювете с пробой.
|
7 Обработка результатов измерений
Значение разницы между конечным и начальным значениями оптической плотности контроля и пробы рассчитывают по формуле
ΔA=(A2-A1)проб-(A2-A1)конт.
(1)
Значение разницы оптических плотностей ΔA должно составлять не менее 0, 100.
Искомую массовую концентрацию аскорбиновой кислоты в исходной пробе, г/дм3, рассчитывают по общей формуле
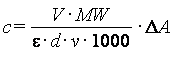 ;
;(2)
где V - общий объем инкубационной смеси, см3;
v - объем пробы, см3;
MW - молекулярный вес аскорбиновой кислоты или аскорбата (176, 13 и 175, 12 г/моль соответственно);
d - длина оптического пути кюветы, см;
ε- молярный коэффициент оптической плотности формазана (при измерении и длине волны 578 нм составляет 16, 9 дм3/ммоль·см).
Подставляя в формулу (2) необходимые значения для аскорбиновой кислоты, получают модифицированную формулу (3) для расчета массовой концентрации аскорбиновой кислоты (в г/дм3) в пробе:
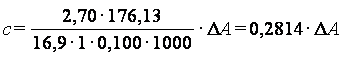 .
.(3)
Если перед ферментативным определением проба подвергалась разбавлению, то результат, полученный по формуле (3), умножают на коэффициент разбавления F.
В случае концентрированных соков или пюре результат определения выражают в г/100 г продукта. Расчет осуществляют с учетом навески, взятой для получения восстановленного продукта (см. 6.3), по формуле
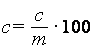 ,
,(4)
где с - массовая концентрация аскорбиновой кислоты в исследованной пробе, рассчитанная по формуле (2), г/дм3;
m - навеска концентрированного сока или пюре, взятая для получения восстановленного продукта (см. 6.3), г.
8 Дополнительные указания
8.1 Факторы, влияющие на определение
Если общая разница оптических плотностей ΔA менее 0, 100, то необходимо повторно провести определение, используя большую навеску или увеличенный объем пробы, дозируемой в инкубационную смесь (до 1, 490 см3 по схеме дозирования таблицы 2 или до 1, 500 см3 по схеме дозирования таблицы 3). В этом случае объем воды, добавляемой в кювету, должен быть уменьшен на соответствующее значение для сохранения общего объема инкубационной смеси (2, 70 см3) в кювете с неизменными контролем и пробой. Увеличенный объем пробы необходимо принимать во внимание при расчете конечного результата согласно формуле (3).
8.2 Специфичность определения
Метод специфичен для определения общей аскорбиновой кислоты, включающей D- и L-изомеры.
В анализе коммерческих препаратов аскорбиновой кислоты (например, витаминов) в свежеприготовленных растворах можно ожидать, что степень повторного нахождения искомого вещества составит 94% - 100%. На качество результатов определения степени повторного нахождения влияет срок хранения коммерческого препарата аскорбиновой кислоты и растворитель, используемый для получения растворов. Рекомендуется использовать раствор метафосфорной кислоты (см. 4.1) с доведением рН пробы до 3, 5 - 4, 0.
На стабильность аскорбиновой кислоты в водных растворах сильно влияет присутствие ионов металлов, например железа и меди, а также наличие в пробе кислорода. В этом случае ожидаемая степень повторного нахождения будет составлять менее 100%, что обусловливается частичной потерей аскорбиновой кислоты.
С помощью настоящего ферментативного метода нельзя определить L-аскорбилпальмитат, так как в ходе щелочного гидролиза происходит спонтанное разрушение свободной аскорбиновой кислоты.
8.3 Причины возможных ошибок при проведении определения
Сахароза, содержащаяся в соках и соковой продукции, не мешает определению, если ее концентрация в кювете не превышает 30 мг.
Определению аскорбиновой кислоты мешает D-сорбит (при концентрации более 20 мг в кювете), который ингибирует аскорбатоксидазу, а также этанол в высоких концентрациях, превышающих 100 мг/кювета. Влияние большинства мешающих факторов на результат определения исключается путем увеличения длительности инкубации контрольной пробы с аскорбатоксидазой до 10 мин.
Диоксид серы в высоких концентрациях, превышающих 50 мкг/кювета, взаимодействует с МТТ и ФМС и вызывает тем самым медленно текущую реакцию. В этом случае пробу подвергают предварительной обработке согласно 6.3.3.
Ионы металлов в концентрациях более 100 мкг/кювета могут понизить рН системы и, тем самым, ингибировать действие аскорбатоксидазы.
Нитрит, который может содержаться в некоторых овощных соках, не мешает определению. Однако его присутствие в системе может привести к спонтанному распаду аскорбиновой кислоты.
Ионы оксалата в концентрациях от 30 мкг/кювета способны оказывать значительное ингибирующее действие на аскорбатоксидазу. Высокую концентрацию оксалата устраняют путем добавления ионов кальция до концентрации 30 мкг/кювета и выше, а также созданием в системе слабокислой среды (рН 5 - 6).
8.4 Выявление и устранение мешающих факторов при проведении анализа. Контроль ферментативного определения
8.4.1 Общие указания
Если разница оптических плотностей ΔA менее 0, 100, следует провести повторную подготовку пробы к определению, увеличив ее навеску или уменьшив разбавление. Значение рН пробы в любом определении должно находиться в интервале от 3, 5 до 4, 0.
8.4.2 Операции с контрольной пробой
Содержимое кюветы с контрольной пробой интенсивно перемешивают стеклянной или пластиковой палочкой (или шпателем с иммобилизованной AO2) в течение предварительной реакции.
После внесения рабочего раствора ФМС реакция проявляет повышенную чувствительность к свету, поэтому инкубирование при температуре 37°С необходимо проводить в полной темноте. Для чего кюветы, находящиеся, например, в держателе, помещенном в водяной или воздушный термостат, накрывают плотной светонепроницаемой тканью. Попадание света приводит к возникновению нежелательной медленно текущей реакции.
В случае медленно текущей реакции, вызванной попаданием света, значение оптической плотности A2 системы определяют в соответствии с рекомендациями 6.4.5. Так как кюветы с пробой и контрольной пробой содержат одинаковый объем инкубационной смеси, медленно текущие реакции в них идентичны. От экстраполяции в этом случае можно отказаться. Однако необходимо принимать во внимание, что оптическую плотность A2 в кювете с контрольной пробой и в кювете с пробой необходимо измерять непосредственно одну за другой.
Если разница оптических плотностей (A2-A1) контрольной пробы менее 0, 020, то следует соблюдать следующие правила: рабочий раствор МТТ должен храниться в темноте; при использовании рабочего раствора МТТ его нельзя подвергать прямому облучению солнечным или электрическим светом; содержимое кюветы с контрольной пробой необходимо интенсивно перемешивать стеклянной или пластиковой палочкой (или шпателем с иммобилизованной АО) с целью насыщения инкубационной смеси воздухом; после внесения в инкубационную смесь рабочего раствора ФМС кюветы с контрольной пробой и пробой защищают от солнечного или электрического света.
8.4.3 Стабильность аскорбиновой кислоты
Водные растворы аскорбиновой кислоты нестабильны. При анализе твердых проб рекомендуется проводить выделение аскорбиновой кислоты раствором метафосфорной кислоты концентрации 15 г/дм3. После экстрагирования рН вытяжки корректируют раствором гидроокиси калия (10 моль/дм3) до 3, 5 - 4, 0.
Для стабилизации аскорбиновой кислоты не рекомендуется применять растворы оксалатов, так как их ионы ингибируют аскорбатоксидазу.
Разбавление пробы дистиллированной водой или метафосфорной кислотой проводят непосредственно перед определением. В этом случае нет необходимости в проведении корректировки рН до 3, 5 - 4, 0.
8.4.4 Медленно текущие реакции
Из практики применения метода следует, что оптическая плотность инкубационной смеси может увеличиваться даже после окончания ферментативной реакции (возникает медленно текущая реакция). В этом случае расчет значения конечной оптической плотности проводят экстраполированием на момент внесения в инкубационную смесь рабочего раствора ФМС (см. 6.2.3).
Экстраполяцию проводят графическим способом или согласно следующей схеме: по истечении 15 мин после добавления в кюветы рабочего раствора ФМС (см. 6.2.3) проводят измерение оптической плотности (A2), измерения повторяют каждые две минуты до тех пор, пока приращение ΔA/Δt не будет принимать постоянные значения. Измерения останавливают и действительное значение конечной оптической плотности инкубационной смеси на момент внесения рабочего раствора ФМС (см. приложение А) рассчитывают по формуле
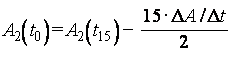 .
.(5)
Затем по формуле (1) рассчитывают значение разницы между значениями конечной и начальной оптической плотности контроля и пробы.
8.5 Контроль ферментативного определения
Контроль определения осуществляют при необходимости проверки качества реактивов, оценки уровня квалификации персонала лаборатории, осуществляющего анализ аскорбиновой кислоты, а также для выявления и устранения случайных и систематических ошибок определения.
8.5.1 Приготовление стандартного раствора аскорбиновой кислоты
Берут навеску в 200 мг аскорбиновой кислоты и количественно переносят ее в мерную колбу вместимостью 100 см3. Объем раствора в колбе доводят до метки метафосфорной кислотой (15 г/дм3), затем тщательно перемешивают. Переносят 10 см3 приготовленного раствора в другую мерную колбу вместимостью 100 см3, затем доводят объем раствора до метки метафосфорной кислотой (15 г/дм3). Содержимое колбы тщательно перемешивают.
Стандартный раствор аскорбиновой кислоты стабилен в течение суток при температуре 20°С, в течение трех дней при температуре 4°С и в течение одной недели при минус 20°С. В схемах дозирования и определения (таблицы 2, 3 и 4) допускается использовать в качестве внешнего стандарта только свежеприготовленный стандартный раствор аскорбиновой кислоты.
8.5.2 Применение стандартного раствора аскорбиновой кислоты в качестве внутреннего стандарта
Ферментативное определение с применением стандартного раствора аскорбиновой кислоты (см. 6.5.1) в качестве внутреннего стандарта проводят по следующей схеме дозирования (см. таблицу 4).
По формуле (1) рассчитывают разницу значений оптических плотностей для кювет "Проба + стандарт (внутренний)", "Стандарт (внешний)" и "Проба". Степень повторного нахождения (ПН, %) для аскорбиновой кислоты, содержащейся в стандартном растворе (см. 6.5.1), рассчитывают по формуле
 .
.(6)
Ферментативное определение проведено без ошибок, если степень повторного нахождения аскорбиновой кислоты находится в интервале от 95% до 100%.
Таблица 4 - Схема дозирования и смешивания реактивов для ферментативного определения с использованием раствора аскорбиновой кислоты в качестве внешнего и внутреннего стандарта (8.5.2)
|
Дозируют в кювету
|
Контрольная проба
|
Проба
|
Стандарт (контроль)
|
Стандарт (внешний)
|
Контроль
+
стандарт
(внутренний)
|
Проба
+
стандарт
(внутренний)
|
|
Рабочий раствор МТТ (см. 6.2.2)
|
1, 000 см3
|
1, 000 см3
|
1, 000 см3
|
1, 000 см3
|
1, 000 см3
|
1, 000 см3
|
|
Дистиллированная вода
|
1, 490(1) см3
(1, 500(2) см3)
|
1, 490(1) см3 (1, 500(2) см3)
|
1, 490(1) см3
(1, 500(2) см3)
|
1, 490(1) см3
(1, 500(2) см3)
|
1, 490(1) см3
(1, 500(2) см3)
|
1, 490(1) см3 (1, 500(2) см3)
|
|
Проба (см. 6.3)
|
0, 100 см3
|
0, 100 см3
|
-
|
-
|
0, 050 см3
|
0, 050 см3
|
|
Стандартный раствор аскорбиновой кислоты (см. 6.5.1)
|
-
|
-
|
0, 100 см3
|
0, 100 см3
|
0, 050 см3
|
0, 050 см3
|
|
Рабочий раствор АО (см. 6.2.4) или иммобилизованная АО
|
0, 010(1) см3
(один шпатель (2))
|
-
|
0, 010(1) см3
(один шпатель (2))
|
-
|
0, 010(1) см3
(один шпатель(2))
|
-
|
|
Рабочий раствор АО (см. 6.2.4) или иммобилизованная АО
|
0, 010(1) см3
(один шпатель (2))
|
-
|
0, 010(1) см3
(один шпатель(2))
|
-
|
0, 010(1) см3
(один шпатель(2))
|
-
|
|
Перемешивают. Помещают кюветы в термостат при 37°С. В течение 6 мин интенсивно перемешивают содержимое контрольных кювет с целью насыщения инкубационной смеси воздухом (необходимое условие полного окисления аскорбиновой кислоты!). После выдержки измеряют значение начальной оптической плотности A1. Продолжают реакцию добавлением:
|
|
Рабочий раствор ФМС (см. 6.2.3)
|
0, 100 см3
|
0, 100 см3
|
0, 100 см3
|
0, 100 см3
|
0, 100 см3
|
0, 100 см
|
|
Перемешивают. Инкубируют (в темноте!) при температуре 37°С в течение 15 мин, после чего немедленно измеряют значение конечной оптической плотности A2.
|
|
(1) При использовании рабочего раствора АО (см. 6.2.4).
(2) При использовании иммобилизованного препарата АО (например, шпателя с иммобилизованной АО).
|
8.6 Граница чувствительности метода
Граница чувствительности метода составляет 0, 30 мг/дм3 при ΔA = 0, 015 (при 578 нм) и максимальном объеме пробы v в 1, 490 (или 1, 600) см3.
8.7 Линейность определения
Линейность определения сохраняется в интервале от 0, 5 мкг аскорбиновой кислоты в кювете (0, 3 мг аскорбиновой кислоты/дм3 пробы; объем пробы - v = 1, 600 см3) до 20 мкг аскорбиновой кислоты в кювете (0, 2 г аскорбиновой кислоты/дм3 пробы; объем пробы v = 0, 100 см3).
9 Метрологические характеристики метода
В параллельном определении возможны различия между значениями оптических плотностей, которые будут составлять от 0, 005 до 0, 010. Это соответствует объему пробы v = 0, 100 см3 и концентрации аскорбиновой кислоты от 1, 5 до 3 мг/дм3. При использовании в определении навески пробы в 1 г/100 см3 (= 10 г/дм3) ожидаемые различия между параллельными определениями составят 0, 015 - 0, 030 г/100 г. Метрологические характеристики метода приведены в приложении Б.
_____________________________
* Вместо кювет из оптического стекла допускается использование одноразовых кювет из полимерных материалов.
Приложение A
(справочное)
Информация о медленно текущих реакциях
Ферментативные реакции в большинстве случаев являются реакциями нулевого порядка. Основная реакция характеризуется высокой скоростью. Для побочной - медленно текущей реакции - характерны низкие скорости. С практической точки зрения начало основной реакции связано с началом побочной реакции нулевого порядка. Характерным признаком медленно текущей реакции является постоянное количественное изменение оптической плотности с течением времени. Для получения достоверных результатов значение имеет только основная реакция. Концентрацию искомого вещества (субстрата в основной реакции) рассчитывают на основе количественной разницы между значением оптической плотности суммарной реакции (основная + медленно текущая реакции) и значением оптической плотности медленно текущей реакции.
Медленно текущая реакция начинается в отправной точке суммарной реакции (рисунок А.1). В этот момент времени в инкубационной смеси отсутствуют продукты ферментативной реакции, в том числе продукты медленно текущей реакции, которые могли бы привести к изменению оптической плотности системы. Для количественного определения общей разницы оптических плотностей значение конечной оптической плотности инкубационной смеси экстраполируют на момент начала основной реакции - внесение фермента или добавление рабочего реактива (рабочего раствора ФМС в ферментативном определении аскорбиновой кислоты). Контроль медленно текущей реакции позволяет получить только один количественный результат - значение оптической плотности в начальной точке суммарной реакции (основная + побочная реакции). Присутствие в инкубационной смеси медленно текущей реакции регистрируют с момента завершения основной реакции.
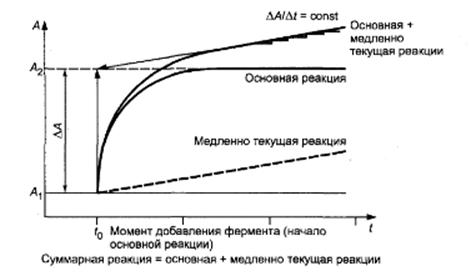
"Рисунок А.1 - Графическое определение конечной оптической плотности инкубационной смеси, в которой присутствует медленно текущая реакция"
Приложение Б
(справочное)
Метрологические характеристики метода
Метрологические характеристики метода, полученные в трех лабораториях, приведены в таблицах Б.1 и Б.2.
Таблица Б.1
|
Показатель
|
В одной серии определений
(количество измерений в серии n = 15)
|
|
Лаборатория 1
|
Лаборатория 2
|
Лаборатория 3
|
|
Среднеарифметическое значение (х), г/дм3
|
0, 059
|
0, 192
|
0, 380
|
|
Среднеквадратичное отклонение повторяемости результатов определения (sr), г/дм
|
0, 00142
|
0, 00346
|
0, 00456
|
|
Коэффициент вариации, %
|
2, 4
|
1, 8
|
1, 2
|
Таблица Б.2
|
Показатель
|
В повторных сериях определений
(общее количество измерений n = 15)
|
|
Лаборатория 1
|
Лаборатория 2
|
Лаборатория 3
|
|
Среднеарифметическое значение (х), г/дм3
|
0, 059
|
0, 192
|
0, 380
|
|
Среднеквадратичное отклонение повторяемости результатов определения (sr), г/дм
|
0, 00224
|
0, 00422
|
0, 0076
|
|
Коэффициент вариации, %
|
3, 8
|
2, 2
|
2, 0
|
Библиография
|
[1]
|
Свод правил для оценки качества фруктовых и овощных соков Ассоциации промышленности соков и нектаров из фруктов и овощей Европейского союза (Свод правил AIJN) (издание на русском языке). - М.: Нововита. - 2004
|
![]() — Все документы — ГОСТы — ГОСТ 31717-2012 СОКИ И СОКОВАЯ ПРОДУКЦИЯ. ИДЕНТИФИКАЦИЯ. ОПРЕДЕЛЕНИЕ АСКОРБИНОВОЙ КИСЛОТЫ ФЕРМЕНТАТИВНЫМ МЕТОДОМ
— Все документы — ГОСТы — ГОСТ 31717-2012 СОКИ И СОКОВАЯ ПРОДУКЦИЯ. ИДЕНТИФИКАЦИЯ. ОПРЕДЕЛЕНИЕ АСКОРБИНОВОЙ КИСЛОТЫ ФЕРМЕНТАТИВНЫМ МЕТОДОМ Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
Городом с самыми дешевыми квартирами в новостройках оказался Воронеж
 Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
Аналитик Гутман: период с мая по июль является лучшим периодом для продажи дачи
 «МК»: в России не отменят льготную ипотеку
«МК»: в России не отменят льготную ипотеку
 Аренда квартир в Москве подешевела на 10 %
Аренда квартир в Москве подешевела на 10 %
 Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов
Вице-премьер Хуснуллин: ставка по ипотеке должна быть пять процентов